
- •Глава 18. Электрохимические элементы
- •18.1. Электрохимические элементы. Электродвижущая сила
- •18.2. Термодинамика электрохимических элементов
- •18.3. Эдс как сумма скачков потенциалов
- •18.4. Двойной электрический слой
- •18.4.1. Электрокапиллярные явления
- •18.5. Электродные потенциалы
- •18.6.Типы электродов
- •18.6.1. Электроды первого рода
- •18.6.2. Электроды второго рода
- •18.6.3. Окислительно-восстановительные электроды
- •18.6.4. Мембранные электроды
- •Стеклянные электроды.
- •Другие ионоселективные электроды.
- •18.7. Типы электрохимических цепей
- •18.7.1.Химические цепи без переноса.
- •18.7.2. Концентрационные цепи без переноса
- •18.7.3. Химические цепи с переносом
- •18.7.4. Концентрационные цепи с переносом
- •18.7.5. Диффузионные потенциалы
- •18.8. Потенциометрия
- •18.8.1. Определение коэффициентов активности электролитов
- •18.8.2. Определение константы диссоциации слабой кислоты
- •18.8.3. Определение рН растворов
- •18.8.4. Определение произведения растворимости
- •18.8.5. Потенциометрическое титрование
18.4.1. Электрокапиллярные явления
При погружении электрода в раствор образование ДЭС происходит самопроизвольно и, следовательно, сопровождается уменьшением потенциальной энергии поверхности электрода и ионов в растворе. Это изменение поверхностной энергии должно зависеть от строения образующегося ДЭС. Меняя это строение за счет изменения потенциала электрода (наложением напряжения от внешнего источника тока), можно изменять поверхностную энергию электрода. При этом будет изменяться и межфазное (поверхностное) натяжение на границе раздела металл – раствор.
Межфазное натяжение меняется вследствие изменения строения ДЭС, т.е. изменения концентрации ионов, адсорбированных на поверхности электрода. Связь между , потенциалом и удельным зарядом (зарядом единицы поверхности) q на границе металл – раствор выражается первым уравнением Липпмана:
![]() . (18.27)
. (18.27)
Зависимость
от представляет
собой электрокапиллярную кривую.
Эта кривая имеет восходящую ветвь (q
> 0,
![]() > 0) и нисходящую ветвь (q < 0,
> 0) и нисходящую ветвь (q < 0,
![]() < 0); в точке максимума q = 0,
< 0); в точке максимума q = 0,
![]() = 0 (рис. 18.5). Потенциал, соответствующий
максимуму на электрокапиллярной кривой,
называется потенциалом нулевого
заряда. Форма электрокапиллярной
кривой, величина и положение максимума
зависит от состава раствора, наличия в
нем ПАВ (ионогенных или молекулярных),
органических и неорганических ионов с
различной способностью к адсорбции.
Потенциал нулевого заряда также сильно
зависит от природы металла.
= 0 (рис. 18.5). Потенциал, соответствующий
максимуму на электрокапиллярной кривой,
называется потенциалом нулевого
заряда. Форма электрокапиллярной
кривой, величина и положение максимума
зависит от состава раствора, наличия в
нем ПАВ (ионогенных или молекулярных),
органических и неорганических ионов с
различной способностью к адсорбции.
Потенциал нулевого заряда также сильно
зависит от природы металла.
Из электрокапиллярных кривых можно определить и дифференциальную емкость Сd двойного электрического слоя:
![]() .
(18.28)
.
(18.28)
Это уравнение известно под названием второго уравнения Липпмана.
Рис. 18.5.
Электрокапиллярные кривые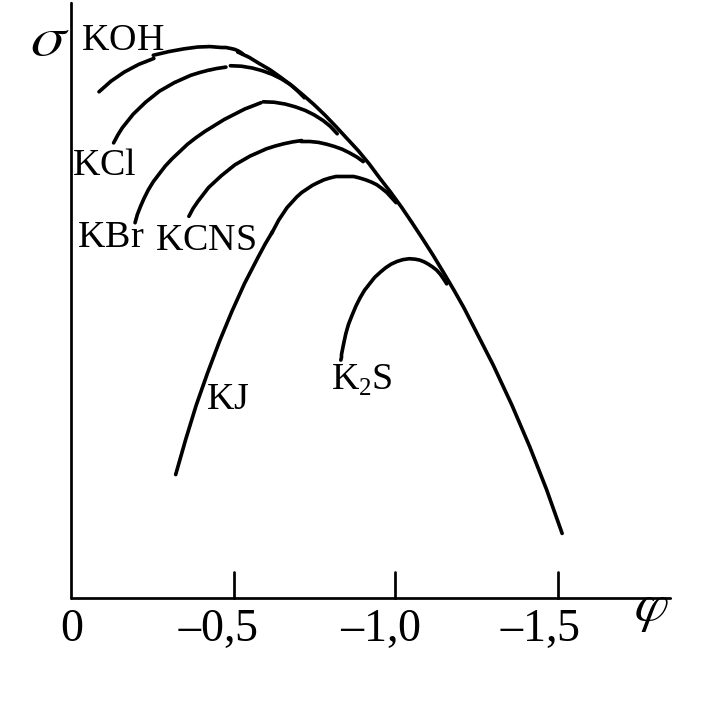
Рис. 18.6. Схема
капиллярного электрометра
Граница между электродом и раствором находится внутри капилляра, и за ее положением можно следить при помощи горизонтального микроскопа. Межфазное натяжение стремится переместить мениск ртути в более широкую часть капилляра, а сила тяжести действует в обратном направлении. Равновесие всех сил поддерживает мениск на определенном уровне. Изменение потенциала электрода или состава раствора приводит к изменению и перемещению границы раздела в капилляре. К первоначальному положению мениск можно привести изменением высоты ртути в трубке. При этом высота столба ртути h будет пропорциональна межфазному натяжению (h = k), а коэффициент пропорциональности k устанавливают, используя какой-либо стандартный раствор, для которого величина k определена другим методом.
