
- •Лекція №1 зміст, предмет та задачі дисципліни.
- •Лекція №2-4 природні α-амінокислоти. Будова класифікація стереоізомерія хімічні властивості
- •Лекція №5 білки. Загальні відомості, функції білків
- •Білки загальні відомості.
- •2. Функції білків,зміст білків в органах і тканинах
- •Лекція № 6-9. Фізико-хімічні властивості білків, їх структурна організація, класифікація білків
- •1. Фізико-хімічні властивості білків. Поняття структурної організації білків
- •2. Первинна й вторинна структура білка
- •3. Третинна й четвертинна структура білка
- •4. Класифікація білків, хімія простих білків, природні пептиди
- •Лекція № 10-12. Особливості білкового обміну, переварювання білків.
- •1. Особливості білкового обміну
- •2. Особливості переварювання білків, эндопептидазы
- •3. Переварювання білків у шлунку й кишечнику
- •4. Усмоктування продуктів гідролізу білків
- •Лекція № 13-15. Знешкодження аміаку в організмі, орнітіновий цикл, специфічні шляхи обміну амінокислот.
- •1. Знешкодження аміаку в організмі
- •2. Специфічні шляхи обміну амінокислот
- •Лекція № 16-18. Складні білки хромопротеины й нуклеопротеины
- •1. Визначення хромопротеинов. Гемо- і флавопротеины
- •2. Нуклеопротеины й липопротеины
- •3. Фосфопротеины й гликопротеины
- •Властивості імуноглобулінів людину
- •Лекція № 19-21. Хімічний склад і структура нуклеиновых кислот
- •1. Хімічний склад нуклеиновых кислот
- •2. Особливості структури нуклеиновых кислот
- •3. Первинна структура нуклеиновых кислот
- •4. Вторинна й третинна структура нуклеиновых кислот
2. Нуклеопротеины й липопротеины
Нуклеопротеины — складні білки, що містять у якості простетической групи нуклеиновые кислоти. У природі існує два типи нуклеопротеинов — рибонуклеопротеины (РНП) і дезоксирибонуклеопротеины (ДНП). Назви їх відбивають природу вуглеводу, що входить до складу нуклеиновых кислот, — у РНП це рибоза, у ДНП — лезоксирибоза. Переважна локалізація ДНП — у ядрі клітки, РНП — у цитоплазмі.
ДНК входить до складу мононуклеосом — складових частин хромосоми. ДНК і білкові молекули утворюють филаменты (нитки), товщина яких визначається білками, а довжина — молекулярною масою ДНК. Усього в хромосомах утримуються ДНК, п'ять класів білківигистонов і негистоновые білки. Кількість ДНК у ядрі становить до 6 X 10—12 г на одну клітку. Гистоны нуклеопротеинов представлені наступними класами:
Hl — багаті лізиному;
H2A — багаті аргініном і лізиному;H2B — помірковано багаті аргініном і лізиному;
H3 — багаті аргініном;
H4 — багаті аргініном і гліцином.
Негистоновые білки — кислі білки, до їхнього складу входять складні білки, ферменти й регуляторні білки. Кількість нуклеиновой кислоти в нуклеопротеинах коливається в межах 40—65% у про- і эукариот і не перевищує 2—5% від загальної маси нуклео- протеїнів у вірусів. Важливою особливістю нуклеопротеинов є їхня здатність до повного відновлення структури й функції після роз'єднання білка й нуклеиновой кислоти.
Липопротеины — складні білки, простетическая група яких представлена яким-небудь ліпідом (нейтральними жирами, жирними кислотами, фосфоліпідами або холестеридами).
Липопротеины входять до складу клітинної мембрани, біомембран ядра й мітохондрій, мікросом, присутні у вільному стані в плазмі крові. Липопротеины беруть участь в організації миелиновых оболонок, нервової тканини, хлоропластів, фоторецептор- ний і электронно-транспортой систем і ін. Липопротеины синтезуються в печінці й у слизуватій оболонці кишечнику. Вони складаються з гідрофобного ліпідного ядра, покритого гідрофільними ліпіду- мі, і білкової оболонки, що полягає з апобелков (апо-AI, AII, B, CI, CII, CIII, D і E). Можуть містити до 5% білків (таких як глюкоза, галактоза, гексозамины, фукоза, сиаловая кислота). Залежно від щільності при ультрацентрифугировании розрізняють липопротеины дуже низької щільності (ЛПОНП), низької щільності (ЛПНП), високої щільності (ЛПВП) і дуже високої щільності (ЛПОВП). При электрофорезе виділяється також фракція хиломикронов. Білковий компонент зв'язується з ліпідами за допомогою нековалент- ных сил різної природи. Якщо простетической групою є фосфоліпіди, то вони зв'язуються з білком іонним зв'язком.
3. Фосфопротеины й гликопротеины
Фосфопротеины — складні білки, що містять у якості простетической групи залишок фосфорної кислоти. До них ставляться казеиноген молока, вителлин, втиеллинин і фосвитин жовтка курячого яйця, овальбумин білка курячого яйця, ікри риб і ін. Фосфорна кислота зв'язується з білком сложноэфирной зв'язком через OhпГрупи Р-оксиаминокислот (серина й треонина).
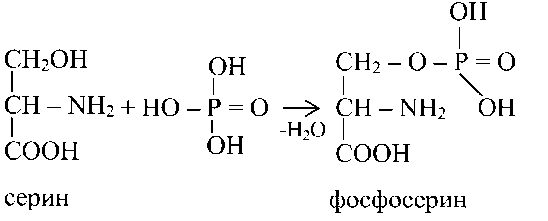
Фосфопротеины містять органічно зв'язаний фосфат, необхідний для нормальної життєдіяльності клітки. Вони також є енергетичним і пластичним матеріалом клітки.
Гликопротеины — складні білки, що містять у якості простетической групи гетероолигосахариды.
Гликоконъюгат — ковалентно зв'язані вуглеводний компонент (гликановая фракція) і білковий компонент (агликановая фракція).
Гликановая фракція складається з 2—15 мономерів гексоз (галактози, маннозы або глюкози) або пентоз (ксилозы, арабинозы) і кінцевого вуглеводу ( NнАцетилгалактозамина, L-фукозы або сиаловой кислоти).
Білки із гликановой фракцією з'єднані за допомогою OыГликозидных (з OhаГрупами серина, треонина й оксилизина), NыГликозидных (з амидными групами аспарагина, глутамина або ω-Ν-групами лізина й аргініну) і ефірних гликозидных зв'язків (з вільними CoohпГрупами глутаминовой і аспарагінової кислот).
Синтез гликопротеинов відбувається в рибосомах ендоплазматичної мережі, потім іде постсинтетическое гликозилирование, при якім олигосахаридная частина, з'єднана з ліпідним переносником долихолфосфатом, переноситься на поліпептидний ланцюг.
Інтерферони — гликопротеины, ингибирующие розмноження вірусів.
Розрізняють α-, β-, і γнінтерферони, що утворюються в клітці у відповідь на впровадження вірусів. Імуноглобуліни — це гликопротеины, що виконують захисну функцію: вони знешкоджують антигени будь-якої хімічної природи. Синтезуються в плазмоцитах.
Розрізняють п'ять класів імуноглобулінів: Igg, Igm, Iga, Igd і Ige.
Таблиця 1
