
- •Часть 2
- •3. Металлургия магния Свойства и области приминения магния.
- •Удельная теплоемкость жидкого магния, Дж/моль:
- •Применение
- •Минералы магния
- •Обезвоживание хлорида магния (бишофита)
- •Обезвоживание карналлита
- •Поэтому процесс ведут в две стадии
- •Хлорирование окиси магния
- •Технологические схемы Карналитовая схема
- •Магнезитовая схема
- •Смешанная схема
- •Печь кс
- •Печь скн (Рис 19, 20.)
- •Хлоратор
- •Сравнение скн и хлоратора
- •3.1.Основы электрометаллургии магния Физико-химические свойства электролитов
- •Состав используемых электролитов
- •Показатели электролиза
- •Электродные процессы. Катодные процессы.
- •Анодные процессы
- •Процессы в объеме электролита
- •Влияние различных факторов на выход по току.
- •Конструкции магниевых электролизеров. Общие сведения.
- •Диафрагменные электролизеры
- •Диафрагменный электролизер с верхним вводом анодов.
- •Диафрагменный электролизер с боковым вводом анодов
- •Диафрагменный электролизер с нижним вводом анода
- •Общие плюсы диафрагменных (относительно бездиафрагменных)
- •Общие минусы
- •Бездиафрагменный электролизер
- •Технология электролиза Питание электролизера
- •Извлечение шлама
- •Извлечение магния
- •Регулировка температуры
- •Отсос газа из электролизера
- •Поточная технология электролиза карналлита
- •3.2. Рафинирование магния
- •3.3. Производство магния термическими способами
Хлоратор
Аппарат для получения безводного карналлита хлорированием карналлита в расплаве в присутствии углерода рис.3.9.
Производительность 4-6 т/ч
Используемая хлоро-воздушная смесь – анодный газ магниевых электролизеров содержащий 75% хлора. При хлорировании в расплаве практически не остаётся воды, но окись магния хлорируется на 75%. Это необходимо для более полного использования хлора (с уменьшением концентрации окиси магния резко снижается). Остаток окиси магния 0,6-0,8% подавляет хлорирование других окислов.
Сравнение скн и хлоратора
Производительность хлоратора, отнесенная к рабочему объему и площади выше в два и более раза, чем у СКН. Полезное использование хлорида магния из карналлита в хлораторе выше на 10-12%. Содержание хлорида магния достигает 52%, в СКН не превышает 49%. Удельный расход энергии в хлораторе на 10% ниже.
Недостатки: низкая степень использования хлора, наличие в карналлите примеси углерода.
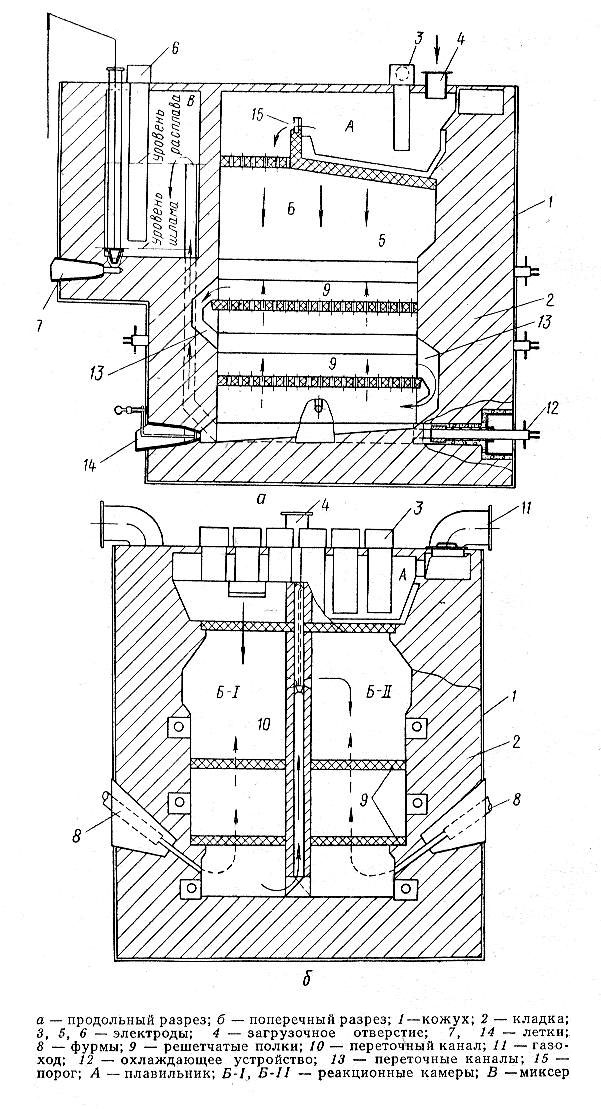
Рис.3.9. Хлоратор для хлорирования окиси магния.
3.1.Основы электрометаллургии магния Физико-химические свойства электролитов
Для любого электрохимического процесса важнейшее значение имеет состав электролита. Индивидуальные соли не обладают требуемым набором физико-химических свойств, поэтому применяют 3-х и 4-х компонентные смеси, где каждая соль приносит в электролит свои характерные свойства.
Электролит для получения магния должен обладать следующими свойствами:
1)_по возможности низкой температурой плавления,
2)_плотность выше плотности магния на 0,1-0,2 г/см3 при темп. электролиза,
3)_низкая летучесть, небольшая склонность к гидролизу,
4)_малая вязкость
5)_низкое содержание примесей влияющих на выход по току.
Поверхностные свойства электролита должны благоприятствовать хорошему покрытия катода магнием и слиянию мелких капель в крупные. Необходима относительно высокая электропроводность, и легкость получения электролита заданного состава.
Чистый MgCl2 как электролит не подходит (высокие Тпл, вязкость, упругость пара, низкая электропроводность, плохая смачиваемость, высокая склонность к гидролизу). Электролиз карналлита позволяет существенно снизить температуру. Карналит имеет более высокую электропроводность и смачиваемость, меньше упругость пара. Хлорид магния в карналлите крепко связан, меньше летит и гидролизуется, резко снижается шламообразование. Но двойные электролиты KCl-MgCl2 и NaCl-MgCl2 имеют и недостатки:
-по мере выработки MgCl2 (3-5%) резко увеличивается температура плавления. Чтобы этого не допускать, необходимо работать как минимум на 3-х компонентном электролите.
Добавка NaCl приводит к тому что за счет существования в системе NaCl-KCl эвтектики с Тпл 650ºС, даже при полной выработке хл. магния электролит остается жидким. Также увеличивается электропроводность, что позволяет снижать энергозатраты.
Однако добавки NaCl и KCl снижают удельный вес электролита, приближая его к удельному весу жидкого магния. Это создает трудности при разделении солевой и металлической фаз и отрицательно сказывается на выходе по току. Поэтому необходима добавка соли утяжелителя CaCl2 или BaCl2, но при этом увеличивается вязкость.
Привлекательными свойствами обладает LiCl. В системе LiCl-KCl есть эвтектика с Тпл=340ºС. Удельная электропроводность LiCl в 6 раз выше чем у MgCl2. Но при этом снижается удельный вес электролита, повышается гигроскопичность соли. Также LiCl имеет высокую стоимость.
Таблица 3.4. Свойства некоторых солей
|
Tпл,С |
Плотн, г/см3 |
Эл-пров,1/Ом·см |
Вязк, сП |
MgCl2 |
718 |
1,682 |
1,01 |
4,69 |
KCl |
770 |
1,539 |
2,42 |
1,42 |
NaCl |
801 |
1,549 |
3,54 |
1,49 |
LiCl |
606 |
1,501 |
5,86 |
1,82 |
BaCl2 |
958 |
3,12 |
1,93 |
- |
