
- •1. Содержание программы курса «Молекулярная физика»
- •6. Контрольные вопросы к экзамену
- •Уравнение теплопроводности и диффузии, зависящие от времени. Граничные и начальные условия. Расчет распределения тепла между пластинами, вокруг нагретой сферы и цилиндра.
- •Осмотическое давление. Кипение растворов с нелетучим и летучим компонентом.
- •1. Тесты на знание формул к экзамену.
- •Справочник для подготовки к экзамену и Интернет-экзамену по курсу «Молекулярная физика». Идеальные газы
- •Молярные массы некоторых газов.
- •Смеси идеальных газов.
- •Процессы в газах
- •Явления переноса в идеальных газах
- •Фазовые переходы и капиллярные явления.
- •9. Капиллярные явления.
Справочник для подготовки к экзамену и Интернет-экзамену по курсу «Молекулярная физика». Идеальные газы
1.
Давление р идеального газа на стенку
сосуда: р
= n
kT
=
 ,
,
Т-
температура, ,
 - скорость, m0
–масса молекулы газа.
- скорость, m0
–масса молекулы газа.
2. Уравнение состояния идеального газа p = nkT
Уравнение
Клайперона – Менделеева: ,
,
m –масса газа, М - молярная масса, - число молей; V- объем газа.
Молярной
массой М
вещества называется масса его 1 моля,
которая численно равна относительной
молекулярной массе
 его молекул, выраженной в килограммах:
М=
его молекул, выраженной в килограммах:
М=
 .
.
Молярные массы некоторых газов.
Газ |
относительная молекулярная масса (безразмерная величина) |
Молярная масса М |
Водород - H2 |
2 |
|
Гелий – He |
4 |
|
Аргон – Ar |
40 |
|
Кислород - O2 |
32 |
|
Азот - N2 |
28 |
|
Углекислый газ - CO2 |
44 |
|
Вода - H2O |
18 |
|
Смеси идеальных газов.
1.
В смеси идеальных газов для каждого
i-ого
газа можно записать уравнение Клайперона
– Менделеева
 .
.
Величина
 в данном уравнении называется парциальным
давлением.
в данном уравнении называется парциальным
давлением.
2.
Давление смеси газов на стенки сосуда
равно сумме парциальных давлений
компонент смеси : р
= - закон Дальтона.
- закон Дальтона.
3.Уравнение Клапейрона-Менделеева для смеси газов:

где
 -
эффективная молярная масса смеси газов.
-
эффективная молярная масса смеси газов.
 =
=
 =
=

где
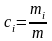 - массовая концентрация; а
- массовая концентрация; а
 - молярная концентрация i-ого
газа в смеси,
- молярная концентрация i-ого
газа в смеси,
 - суммарное число молей в смеси газов.
- суммарное число молей в смеси газов.
Функции распределения Максвелла:
1.
( )
=
)
=
 ;
dN/N
= dP
=
(
)d
-
;
dN/N
= dP
=
(
)d
-
относительное число молекул, скорость которых лежит в интервале
[ ; + d ] и вероятность dP этого явления.
2.
f(
)= ;
dN/N=
dP
=f(
)
d
-
относительное число молекул и вероятность
того, что компоненты
,
;
dN/N=
dP
=f(
)
d
-
относительное число молекул и вероятность
того, что компоненты
, и
и
 их скоростей меняются в интервалах:
[
;
+
d
];
[
;
+
d
];[
;
+
d
].
их скоростей меняются в интервалах:
[
;
+
d
];
[
;
+
d
];[
;
+
d
].
3.
F(
)=
 ;
dN/N
= dP
= F(
)d
-
;
dN/N
= dP
= F(
)d
-
относительное число молекул, модули скоростей которых лежат в интервале [ ; + d ] и вероятность этого явления.

F( )
F( )

Вид функции распределения Максвелла по скоростям F( )
.
Максимум функции распределения F( ) наблюдается при
наиболее
вероятной скорости молекул:
 .
При повышении температуры Т максимум
F(
)
смещается
в область более высоких скоростей и
уменьшается, поскольку площадь под
кривой должна оставаться постоянной
.
При повышении температуры Т максимум
F(
)
смещается
в область более высоких скоростей и
уменьшается, поскольку площадь под
кривой должна оставаться постоянной
 -
условие нормировки функции распределения.
-
условие нормировки функции распределения.
5.
Среднеквадратичная скорость молекул
:

6.
Среднеарифметическая скорость молекулы:


Функция распределения Больцмана:
n = no exp (- U/kT) , где U – потенциальная энергия частицы;
В гравитационном поле эта функция имеет вид: n=no exp (- m0 gh/kT) – для частиц массой m0 , либо n = no exp (- Mgh/RT) –для молекул газа с молярной массой М.
Термодинамические свойства и процессы в идеальных газах.
«0» начало термодинамики постулирует равенство температуры во всех частях системы, находящейся в состоянии термодинамического равновесия.
I
начало термодинамики является
обобщением закона сохранения энергии
на молекулярные системы:

где
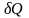 – бесконечно малое количество теплоты,
– бесконечно малое количество теплоты,
 – элементарная работа,
– элементарная работа,
 – бесконечно малое изменение внутренней
энергии системы.
– бесконечно малое изменение внутренней
энергии системы.
II
начало термодинамики накладывает
ограничение на процессы. По современной
формулировке в изолированной системе
возможны лишь процессы, при которых
энтропия не убывает: S
≥ 0. Для обратимых процессов изменение
энтропии S= и для таких процессов II
начало термодинамики записывается
в виде : TdS=
и для таких процессов II
начало термодинамики записывается
в виде : TdS= .
.
III начало термодинамики (теорема Нернста) сводится к двум утверждениям: 1) при приближении к абсолютному нулю энтропия стремится к определенному конечному пределу (этот предел полагается равным 0);
2) все процессы при абсолютном нуле температур идут без изменения энтропии.
Молярная теплоемкость С – количество теплоты, необходимое для нагревания 1 моля вещества на 1К: С = Q/( ν·dT).
Молярная теплоемкость при постоянном объеме Cv= iR/2;
при
постоянном
давлении:
Cp
=
(i+2)
R/2;
 (соотношение Майера), где i
– число степеней свободы молекул –
число независимых компонент энергии
молекулы в выражении для внутренней
энергии газа. Для одноатомной молекулы
i=3,
двухатомной
i=5,
состоящей из 3-х и более молекул
i=6.
(соотношение Майера), где i
– число степеней свободы молекул –
число независимых компонент энергии
молекулы в выражении для внутренней
энергии газа. Для одноатомной молекулы
i=3,
двухатомной
i=5,
состоящей из 3-х и более молекул
i=6.







