
ХИМИЯ НЕФТИ И ГАЗА для студентов
.pdf
vk.com/club152685050 | vk.com/id446425943
70
244. При сжигании органического вещества массой 31,2 г, плотность по воздуху которого равна 2,69, образовались диоксид углерода объемом
53,76 л и вода массой 21,6 г. Какова структурная формула этого вещества?
245.Получите этилбензол двумя способами. Напишите возможные пути его окисления.
246.Напишите уравнения реакций окисления раствором перманганата калия:
а) толуола; б) изопропилбензола; в) бутилбензола; г) о-ксилола.
247. Напишите формулы строения промежуточных и конечных продуктов в следующих схемах:
+ C H Br |
|
+ HNO3 |
|
+ KMnO4 |
|
||
2 |
5 |
A |
|
|
B |
|
C |
AlBr |
H SO |
|
o |
||||
|
4 |
|
t |
|
|||
|
3 |
|
2 |
|
|
|
|
248. Установите строение углеводорода C8H6, обесцвечивающего бромную воду, образующего белый осадок с аммиачным раствором окиси серебра, а
при окислении дающего бензойную кислоту. Напишите соответствующие уравнения реакций.
249. Установите строение ароматического углеводорода C8H10, при окислении которого получается фенилендикарбоновая кислота, а при нитровании — только одно мононитропроизводное.
250. С помощью каких реактивов и в каких условиях можно осуществить следующие превращения:
Cl |
Cl |
C Н |
C H |
COOH |
|
2 5 |
|||
|
2 |
5 |
|
251. Напишите структурные формулы соединений: а) пара-хлорбензол-
сульфокислота; б) 3-этилбензолсульфокислота; в) мета-толуолсульфохло-
рид; г) п-толуолсульфамид; д) м-сульфобензойная кислота.
252. Какие сульфокислоты получатся в результате сульфирования следующих соединений, учитывая ориентирующее влияние заместителей:

vk.com/club152685050 | vk.com/id446425943
71
а) |
Cl |
б) |
в) |
г) |
|
д) |
е) |
|
|
|
|
||||||
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
3 |
|
|
|
|
SO Н |
COOH |
C H |
NO |
2 |
|
|
|
|
|
2 |
5 |
|
||
|
|
|
3 |
|
|
|
|
|
Какая из указанных реакций сульфирования проходит легче, чем сульфирование бензола?
253. Проведите нитрование соединений: а) хлорбензола; б) этилбензола; в)
кумола; г) нитробензола; д) бензойной кислоты; е) фенола; ж) орто-
нитроэтилбензола. Какие из них нитруются легче, чем бензол? Почему?
254.Из бензола получите о-хлорбензойную кислоту.
255.Из бензола получите бензофенон.
256.Из анилина получите п-нитробензойную кислоту.
257.В каком объемном соотношении (в газовой фазе при н.у.) следует взять углеводороды метан и бензол, чтобы газ, выделившийся при разложении первого из них на элементы, полностью поглотился при определенных условиях вторым?
258.При пропускании 30,24 л ацетилена над углем в качестве катализатора
(при 650°С) образовалось вещество, горящее коптящим пламенем. Сколько
граммов вещества образовалось, если выход реакции составляет 80%?
259.При взаимодействии смеси этилового спирта и фенола с избытком бромной воды выделилось 33,1 г осадка. Такое же количество смеси может прореагировать с 13,8 г металлического натрия. Каков состав исходной смеси в граммах?
260.Основными процессами, протекающими при ароматизации нефти (ка-
талитическом риформинге), являются: 1) дегидрирование шестичленных нафтенов, 2) изомеризация пятичленных нафтенов в шестичленные с последующей дегидрогенизацией, 3) дегидроциклизация алканов и алкенов. Составьте схемы образования этими способами толуола.
261. Какие ароматические углеводороды могут образоваться при каталити-
ческом риформинге: 1)н-гептана, 2) метилциклогексана, 3) н-октана, 4)
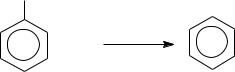
vk.com/club152685050 | vk.com/id446425943
72
метилциклопентана, 5) пропилциклопентана? В каких условиях проводят ароматизацию нефти?
262. Как можно получить бензол, исходя из следующих веществ: 1) цикло-
гексана, 2) циклогексадиена, 3) гексана, 4) бензоата натрия, 5) ацетилена,
б) фенола? Напишите уравнения реакций.
263. Одним из промышленных способов получения бензола является ката-
литическое деметилирование толуола в атмосфере водорода:
СН3
|
Ni / Al O |
3 |
|
+ Н |
2 |
+ CH |
|
|
|
||
2 |
|
|
4 |
Сколько килограммов бензола может быть получено этим способом из
460 кг толуола, если на практике выход бензола составляет 40%?
264.В результате каталитической гидрогенизации бензола получено 840 кг циклогексана. Какое количество бензола прогидрировалось, если выход составляет 80% от теоретического?
265.Сколько килограммов бензола получится при пропускании 210 кг цик-
логексана над платиновым катализатором при 350-450°С, если выход составляет 85% от теоретического? Что может быть использовано в качестве источника бензола?
266.В 1936 г. Н.Д.Зелинский, Б.А.Казанский и А.Ф.Платэ открыли новый способ получения бензола при пропускании н-алканов над катализатором при 500°С. Сколько килограммов бензола может быть получено этим способом при ароматизации (дегидроциклизации) 129 кг н-гексана, если выход составляет 80% от теоретического?
267.Один из важнейших инсектицидов — 4,4'-дихлордифенил-трихлорметил-
метан (ДДТ) образуется при конденсации хлорбензола с трихлоруксусным альдегидом (хлоралем). Сколько граммов исходных реагентов требуется для получения 18,5 г ДДТ? С чем связано ограничение использования ДДТ в сельском хозяйстве?

vk.com/club152685050 | vk.com/id446425943
73
268. Сколько кг бензола может быть получено при ароматизации (дегидро-
циклизации) 129 кг н-гексана, если выход составляет 80%?
269. Какие углеводороды получатся, если подвергнуть каталитической ароматизации изогексан, н-гептан, н-октан?
2.4. Кислородсодержащие органические соединения
К кислородсодержащим соединениям относят большую группу органических соединений, в молекулах которых содержатся углеродные атомы,
непосредственно связанные с кислородом. К этим соединениям относятся:
Класс соединений
Спирты
Альдегиды
Кетоны
Карбоновые кислоты
Простые эфиры
Сложные эфиры
Общая формула
R-OH
|
|
O |
R |
C |
|
|
|
H |
R |
C |
R' |
|
O |
|
|
|
O |
R |
C |
|
|
|
OH |
R |
O |
R' |
O
R C
OR'
Каждый из этих классов имеет группу определенного состава и строения,
содержащую кислород - функциональную группу. Наличием этой группы в молекулах кислородсодержащих соединений определяются во многом особенности химических свойств каждого класса соединений.
2.4.1. Спирты
Спирты - это класс соединений, в состав которых входит функциональная группа -ОН. Например:

vk.com/club152685050 | vk.com/id446425943
CH -CH |
CH -CH-СН |
CH -CH -СН |
||||
2 |
2 |
2 |
3 |
2 |
2 |
2 |
OH OH |
OH OH |
|
OH |
|
ОН |
|
этиленгликоль |
1,2-пропиленгликоль |
1,3-пропиленгликоль |
||||
этандиол-1,2 |
пропандиол-1,2 |
пропандиол-1,3 |
||||
Соединения с тремя гидроксильными группами в молекуле – это трехатомные
спирты. Например: СН2(ОН) –СН(ОН)-СН2(ОН) – глицерин.
Методы получения спиртов.
1.Спирты можно получить действием воды на алкены. Реакцию проводят
вприсутствии серной кислоты, при этом сначала образуется эфир серной
кислоты, а затем под действием воды - соответствующий спирт.

vk.com/club152685050 | vk.com/id446425943
75
CH |
CH |
+ H |
OSO H |
CH |
CH |
OSO H |
+ HOH |
|
|
|
CH CH |
+ H SO |
|
||||||||
2 |
2 |
|
3 |
3 |
2 |
3 |
4 |
|||
|
|
|
|
|
|
|
3 |
2 |
2 |
|
этилен |
|
|
этилсульфат |
|
OH |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
этанол |
|
|
|
СH |
CH CH |
+ H |
OSO H |
СH |
CH CH |
+ HOH |
CH |
CH CH |
+ H SO |
|
|
4 |
|||||||||
3 |
2 |
|
3 |
3 |
3 |
|
3 |
3 |
2 |
|
пропилен |
|
|
|
OSO H |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
3 |
|
изопропиловый |
|
|
|
|
|
|
|
изопропилсульфат |
|
|
||||
|
|
|
|
спирт, пропанол-2 |
|
|||||
|
|
|
|
|
|
|
|
|||
Этот метод используют в промышленности для получения этилового и изопропилового спирта. Он называется методом сернокислотной гидратации.
2. Кроме того, спирты можно получать действием водного раствора щелочи на галогенпроизводные (гидролиз галогенпроизводных):
CH -CH -Br |
NaOH |
CH -CH -OH + NaBr |
||
|
||||
3 |
2 |
водный |
3 |
2 |
|
|
|
|
|
3. Этиловый спирт получают брожением глюкозы: С6Н12О6 2 С2Н5-ОН + 2СО2
Основные реакции спиртов - это реакции по гидроксильной группе.
1. Спирты реагируют с металлическим натрием. При этом водород в
гидроксильной группе замещается на металл - образуется алкоголят и выделяется водород
2CH3-CH2-OH + 2Na 2 CH3-CH2-ONa + Н2
этилат натрия
2. Спирты взаимодействуют с минеральными и органическими кислотами,
при этом происходит образование сложных эфиров:
СH |
CH O |
H + HO SO H |
СH |
CH |
+ |
H O |
|||||||||||||||||||||||||
3 |
2 |
|
|
3 |
3 |
2 |
|
|
2 |
||||||||||||||||||||||
этанол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OSO H |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
этилсульфат |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
СH3 |
|
CH2 |
|
O |
|
|
|
H + HO |
|
|
|
С |
CH3 |
|
CH2 |
|
O |
|
C |
|
CH3 + H2O |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
этанол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
O |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
уксусная кислота |
этилацетат, этиловый |
|
|
|
эфир уксусной кислоты |
3. При нагревании спиртов с водоотнимающими средствами происходит отщепление молекулы воды от молекулы спирта, и образуется алкен:

vk.com/club152685050 | vk.com/id446425943
76
|
|
o |
|
|
|
СH |
CH |
t |
CH |
CH |
+ H O |
|
|||||
2 |
2 |
H SO |
2 |
2 |
2 |
|
|
4 |
|
|
|
H |
OH |
2 |
|
|
|
|
этилен |
|
|||
этанол |
|
|
|
|
|
4. Если эту реакцию проводить в избытке спирта и при температуре, не превышающей 160°С, происходит отщепление молекулы воды от двух молекул спирта, и образуется простой эфир:
|
|
|
to |
|
|
CH3-CH2-OH + H-O-CH2-CH3 |
CH3-CH2-O-CH2-CH3 + H2O |
||||
H2SO4 |
|||||
|
|
|
диэтиловый эфир |
||
|
|
|
|
||
5. При действии галогенводородов (НС1, HBr, H ) гидроксильная группа замещается на галоген (Cl. Br, )
СH |
CH OH + H |
Br |
CH |
CH |
Br + H O |
3 |
2 |
|
3 |
2 |
2 |
этанол |
|
бромэтан |
|||
6. Спирты окисляются сильными окислителями или кислородом воздуха при температуре 300-500°С на катализаторах. При этом первичные спирты образуют альдегиды, вторичные - кетоны.
|
|
[O] |
|
O |
|
CH |
CH OH |
CH |
C |
||
|
|||||
3 |
2 |
кат. |
3 |
H |
|
|
|
|
|||
|
|
|
ацетальдегид |
||
|
|
|
этаналь |
||
CH |
CH СH |
[O] |
CH |
C |
CH |
|
|||||
3 |
3 |
кат. |
3 |
|
3 |
|
|
|
|
|
|
|
OH |
|
|
O |
|
|
|
|
ацетон |
||
|
|
|
пропанон-2 |
||
Для получения двухатомных спиртов (гликолей) применимы те же
способы, что и для одноатомных спиртов. Этиленгликоль обычно получают из
этилена следующими методами:
|
|
|
O |
2 |
|
|
|
H O |
|
|
|
CH CH |
|
CH |
|
CH |
2 |
CH |
CH |
||||
|
|
2 |
2 |
|
|||||||
2 |
2 |
Ag |
|
|
|
+ |
2 |
2 |
|||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
O |
|
|
H |
OH |
OH |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
этиленгликоль |
|||
|
|
|
|
|
окись этилена |
|
|||||
|
|
|
|
|
эпоксиэтан |
|
этандиол-1,2 |
||||
|
|
|
|
Cl2 |
|
|
|
H O |
|
|
|
CH |
|
CH |
|
CH2 |
|
CH2 |
2 |
CH2 |
|
CH2 |
|
|
|
|
|
|
|||||||
|
|
|
|||||||||
2 |
|
|
2 |
|
|
|
|
|
- |
|
|
|
|
|
|
|
Cl |
|
Cl |
OH |
|
OH |
|
|
|
|
|
|
|
|
OH |
|
|||
1,2-дихлорэтан

vk.com/club152685050 | vk.com/id446425943
77
|
|
HOCl |
|
|
H O |
|
|
CH |
CH |
|
CH |
CH |
2 |
CH |
CH |
|
2 |
2 |
|
2 |
2 |
||
2 |
2 |
|
|
|
|
- |
|
|
|
|
|
|
OH |
|
|
|
|
|
Cl |
OH |
OH |
OH |
|
|
|
|
|
||||
|
|
|
2-хлорэтанол |
|
|
|
|
|
|
этиленхлоргидрин |
|
|
|||
Гликоли дают все реакции одноатомных спиртов с тем лишь различием,
что в реакции могут участвовать как одна, так и две гидроксильные группы.
При действии на гликоли гидрата окиси меди образуется голубой раствор комплексного соединения. Эта реакция используется как качественная реакция на гликоли.
|
|
|
|
H |
|
CH |
OH |
CH |
O |
O |
CH |
2 |
|
|
2 |
||
2 |
|
|
|
|
|
2 |
|
+ Cu(OH) |
|
Cu |
+ 2H O |
|
2 |
|
|
2 |
|
CH |
OH |
CH |
O |
O |
CH |
2 |
|
|
2 |
||
2 |
|
|
|
|
|
|
|
|
|
H |
|
Этиленгликоль применяется как антифриз для автомобильных двигателей, т.к. понижает температуру застывания воды. Полиэфиры этиленгликоля находят применение в различных отраслях промышленности.
Первым представителем трехатомных спиртов является глицерин. Его получают гидролизом жиров, которые представляют собой сложные эфиры глицерина и высших жирных кислот. Гидролиз жиров обычно называют омылением, поскольку образующиеся при этом натриевые соли высших жирных кислот являются мылами. Глицерин также получают из пропилена,
который выделяют из газов процессов крекинга.
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
CH |
O |
C |
C |
15 |
H |
|
CH |
OH |
|
|
|
|||
2 |
|
|
O |
|
|
31 |
|
2 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
O |
C |
C |
15 |
H |
|
+ 3 NaOH |
CH |
OH |
+ 3 C |
15 |
H COONa |
||
|
|
|
|
|
31 |
|
|
|
|
31 |
||||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
CH |
O |
C |
C |
15 |
H |
|
|
CH |
OH |
|
|
|
||
2 |
|
|
|
|
31 |
|
2 |
|
|
|
|
|||
|
жир |
|
|
|
|
|
|
|
глицерин |
|
|
мыла |
||
Химические свойства глицерина обусловлены наличием трех гидроксильных групп, при этом глицерин может давать три ряда производных:
моно-, ди- и трипроизводные. Глицерин применяется в парфюмерии,
кондитерском производстве, для получения нитроглицерина.

vk.com/club152685050 | vk.com/id446425943
78
Ароматические соединения, у которых гидроксильная группа находится при углеродном атоме в боковой цепи, называют ароматическими спиртами. Их простейшими представителями являются:
Для этих спиртов присущи способы получения и химические свойства,
которые характерны для алифатических спиртов. Эти спирты представляют практический интерес, поскольку в свободном виде и в виде эфиров широко распространены в растительном мире и часто в виде сложных эфиров применяются в парфюмерии из-за приятного запаха. Например, бензиловый спирт в свободном виде или в виде эфиров встречается в масле жасмина. -Фе-
нилэтиловый спирт является основной составляющей в розовом масле.
2.4.2. Фенолы - органические соединения, в которых гидроксильная группа связана непосредственно с углеродным атомом ароматического кольца.
Простейшие представители:
Фенол получают сплавлением солей сульфокислот со щелочами:
Этот метод применяется в промышленности.

vk.com/club152685050 | vk.com/id446425943
79
Фенол можно получить окислением изопропилбензола (кумола)
кислородом воздуха в присутствии катализатора с последующим разложением образующейся гидроперекиси кумола. В результате получается два продукта -
фенол и ацетон:
Этот метод, применяемый в промышленности для получения фенола и ацетона, называется - кумольный метод.
С хорошим выходом можно получить фенол пиролизом хлорбензола.
Химические свойства
1.Фенолы проявляют большую кислотность, чем спирты, однако они слабее,
чем карбоновые кислоты. Фенолы реагируют со щелочами, с образованием фенолятов.
2. Феноляты реагируют с галогенпроизводными с получением эфиров фенолов:
