
- •Геология месторождений горючих полезных ископаемых
- •17 Час. – лекции; 17 час. – лаб. Занятия; 2 – тек. Конс., 4 час.–проверка к/р, 4 час. – зачет (всего 44)
- •Тема 1. Введение. Общие сведения о горючих полезных ископаемых
- •Перечень продуктов глубокой переработки углей подтверждает слова д.И. Менделеева: «Сжигать нефть и уголь – то же, что топить печь ассигнациями».
- •Тема 2. Горючие ископаемые сапропелевого ряда
- •Тема 4. Горючие ископаемые угольного ряда. Торф
- •Тема 5. Ископаемый уголь
- •Тема 6. Горючие ископаемые нефтяного ряда.
- •Тема 7. Химический состав, физические свойства и технологическая характеристика нефтей
- •Классификация нефтей по содержанию серы*
- •Классификация нефтей по содержанию парафинов*
- •Классификация нефтей по плотности*
- •Тема 8. Нефтегазоматеринский потенциал осадочных толщ. Залежи и ловушки нефти и газа
Геология месторождений горючих полезных ископаемых
РМ-07 (2011)
17 Час. – лекции; 17 час. – лаб. Занятия; 2 – тек. Конс., 4 час.–проверка к/р, 4 час. – зачет (всего 44)
№ п/п |
Дата занятий |
Кол-во часов |
ТЕМЫ ЗАНЯТИЙ |
ЛЕКЦИИ |
|||
1 |
22.02 |
2 |
Введение. Общие сведения о горючих полезных ископаемых. Углерод |
2 |
09.03 |
2 |
Горючие ископаемые сапропелевого ряда |
3 |
22.03 |
2 |
Прибалтийский и Волжский бассейны горючих сланцев. Шунгит |
4 |
05.04 |
2 |
Горючие ископаемые угольного ряда. Торф |
5 |
19.04 |
2 |
Ископаемый уголь |
6 |
03.05 |
2 |
Горючие ископаемые нефтяного ряда. Происхождение нефти и природного газа |
7 |
17.05 |
2 |
Химический состав, физические свойства и технологическая характеристика нефтей |
8 |
31.05 |
3 |
Нефтегазоматеринский потенциал осадочных толщ. Залежи и ловушки нефти и газа |
|
|
|
ЛАБОРАТОРНЫЕ |
1 |
09.02; 16.02 |
2 |
Построение гипсометрического плана выхода пластов угля под наносы по данным бурения. Задача №78 |
2 |
24.02; 02.03 |
2 |
Макродиагностика твердых горючих полезных ископаемых |
3 |
09.03; |
2 |
Размещение бассейнов угля и горючих сланцев. |
4 |
16.03; 23.03 |
2 |
|
5 |
30.03; 06.04 |
2 |
Размещение нефтегазовых бассейнов. |
6 |
13.04; 20.04 |
2 |
Свойства флюидов в пласте |
7 |
27.04; 04.05 |
2 |
Залежи, ловушки и месторождения нефти и газа |
8 |
11.05; 18.05 |
3 |
Подсчет запасов нефти в антиклинальной ловушке |
9 |
25.05 |
|
|
ВОПРОСЫ
1. Что понимается под горной породой?
2. Что собой представляет ископаемый уголь?
3. В чем состоит коренное отличие ископаемого угля от горючего сланца?
4. По каким макроскопическим признакам различают бурые и каменные угли?
5. Что такое мацерал?
6. В чем состоит отличие коксовых и коксующихся углей?
7. Какие марки углей не могут быть изучены в проходящем свете?
8. Что собой представляет подошва угольного пласта?
9. Что понимается под ложной кровлей угольного пласта?
10. Какова максимальная мощность известных угольных пластов?
11. Откуда в угленосной толще берется метан?
12. Каков геологический возраст наиболее древних ископаемых углей?
Тема 1. Введение. Общие сведения о горючих полезных ископаемых
Ключевые слова: Твердые горючие полезные ископаемые. Уголь. Горючий сланец. Кероген. Мацерал (микрокомпонент). Высшие и низшие растения. Простейшие животные организмы. Белки. Липиды. Углеводы. Лигнин. Гумолиты. Гумиты. Липтобиолиты. Стадии углефикации. Неорганические компоненты углей. Влага угля.
Все виды минерального сырья могут быть разделены на две крупные группы: обеспечивающие развитие человечества и обеспечивающие существование человечества. Несомненно, человечество получило бы иной вектор развития, если бы на смену орудиям труда из дерева и кости не пришли бы каменные орудия, а затем изделия из бронзы и железа. Десятки тысяч лет люди обходились без вольфрама и германия. Но уже для неандертальцев был необходим огонь, а значит природные энергоносители. Физическое существование цивилизации не возможно без потребления энергии. Свыше 2/3 территории России находится в области развития многолетнемерзлых пород. Поэтому объективно энергоемкость ВВП РФ в 2,5 раза выше чем в США, в 3,5 чем в Западной Европе и в 6 раз чем в Японии. «За право и честь жить в России мы должны потреблять больше ТЭР» (акад. Конторович А.Э.). По масштабу мирового торгового оборота горючие полезные ископаемые превосходят все другие виды минерального сырья вместе взятые.
Горючими полезными ископаемыми называются существенно углеводородные образования, извлекаемые из недр, которые могут быть эффективно использованы в сфере материального производства. Горючие полезные ископаемые способны к экзотермическим окислительным реакциям с интенсивным выделением тепла и ярким свечением (пламенем), т. е. горению и отвечают общей химической формуле CnHm, при незначительном (как правило, до нескольких процентов) содержании O, S, N, P и др.
Горючие ископаемые отличаются разнообразием строения и изобилием соединений, встречаются в различных агрегатных состояниях: твердом (угли, горючие сланцы, торф, твердые битумы, шунгит), жидком (нефти), газообразном (природные и попутные газы, угольный метан) и других особых состояниях (газогидраты, конденсаты). Фазовое состояние горючего ископаемого определяется соотношением водорода и углерода по массе. Алканы (формула CnH2n+2), преобладающие в составе органического вещества (ОВ) горючих ископаемых при n<5 - газы, при 5<n<16 – жидкие, а при n>16 твердые вещества.
По составу органического вещества горючие полезные ископаемые разделяются на три ряда: сапропелитовый - сапропели, горючий сланец и шунгиты; гумолитовый (угольный) - торф, бурый уголь, каменный уголь и антрацит; битумный (нефтяной) - горючий газ, нефть, асфальт и асфальтит.
В природе горючие полезные ископаемые, как и основная часть других углеродсодержащих горных пород, сосредоточены в особой области недр Земли сопряженной с биосферой - карбосфере, где особая роль принадлежит углероду и осуществляется его круговорот. Латинское название carboneum углерод получил от carbo — уголь.
Основным химическим элементом, определяющим полезные свойства горючих ископаемых, является углерод.
Углерод, C – химический элемент IV группы периодической системы Менделеева, атомный номер 6, атомная масса 12,01. Стабильные изотопы: 12С (98,99%) и 13С (1,11%). Радиоактивный изотоп 14C имеет период полураспада 5,6103 лет и образуется в верхних слоях атмосферы из атома 14N под действием космического излучения. Электронное строение углерода 1s22s22p2, элементарная природа была установлена А. Лавуазье в 1789 г. Углерод обладает свойствами, как металла, так и неметалла. Степени окисления углерода ±4. Электронную оболочку атома углерода образуют 4 валентных электрона, за счет обобществления которых атомы углерода соединяются между собой ковалентными связями с образованием структурных решеток различной размерности, а также прочных и длинных полимерных цепей и циклов с общей формулой Cn (Д.И. Менделеев) (рис. 1).
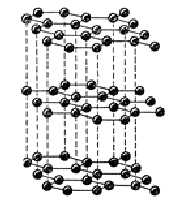


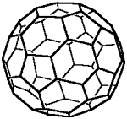
а) б) в) г)
Структуры аллотропных модификаций углерода
а) графит, б) алмаз, в) фуллерен, г) карбин
Аллотропные модификации углерода при обычных условиях химически инертны, при высоких температурах соединяются со многими элементами, проявляя сильные восстановительные свойства, нерастворимы в обычных растворителях, но растворяется в некоторых расплавленных металлах (например, Fe, Ni, Co, Ag).
Углерод - основной элемент, определяющий теплоту сгорания углеводородов. В металлургическом процессе углерод кокса (продукта переработки угля) является источником энергии и восстановителем металлов. Водород в составе органической части угля также является источником энергии и при сгорании выделяет в 4,2 раза больше тепла на единицу массы, чем углерод. Кроме химического состава на величину теплоты сгорания углей при прочих равных условиях влияет и структурная организация вещества.
Кларк углерода 2,3∙10–2% (по массе). По распространенности среди химических элементов углерод занимает в земной коре 16 место. Число собственных минералов углерода – 112, число изученных органических соединений углерода превышает 10 млн. Углерод встречается в свободном (графит, алмаз, карбин, фуллерен, лонсдейлит) и связанном состоянии, главным образом в составе карбонатных и органических горных пород, в биомассе, атмосфере и в водных растворах. Сорг в виде форменных остатков (окаменелостей бактерий) обнаружен в архейских метаморфических сланцах и метакварцитах Гренландии и Южной Африки. В парообразном состоянии и в виде соединений с N и H углерод присутствует в атмосфере Солнца, планет, в метеоритах, в спектрах холодных звезд. В составе вещества Солнца углерод занимает четвертое место после водорода, гелия и кислорода. Монокристаллы углерода могут рассматриваться как высокомолекулярные углеводороды с предельно низким содержанием водорода. В нефтях и воде океанов выявлены наночастицы алмазоидов (адамантана, диадамантана, триадамантана), веществ по составу, структуре и физическим параметрам, близким к алмазам.
Общие характеристики и практическая значимость таких аллотропных форм углерода как графит и алмаз широко известны. Поэтому приведем краткие сведения только о других формах свободного углерода.
Карбин - линейный полимер, состоит из параллельно ориентированных цепочек атомов углерода с sp-гибридизацией валентных электронов, образующих макромолекулы типа …=С=С=С=… и …– С ≡ С – С ≡ С – С ≡… Обнаружен в 60-х гг. ХХ в. в природном графите, в виде белых прожилков и вкраплений, а в 1970 г. в астроблеме Рис в ФРГ (минерал чаоит). Плотность карбина 1,9-2 г/см3. Благодаря сильным химическим связям углерода карбин имеет наибольшую теоретическую предельную прочность (до 23 т/мм2) из всех известных на Земле веществ.
В 1992 г. в шунгите (Карелия) был обнаружен фуллерен - шарообразные молекулы углерода с химической формулой C60. Молекулы С60 содержит фрагменты с пятикратной симметрией, запрещенной природой для неорганических соединений, и являются связующим звеном между органическим и минеральным веществом. Форма молекул фуллерена совпадает с формой скелетов радиолярий известных с докембрия в составе морских отложений. Все атомы углерода в молекуле С60 равнозначны, так как каждый атом принадлежит одновременно двум шестиугольникам и одному пятиугольнику. Молекулы высших фуллеренов (С70, С74, С76, С84, С164, С192, С216) также имеют замкнутую поверхность. Между молекулами фуллерена существует слабая связь Ван-дер-Ваальса. Фуллерен имеет плотность 1,7 г/см3, растворим в органических растворителях (бензоле, гексане, сероуглероде), электроотрицателен, является сильным окислителем. В настоящее время получение фуллеренов в лабораторных условиях дорого и малопроизводительно.
Лонсдейлит обнаружен в метеоритах, а также получен искусственно, его структура и физические свойства не ясны.
Углерод - важнейший биогенный элемент, составляющий основу жизни на Земле. Значительная часть энергии необходимой организмам образуется в живых клетках за счёт окисления углерода. Возникновение жизни на Земле обусловлено сложным процессом эволюции углеродистых соединений.
Соединения углерода - материальная основа теплоэнергетики. Углерод - сырье для разнообразных химических производств, производства конструкционных материалов; в составе карбонатов применяется в металлургии, строительстве; алмазы используются в ювелирном деле и технике; графит – в ядерной технике, для производства смазок, карандашей и др.; уголь применяется для производства адсорбентов, карбидов, электродов, как восстановитель руд и др. Из карбина получают углеродные волокна, обладающие полупроводниковыми свойствами, которые усиливаются под действием света, изготавливают пуленепробиваемые жилеты, конструкционные элементы самолетов, ракет, костюмы, обогреваемые электричеством, фотоэлементы, биологически совместимые материалы и др. Фуллерены могут быть использованы для создания фотоприемников и оптоэлектронных устройств, катализаторов роста, алмазных и алмазоподобных пленок, сверхпроводящих материалов, а также в качестве красителей для копировальных машин, получения новых сплавов, аккумуляторных батарей, накопителей свободного водорода, запоминающей среды со сверхвысокой плотностью информации, присадок ракетных топлив, смазочного материала. Изотоп 14С используется для целей радиоуглеродной датировки.
Углерод важнейший элемент органического вещества и до конца еще неизведанный.
В 2004 г. был получен графе́н — слой атомов углерода толщиной в один атом, соединённых посредством sp2 связей в гексагональную двумерную кристаллическую решетку. Идеальный графен состоит из шестиугольных ячеек. Присутствие пяти- и семиугольных ячеек приводит к различным дефектам. Наличие пятиугольных ячеек обуславливает сворачивание атомной плоскости графена в конус. Структура с 12 такими дефектами одновременно известна как фуллерен. Присутствие семиугольных ячеек вызывает седловидные искривления атомной плоскости. Комбинация дефектов и нормальных ячеек приводит к образованию сложных поверхностей.
Графен обладает большой механической прочностью и теплопроводностью. Высокая подвижность электронов при комнатной температуре делает его перспективным материалом для использования в наноэлектронике с базовой толщиной транзисторов до 10 нм и заменителем кремния в интегральных микросхемах, обеспечивая при этом большее быстродействие.
Перспективно использование графена для изготовления электродов и в ионисторах (суперконденсаторах). Ионисторы на графене имеют удельную энергоёмкость 32 Вт·ч/кг, как и у свинцово-кислотных аккумуляторов (30−40 Вт·ч/кг).
В отличие от графита, графен вступает в химические реакции с некоторыми веществами. При этом его проводимость уменьшается. Это позволяет применять графен в качестве очень чувствительного сенсора для обнаружения отдельных молекул веществ.
При взаимодействии графена с водородом, к двумерной кристаллической сетки атомов углерода поочередно сверху и снизу присоединяются атомы водорода, немного деформируя плоскую структуру графена. Этот материал получил название графан. В отличие от графена, графан является диэлектриком.
Полосами графана можно разделить пленку исходного графена на множество проводящих полос и получить сверхминиатюрные транзисторы с различными параметрами. Современная полупроводниковая индустрия для получения изоляторов, полупроводников и проводников с различными свойствами использует множество химических элементов. В будущем любые электронные компоненты можно будет получать, модифицируя один единственный исходный материал – графен.
Реакция взаимодействия графена с водородом является обратимой. Нагрев графана приводит к высвобождению атомарного водорода. Поэтому графан может найти применение при производстве водородных топливных элементов с чрезвычайно высоким КПД.
Различают взаимосвязанные малый и большой циклы обращения органического углерода. Малый цикл имеет продолжительность от нескольких дней до тысячелетий. В ходе малого цикла обращения углекислота при фотосинтезе связывается в живое органическое вещество, которое при отмирании частично разлагается на углекислый газ и воду и в незначительном количестве захоранивается в виде ОВ осадков и таким образом поступает в большой цикл обращения органического углерода длительностью в млн. лет. В результате выветривания преобразованное в недрах ОВ может генерировать углекислоту, поступающую в малый цикл обращения органического углерода
Изотопный состав углерода индивидуальных природных соединений зависит от их генезиса (фракционирования). В процессе фотосинтеза в биомассу переходит лишь незначительная часть изотопа 13С. Дефицит 13С служит показателем биогенного генезиса вещества.
По оценке В.А. Успенского, общее количество углерода в атмосфере достигает 610 млрд. т, а в земной коре имеется около 6×1018 т углерода. Процесс захоронения органического вещества идет не менее 3 млрд. лет. В течение года более 1 млрд. т углерода из атмосферы, гидросферы и биосферы уходит в литосферу. Примерно за 1000 лет весь углерод атмосферы мог бы быть связан в органических отложениях, если бы атмосфера систематически не пополнялась углекислым газом за счет деятельности вулканов и других газовыделений земной коры и мантии. Полный круговорот углерода в атмо- и гидросфере осуществляется за 300-400 лет, что создает условия для развития биосферы и находит отражение в периодичности фаз и неравномерности размещения поясов палео- и современного торфонакопления.
В мировом океане в результате фотосинтеза ежегодно фиксируется порядка 1011 т углерода, из них до 1% захоранивается в осадках. Значительно большее количество СО2 связывается в карбонатных породах
По степени концентрации Сорг выделяют три основные градации породных комплексов:
Концентрированное ОВ (Сорг>50%). Сюда относят ископаемые угли и битумолиты, на долю которых приходятся десятые доли процента от общей массы ОВ заключенного в земной коре.
Умеренно концентрированное ОВ (50>Сорг>5%) входит в состав горючих сланцев, углистых и битуминозных пород, черных сланцев. На их долю приходится порядка 5% от общей массы ОВ заключенного в земной коре.
Рассеянное ОВ (РОВ) (Сорг<5%). На долю РОВ приходится >90% от общей массы ОВ заключенного в земной коре.
Геологическую историю горючих полезных ископаемых обычно разбивают на 2 этапа докембрийский и фанерозойский. Наиболее древние породы, содержащие преобразованные органические вещества и некарбонатный углерод (графит) имеют возраст 3,5 млрд. лет (AR1) и выявлены на всех древних платформах. Углеродистые глинистые сланцы, гнейсы, доломиты, кварциты могут слагать толщи мощностью в сотни метров. Преобладает дисперсная форма ОВ при среднем содержании 0,5-0,8%. Слоистость и ритмичность этих толщ свидетельствует о седиментогенной и сингенетической природе основных количеств ОВ. Возраст углеродистого вещества указывает на время появления хемосинтезирующих бактерий и возникновения биосферы. Прямые признаки биогенной природы ОВ (остатки простейших водорослей) устанавливаются для пород не прошедших стадию амфиболитового метаморфизма.
С толщами архея и протерозоя связаны многочисленные промышленные месторождения графита, большая часть которых считается осадочно-метаморфогенными. Связь графита этих месторождений с ОВ обосновывается их приуроченностью к стратифицированным горизонтам. Графит, залегающий в виде жил и гнезд интерпретируется как результат флюидизации ОВ. Многие высокоуглеродистые углистые или графитовые сланцы и гнейсы могут представлять собой остатки месторождений (бассейнов) метаморфизованных горючих сланцев.
Кроме графита концентрированное ОВ в отложениях криптозоя встречается в виде метаморфизованных горючих сланцев – шунгитов, а также углеводородов нефтяного ряда. Гумолиты встречаются исключительно в отложениях фанерозоя. Органическое вещество распространено по стратиграфическому разрезу крайне неравномерно. Если средние значения Сорг максимальны для кайнозоя, то общая масса максимальна для юры, затем для мела, карбона и девона. Отложения, обогащенные РОВ, прослеживаются на одних и тех же стратиграфических уровнях на разных континентах и не совпадают с эпохами палеоторфонакопления. При среднем содержании Сорг в глинистых породах 0,9% на них приходится 75% массы Сорг в недрах. В ископаемых углях среднее содержание Сорг 67%, но на них приходится лишь 0,28% массы Сорг в недрах.
В отличие от минеральных составляющих горных пород ОВ является весьма «агрессивным». При содержании Сорг>0,1 мас.% ОВ оказывает влияние на свойства пород, в т. ч. на визуально наиболее значимое свойство – цвет гуминосапропелей1, а также на «геохимические» особенности пород. Сероцветные породы (например, субдоманикоиды) содержат 0,1-0,5% Сорг; коричневые 0,5-5% (доманикоиды); черные 5-25% (доманикиты).
В структуре мировой ресурсной базы абсолютное первенство (на порядок) среди первичных традиционных источников энергии в пересчете на УТ имеют твердые горючие полезные ископаемые. Ограниченность ресурсов нефти и газа и интенсивное их использование позволяют считать нефть и газ главенствующими видами энерготехнологического сырья лишь на период 1950-2050 гг. Уголь и горючий сланец является распространенным и стабильным энерготехнологическим минеральным сырьем на многие сотни лет.
Ископаемый уголь и горючий сланец – это горные породы осадочного происхождения, полезные свойства которых определяются, прежде всего, наличием в их составе преобразованного органического вещества высших растений и простейших организмов.
Кроме остатков различных органов и тканей главным образом высших растений в состав угля входят минеральные компоненты (менее 50% от сухой массы), влага (от 58% у 1Б до 2% у А) и газовые компоненты.
В отличие от угля горючий сланец содержит равномерно распределенные органические остатки в основном простейших организмов (20÷70%) - кероген. Горючие сланцы обычно коричневато-бурые, реже черные, текстура массивная их или тонкослоистая (при выветривании листоватая). Плотность (при содержании керогена 30÷50 %) 1,5÷1,8.
Основные компоненты твердых горючих полезных ископаемых: органическое вещество, минеральное вещество и влага. Органическое вещество – носитель горючих и химико-технологических свойств горючих полезных ископаемых. Минеральное вещество и влага являются балластом, их наличие снижает потребительские свойства и затрудняет использование природных твердых энергоносителей.
Органическое вещество твердых горючих полезных ископаемых сложено различными компонентами преобразованных остатков растений и простейших (одноклеточных) животных организмов.
Клетки растений и простейших животных организмов содержат протеины (белки), жиры, углеводы, смолы, хлорофилл и др. Различают низшие и высшие растения. Низшие растения лишены дифференцированных органов, их тело представляет собой слоевище, не расчлененное на стебель и листья. Низшие растения и простейшие (фито и зооплантон) развиваются в водной среде, обмен веществ осуществляют всей поверхностью, ориентация низшего растения и простейших организмов в пространстве может быть любая, переносятся током воды. Высшие растения – обладают специализированной корневой системой расположенной в минеральном субстрате, стеблем, вегетативными органами. Для сохранения преимущественной вертикальной ориентировки – стенки клеток (целлюлоза) пропитываются (скрепляются) лигнином, иногда пробковой тканью (кутином). В высших растениях преобладают оболочки, в низших растениях и простейших организмах клеточное содержимое (в основном липиды и белки).
Белки (протеины) - высокомолекулярные природные органические вещества, построенные из аминокислот и играющие фундаментальную роль в структуре и жизнедеятельности организмов. Белки (ферменты и др.) обеспечивают активные биологические функции: обмен веществ и энергетические превращения. После отмирания клеток белки быстро гидролизируются до аминокислот. Белки – источник N и S в твердых горючих полезных ископаемых.
Липиды (от греч. lípos — жир) - жироподобные вещества, входящие в состав живых клеток и играющие важную роль в жизненных процессах. Будучи одним из основных компонентов биологических мембран, липиды влияют на проницаемость клеток и активность многих ферментов, участвуют в передаче нервного импульса, в мышечном сокращении, создании межклеточных контактов, в иммунохимических процессах. Другие функции липидов — образование энергетического резерва и создание защитных водоотталкивающих и термоизоляционных покровов у животных и растений, а также защита различных органов от механических воздействий. В биогенной концепции образования нефтей именно липидам придается особое значение. При отмирания клеток переходят в сложные эфиры и высшие жирные кислоты.
Углеводы - обширная группа органических соединений, входящих в состав клеток живых организмов. Основные углеводы имеют общую формулу Cm(H2O)n, то есть углерод + вода (отсюда название). Наиболее распространенные в природе углеводы полисахариды целлюлоза и хитин, широко известны глюкоза (C6(H2O)6) и фруктоза(C5(H2O)5). Целлюлоза (от лат. cellula, буквально — комнатка, клетушка) (клетчатка) - главная составная часть клеточных стенок растений, обусловливающая механическую прочность и эластичность растительных тканей. Содержание целлюлозы в волосках семян хлопчатника 97—98%; в стеблях лубяных растений (лён, рами, джут) 75—90%; в древесине 40—50%, камыше, злаках, подсолнечнике 30—40%. Хитин (от греч. chiton — одежда, кожа, оболочка) - основной компонент наружного скелета (кутикулы) членистоногих и ряда др. беспозвоночных, входит также в состав клеточной стенки грибов и бактерий. Выполняет защитную и опорную функции, обеспечивая жёсткость клеток. При отмирании целлюлоза растений бактериями и грибками преобразуется в жиры и далее в более устойчивые жирные кислоты.
Лигнин (от лат. lignum — дерево, древесина) - наиболее углеродистое из полимерных соединений в составе ОВ растений. Инкрустирует оболочки растительных клеток. Отложение лигнина в оболочках клеток вызывает одревеснение клеток и увеличивает их прочность. Древесина лиственных пород содержит 20—30% лигнина, хвойных — до 50%; у низших организмов лигнин не обнаружен. Лигнин преобразуется в гуминовые кислоты - главные составные компоненты торфа. В живых растениях гуминовых кислот нет.
Таблица 1
Групповой состав биопродуцентов, %
Биопродуценты |
Липиды |
Белки |
Углеводы |
Лигнин |
Высшие растения |
<5 |
5-10 |
>50 |
>25 |
Лиственные мхи |
8-10 |
15-30 |
30-40 |
10 |
Фитопланктон |
5-20 |
24-48 |
30-65 |
- |
Зоопланктон |
10-22 |
65 |
20 |
- |
Бактерии |
20 |
<60 |
20 |
- |
Высшие растения – многоклеточные наземные растения. Обладают дифференцированными органами; закреплены на минеральном субстрате. В химическом составе высших растений главенствующее значение имеет углевод - целлюлоза (клетчатка).
Низшие растения и простейших животные, существующие в водной среде, в совокупности составляют планктон. По химическому составу в планктоне преобладают белки и жиры.
Основное значение в образовании органического вещества растений имеет фотосинтез, при котором световая энергия Солнца, воздействуя на хлорофилл, запускает механизм трансформации углекислого газа и воды в сложные органические соединения и преобразуется во внутримолекулярную энергию углеводов. Реакция фотосинтеза выражается схемой:
6СО2 + 12Н2О+ солнечная энергия/2,7 МДж/ + хлорофилл = С6Н12О6 + 6О2
Ежегодно растения связывают и превращают в химическую энергию 2000 трлн. квт/час солнечной энергии. При этом в процессе фотосинтеза из воздуха изымается 175 млрд. т углерода. Большая часть углерода возвращается в атмосферу в результате разложения (окисления, горения) органики одновременно высвобождая солнечную (тепловую) энергию. Поедая пищу и обогревая жилье, люди используют законсервированную энергию Солнца.
В соответствии с характером исходного материала выделяют группы твердых ископаемых энергоносителей: гумолиты, образовавшиеся преимущественно из продуктов преобразования отмерших высших растений; сапропелиты, сложенные продуктами преобразования отмершего фито и зоопланктона и сапрогумолиты – переходная группа с органическим веществом смешанного состава. В группе гумолитов выделяют подгруппы: гумитов, исходным материалом которых явились преимущественно лигнино-целлюлозные ткани высших растений, и липтобиолиты – сложенные в основном устойчивыми к биохимическому разложению компонентами этих растений: кутикулами, спорами, восковыми, смолистыми и пробковыми веществами. Преобладающая масса углей относится к гумолитам, все без исключения горючие сланцы к сапропелитам.
В химическом отношении органическое вещество твердых горючих полезных ископаемых представлено комплексом сложных высокомолекулярных соединений. В элементном составе этих высокомолекулярных соединений преобладает С, подчиненное значение имеют O, H, N и органическая S. Менее 1% приходится на фосфор, металлы и др. элементы. В отмершем органическом веществе при благоприятных условиях под воздействием постепенно сменяющихся процессов биохимического, химического и физического преобразования необратимо увеличивается содержание С и уменьшается содержание О и Н. Этот процесс называют углефикацией (метаморфизмом, карбонизацией). Изменение химического состава при углефикации приводит к изменению физических и технологических свойств твердых горючих полезных ископаемых. По характеру и степени преобразований органического вещества высших растений различают четыре стадии углефикации: торфяную, буроугольную, каменноугольную и высшую (антрацитовую) (табл. 2).
Таблица 2
Состав органического вещества (%) и свойства твердых видов топлива
Элементы и показатели |
Древесина |
Торф |
Бурый уголь |
Каменный уголь |
Антрацит |
Углерод Кислород Водород Азот |
50 43 6 1 |
56 36 6 2 |
72 22 5 1 |
84 9 5 2 |
96 <1 2 <1 |
Влажность, % Низш. теплота сгорания (МДж/кг) Выход летучих, % |
>20 <25 30÷40 |
До 97 <17 |
16÷58 <19 30÷60 |
5÷16 <28 8÷50 |
<2 <31 2÷9 |
Глубина погружения, км tоС |
0 0÷30 |
0 0÷30 |
<1,5 <50 |
<6,5 <220 |
>6,5 >220 |
Химический состав органической части горючих сланцев: углерод 56÷82, водород 5÷10, кислород 10÷40, азот 0,2÷2,8, сера 0,2÷11 %.
Размер элементарных составляющих твердых горючих полезных ископаемых, как правило, не превышает 50 мкм. Поэтому главное значение при изучении состава и строения ископаемых углей и горючих сланцев имеют углепетрографические исследования с помощью микроскопа.
Элементарные органические составляющие твердых горючих полезных ископаемых различимые под микроскопом по форме, цвету, рельефу, отражательной способности, показателю преломления и др. оптическим признакам носят название мацералов или микрокомпонентов. Различными исследователями выделяется от 14 до 40 петрографических компонентов углей, объединяемых по исходному материалу и условиям его превращения в торфяной стадии углеобразования в три основные (витринитовые или гелинитовые, фюзинитовые и лейптинитовые) и две промежуточные (слабо гелифицированные и слабо фюзенизированные) группы микрокомпонентов.
Количественное соотношение микрокомпонентов и состав исходных растений определяют генетические типы углей, характеризующиеся определёнными химическими и технологическими свойствами в пределах каждой данной стадии углефикации.
В зависимости от исходного органического вещества, характера и степени его преобразования, содержания и состава минеральных веществ ископаемые угли представлены разновидностями, существенно различающимися по химическому составу, физическим и технологическим свойствам. С повышением степени зрелости в химическом составе органического вещества углей увеличивается содержание углерода (от 63 до 95 %) и снижается содержание кислорода, водорода и азота. Цвет малозольных углей изменяется, от бурого до интенсивно черного, блеск – от матового до стеклянного, твердость по шкале Мооса от 1 до 5, плотность от 0,92 до 1,7, значительно изменяются твердость, хрупкость, электропроводимость, термическая стойкость, другие механические и физические свойства. На средних стадиях углефикации угли приобретают свойство спекаться – переходить при нагревании без доступа кислорода в пластическое состояние и образовывать полукокс или кокс. Высшая теплота сгорания углей 25÷37 МДж/кг.
Неорганические компоненты в углях представлены минеральным веществом в виде рассеянных микроскопических зерен, конкреций (макроскопических минеральных стяжений), породных линз и прослоев пустых пород. Минеральное вещество состоит в основном из алюмосиликатов (минералов глин) и кремнезема (кварца), подчиненное значение имеют сульфиды (главным образом Fe), карбонаты Ca, Mg, Fe, сульфаты (гипс), оксиды и гидрокиды Fe и Al, хлориды K и Na, фосфаты, соединения цветных и редких металлов, рассеянных элементов.
При сжигании углей большая часть минеральных веществ переходит в золу и шлак, частично разлагается. Состав минеральных компонентов углей определяет химический состав и технологические свойства золы и шлаков, состав дыма, играет существенную роль в процессах энергетического и технологического использования углей, а также определяет возможность и целесообразность использования зол, шлаков и отходов обогащения углей для производства строительных материалов и глинозема. Минеральное вещество твердых горючих полезных ископаемых в совокупности с параметрами топочных агрегатов, техническими и термодинамическими условиями сжигания определяет токсичность золошлаковых отходов при утилизации или размещении их в золошлакоотвалах.
В некоторых месторождениях углей и горючих сланцев установлены повышенные содержания германия, галлия, урана, скандия, молибдена, свинца и цинка, промышленное извлечение которых может существенно повысить экономический потенциал этих месторождений. Наличие в твердых горючих полезных ископаемых серы, радионуклидов, а также других элементов, образующих при использовании высокотоксичные, радиоактивные и сильно активные соединения (ртути, мышьяка, бериллия, фтора, урана, тория и др.) при массовом сжигании (переработке) может создать опасность загрязнения окружающей среды. Золошлаковые отходы сжигания углей и горючих сланцев могут быть не токсичными (V класс) или иметь различные классы токсичности.
Влага угля – массовая доля влаги (воды) в угле, в процентах (%). Влага в угле содержится в различных формах и количествах. Влага угля условно делится на влагу воздушно-сухого угля (внутреннюю: гигроскопическую, адсорбционную и химически связанную) и внешнюю (пленочную, капилярную и гравитационную, механически удерживаемую в порах). Оба вида составляют общую влагу угля, которая также называется "влагой рабочего топлива".
Вода в угле может быть связана с ним физико-механически (свободная гравитационная влага), физико-химически (гигроскопическая, пленочная и капиллярная влага) или химически (конституционная влага). Свободная гравитационная влага, поровая, пленочная, а также часть капиллярной влаги могут быть удалены механическими и термическими способами обезвоживания. Гигроскопическая влага удерживается адсорбционными силами и удаляется только термической сушкой. Химически связанная (конституционная) влага может быть удалена только при химической деструкции угля.
Основным направлением промышленного использования углей является энергетическое – сжигание в слоевых и факельных топках. В значительных масштабах спекающиеся каменные угли перерабатываются в металлургический кокс, в более ограниченном объеме угли поступают на полукоксование. При коксовании и полукоксовании углей получают также жидкие и газообразные продукты, являющиеся ценным химическим сырьем. Угли следует рассматривать как сырье для получения синтетического газообразного и жидкого топлива, пластических масс, буроугольного воска, высокоуглеродистых конструкционных и углеграфитовых материалов, гуминовых удобрений, а также для других целей. Зола и шлак от сжигания углей, отходы их добычи и обогащения используют в производстве строительных материалов. Перспективным является получение из отходов коксования и полукоксования углей глинозема, раскислителей, керамических, огнеупорных и абразивных материалов и другой продукции.
