
- •Д.м.н., профессор Апанасевич В.И.
- ••Злокачественные новообразования возникают в результате неограниченной пролиферации клеточного клона, выходящего за пределы собственной
- •Характерные признаки опухолевой клетки
- •Нормальный клеточный
- ••После получения промитотического внеклеточный сигнал , G1 циклин- CDK комплексы становятся активным. Они
- •Ингибиторы циклиновых
- •Прохождение через контрольные точки (cell checkpoints)
- •Изменение морфологии и движения
- •Отсутствие реплекативного
- •Изменение регуляции
- •Генетическая
- ••Канцерогенез – это многоступенчатый процесс накопления мутаций и других генетических изменений, приводящих к
- •Молекулярно-генетические изменения в злокачественных клетках
- •Онкогены
- •Структурные компоненты клетки (онкогены), вовлеченные в канцерогенез
- •Протоонкогены
- •Основные молекулярные механизмы активации протоонкогенов
- •Гены супрессоры
- •Мутация гена Р-53
- •Роль гена Р53 в опухолевом процессе
- •Существующие типы канцерогенеза
- •Травматический канцерогенез
- •Термический канцерогенез
- •Радиационный канцерогенез Ультрафиолетовое излучение
- •Радиационный канцерогенез Ионизирующая радиация
- •Химический канцерогенез
- •Эстрогенные гормоны
- •Тропные гормоны гипофиза
- •Метаболиты холестерола и желчных кислот
- •Метаболиты тирозина и триптофана
- •Экзогенные канцерогены
- ••Канцерогены локального действия вызывают развитие опухолей в месте аппликации (типичные представители этой группы
- ••Полициклические ароматические углеводороды (ПАУ) являются типичными проканцерогенами.
- •Куренье табака
- •Ароматические азосоединения и ароматические аминосоединения
- •Нитрозосоединения и
- •Природные неорганические канцерогены
- •Природные минеральные волокнистые материалы
- •Природные органические канцерогены
- •Органические вещества антропогенного происхождения
- •Вирусный канцерогенез
- •Симплексвирус 2 типа (Вирус простого герпеса 2 типа HHV-2)
- •Вирус герпеса человека 8 типа
- •Вирус Эпштейна—Барра
- •Вирус папилломы человека (HPV)
- •Онкорнавирусы
- •Этапность процесса химического канцерогенеза
- •Общие этапы
- •Спасибо за

Д.м.н., профессор Апанасевич В.И.
Канцерогенез

•Злокачественные новообразования возникают в результате неограниченной пролиферации клеточного клона, выходящего за пределы собственной ткани и способного к росту на территориях других тканей

Характерные признаки опухолевой клетки
•Нечувствительность к ростсупрессивным сигналам
•Самодостаточность в пролиферативных сигналах
•Генетическая нестабильность
•Блокировка клеточной дифференциации
•Отсутствие реплекативного старения (иммортализация)
•Ослабление индукции апоптоза
•Стимуляция неоангиогенеза
•Изменение морфологии / локомоции – инвазия , метастазирование
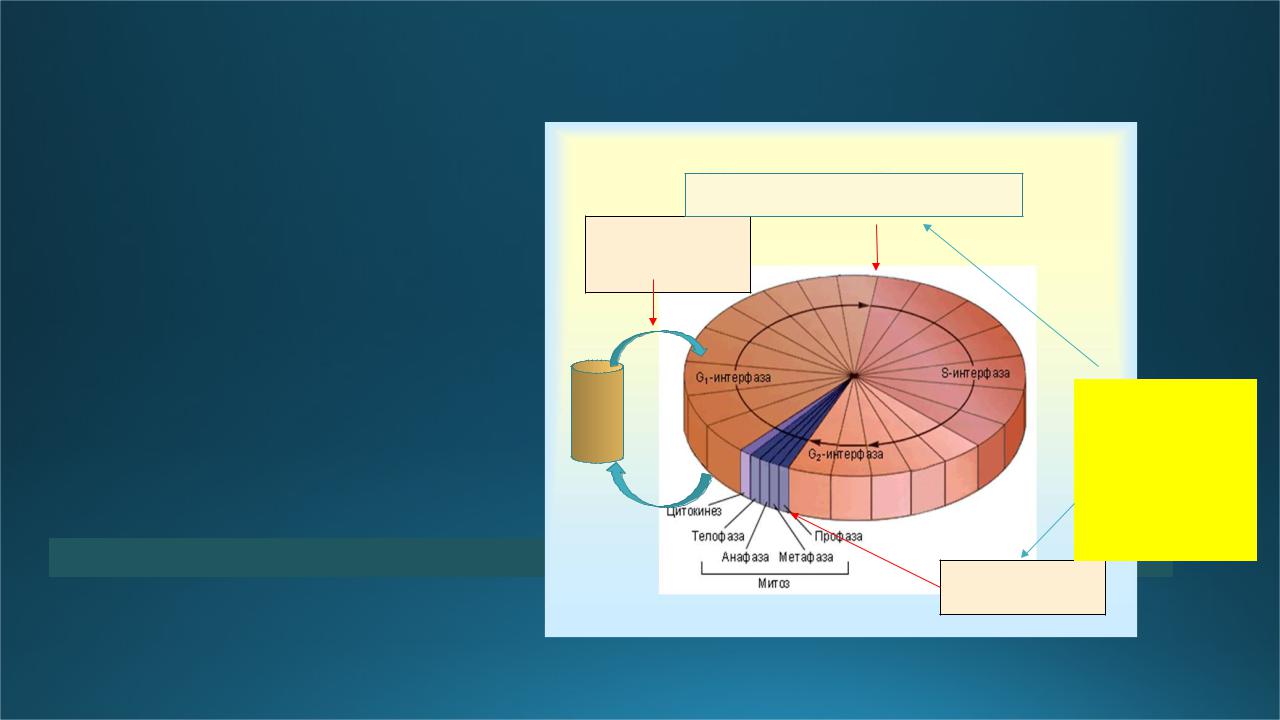
Нормальный клеточный
цикл
•G-1 - фаза – подготовка к синтезу ДНК (образование комплекса циклинов D(D-1 –D-3) с каталитической субединицей cdk4, cdk6)
•S- фаза –период репликации ДНК (переход обусловлен появлением комплекса циклина Е с каталитической субединицей cdk2)
•G-2- фаза подготовки к митозу
•М- митоз – процесс разделения клетки (переход к делению контролируется образованием комплекса циклина В с каталитической субединицей cdk1, (Сdk2)
•G-0- фаза покоя
Комплекс Е с cdk2
Комплекс D1- D3 с cdk4, cdk6
G-0
Группа белков CKI (ингибирова ние комплека cdk)
Комплекс В с cdk1, (Сdk2)

•После получения промитотического внеклеточный сигнал , G1 циклин- CDK комплексы становятся активным. Они подготовливают клетку для S фазы. Это в первую очередь синтез компонентов S циклинов и ферментов , необходимых для репликации ДНК .
•G1, циклин- CDK комплекс способствует деградации молекул , которые действуют как ингибиторы S фазе путем денатурации.
•Циклин Е производится , связывается с CDK2 , образуя циклин E- CDK2 комплекс, который толкает клетку от G1 к S фазе ( G1 / S , что, в свою очередь, инициирует G2 / M переход. Циклин B- cdc2 комплекс при активации вызывает разрушение ядерной оболочки что является началом профазы митоза

Ингибиторы циклиновых
киназ
• семейства генов, и синтезируемых на них белков способных предотвращать продвижение клеток по циклу. Эти гены играют важную роль в предотвращении образования опухоли, они известны как опухолевых супрессоров
• Cip / Kip (CDK взаимодействующий белок /Киназы ингибирующий белка) - p21, (инактивация CDK2 остановка в G1 )
-р27 (инактивация CDK2 остановка в G1 )
-p57(инактивация CDK2 остановка в G1 )
•INK4a/ARF (ингибитор киназы 4/Альтернативной рамки считывания) -p16INK4a, (инактивация CDK4 остановка в G1 )
•-p19ARF (предотвращение деградации Р53)
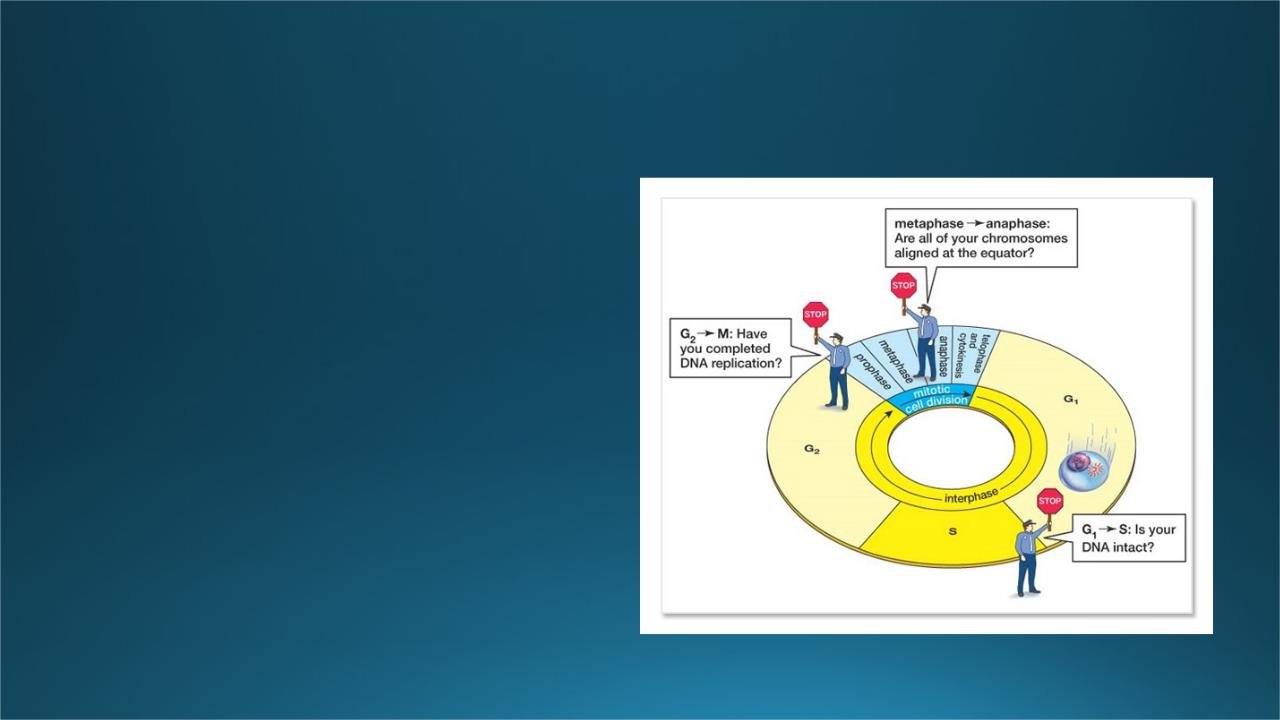
Прохождение через контрольные точки (cell checkpoints)
•Наличие трёх контрольных точек:
•G1-S – отсутствие повреждений ДНК
•G2-M – Правильное репликация ДНК
•Метафаза-анафаза – правильность расположения хромосом на экваторе.
•В G1-S и G2-M точках важнейшую роль играет ген Р53

Изменение морфологии и движения
клеток
•Ростовые факторы (цитокины) являются не только митогенами, но и моторогенами.
•Факторы движения клеток EGF, HGF/SF, PDGF, VGFR
•Характерны мутации протоонкогенов семейства RASчто ведет к появлению пула клеток с повышенной пролиферацией, измененной морфологией и увеличенной способностью к миграции.
•Это ведет к инвазивному росту и метастазированию.

Отсутствие реплекативного
старения• В норме человеческие клетки могут совершать 60-70 делений, после чего перестают размножаться и останавливаются в G-1 фазе
•В основе счетно-ограничительного механизма детерминирующего репликативное старение клеток лежит прогрессивное укорочение теломер (концевых отделов хромосом), представляющая собой более тысячи повторов TTAAGG.
•В норме при укорочении теломер до критического состояния происходит распознавание как нарушение структуры ДНК и остановка деления.
•Возникает «ранний кризис» после которого клетки перестают делиться. У части клеток происходит нарушение сигнальных систем, что что сопровождается делением клеток, пока теломеры практически не исчезнут.
•Затем концы хромосом слипаются что называется «генетической катастрофой».
•В опухолевых клетках имеется способность достраивать недореплицированные участки с помощью теломеразы.

Изменение регуляции
апоптоза• Апоптоз - вызывается разлиичными сигналами как физиологическим так и нефизиологическим – внутриклеточными повреждениями или неблагоприятными условиями.
•В основе – расщепление каспазами 3,6,7 ряда ключевых субстратов: ингибиторов нуклеаз, ламинов (ядерный цитоскелет)
•Опухолевые клетки имеют генетические изменения ведущие к ослаблению апоптоза:
•Потеря экспрессии на поверхности рецептора смерти FAS
•Нарушение проведения апоптотического сигнала (инактивацие белков Р- 53 и PTEN)
•Ингибирование проницаемости митохондриальной мембраны для цитохрома С и AIF
•Блокирование активации каспаз
•Резкое уменьшение времени жизни каспаз ввиду их соединения с белками IAP (Inhibiton of Apoptosis)
