- •Система единиц си. Основные и дополнительные единицы.
- •Здесь формула
- •Закон сохранения момента импульса точки
- •27. Энтропия, ее статистическое толкование
- •29. Испарение, конденсация, сублимация, плавление и кристаллизация.
- •30. Электрический заряд. Ионизация. Элементарный заряд. Закон сохранения электрического заряда.
27. Энтропия, ее статистическое толкование
Энтропия
является мерой неупорядоченности
системы.
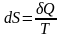
Изменение энтропии в замкнутой системе ∆S=0 –для обратимых циклов. ∆S>0 – для необратимых циклов
Изменение
энтропии при переходе из состояния 1 в
состояние 2
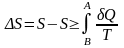 это следует из неравенства Клаузиуса
это следует из неравенства Клаузиуса
Из закона возрастания энтропии родилась теория «тепловой смерти» Вселенной. тепловая смерть — термин, описывающий конечное состояние любой замкнутой термодинамической системы, и Вселенной в частности. Т.е. Вселенная должна прийти в состояние полного термодинамического равновесия (состояние «тепловой смерти»). Но вселенная, наполненная тяготеющим веществом должна сжиматься или расширятся
3-ий
закон термодинамики. Энтропия
S
равновесной системы стремится к конечному
пределу, не зависящему от давления,
плотности, других термодинамических
параметров или фазы, при стремлении
температуры к абсолютному нулю.
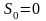
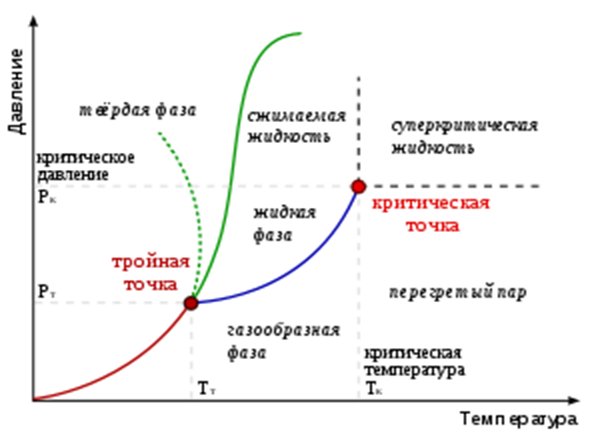
28. фазовые переходы 1 и 2 рода. Тройная точка.
Фазой называется термодинамически равновесное состояние вещества, отличающееся по физическим свойствам от других равновесных состояний того же вещества. Если, например, в закрытом сосуде находится вода, то эта система является двухфазной: жидкая фаза — вода; газообразная фаза — смесь воздуха с водяными парами. Если в воду бросить кусочки льда, то эта система станет трехфазной, в которой лед является твердой фазой. Переход вещества из одной фазы в другую — фазовый переход — всегда связан с качественными изменениями свойств вещества. (например, переход кристаллического вещества из одной модификации в другую).
Фазовый переход I рода (например, плавление, кристаллизация и т. д.) сопровождается поглощением или выделением теплоты, называемой теплотой фазового перехода. Фазовые переходы 1 рода характеризуются постоянством температуры, изменениями энтропии и объема. Объяснение этому можно дать следующим образом. В подобных переходах — из более упорядоченного кристаллического состояния в менее упорядоченное жидкое состояние — степень беспорядка увеличивается, т. е., согласно второму началу термодинамики, этот процесс связан с возрастанием энтропии системы. Если переход происходит в обратном направлении (кристаллизация), то система теплоту выделяет.
Фазовые переходы, не связанные с поглощением или выделением теплоты и изменением объема, называются фазовыми переходами II рода. Эти переходы характеризуются постоянством объема и энтропии, но скачкообразным изменением теплоемкости. фазовые переходы II рода связаны с изменением симметрии: выше точки перехода система, как правило, обладает более высокой симметрией, чем ниже точки перехода. Примером является превращение обыкновенного жидкого гелия (при Т — 2,9 К) в другую жидкую модификацию (гелий II), обладающую свойствами сверхтекучести.
Тройная точка -точка пересечения кривых фазового равновесия состояния в-ва, соответствующая устойчивому равновесию трёх фаз, обычно твёрдой, жидкой и газообразной. Напр., Т.т. воды соответствует равновесному состоянию системы из льда, воды и водяного пара.