
- •Вопрос1
- •Вопрос 2
- •Вопрос 3
- •Вопрос 4
- •Вопрос 5.
- •Вопрос 6.
- •Вопрос 6.
- •Вопрос 8
- •Вопрос 9.
- •Вопрос 10.
- •Вопрос 11.
- •Вопрос 12.
- •Вопрос 13.
- •Вопрос 14
- •Вопрос 15
- •Вопрос 16
- •Вопрос 17
- •Вопрос 18
- •Вопрос 19
- •Вопрос 20
- •Вопрос 21
- •Вопрос 22
- •Вопрос 23
- •Вопрос 24
- •Вопрос 25
- •Вопрос 26
- •Вопрос 27
- •Вопрос 28(зошпышоп)))
- •Вопрос 29
- •Вопрос 30
- •Вопрос 32
- •Вопрос 33
- •Вопрос 34
- •Вопрос 35
- •Вопрос 36
- •Вопрос 37
Вопрос 14
Диаграмма состояния и правило фаз Гиббса
Диаграммой состояния называет геометрическое изображение равновесных состояний термодинамической системы при различных значениях параметров (температуры Т, давления Р, концентрации компонентов xi, молярного объёма V и др.). Диаграмма состояния даёт информацию о фазовом составе системы в зависимости от параметров.
Правило фаз Гиббса представляет собой математическое выражение условия равновесия системы, показывающее количественную зависимость между числом степеней свободы системы С и числом компонентов k и фаз f.
C = k-f+n
Вопрос 15
Однофазовая диаграмма состояния
Однофазовые диаграммы состояний – это графики, на которых в зависимости от давления, объема и температуры изображают фазовые состояния только одного материала.
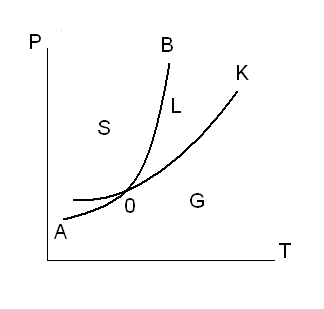
На диаграмме четко разграничены области, в которых материал может существовать только в одном агрегатном (фазовом) состоянии – как твердое тело, жидкость или газ. Вдоль разграничительных линий вещество может иметь два агрегатных состояния (две фазы), находящихся в равновесии друг с другом.
В точке пересечения линий диаграммы, так называемой тройной точке (точка О на рисунке), могут одновременно существовать все три фазы(лед вода пар).
O – равновесие трёх фаз, тройная точка; ОК – кривая испарения или конденсации; OB – кривая плавления или кристаллизации; ОА- кривая сублимации или возгонки А, K, B – критические точки, в точке К исчезает различие агрегатных состояний газ – жидкость (G – L); в точке В – агрегатных состояний жидкость – твердое тело (L – S); в точке А – агрегатных состояний твердое тело – газ (S – G).
Вопрос 16
Диаграмма состояния для сплавов с неограниченной растворимостью в твердом состоянии
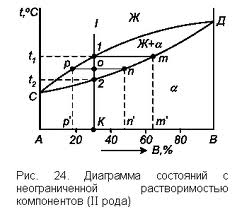
Диаграмма состоит из трех областей: жидкость, жидкость и твердый раствор и твердый раствор
Линия С1Д является линией ликвидус – то есть линией начала кристаллизации, линия С2Д – линия солидуса, т.е. линия конца кристаллизации.
Точка 1 соответсвует начачу кристаллизации, а точка 2 – концу. Между ними сплав может находится в двухфазном состоянии. Концентрауия и количесвто фаз у сплава лежащего между линиями солидуси ликвидус, определяются правилось отрезков. Например, в точке О сплав состоит из жидкости, состава определяемого в точке p и твердой фазы состава определяемого в точке n.
Вопрос 17
Правило отрезков (рычага)
Чтобы определить концентрации компонентов в фазах через данную точку, характеризующую состояние сплава, проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область; проекции точек пересечения на ось концентрация показывают составы фаз.
Для того чтобы определить количественное соотношение фаз через заданную точку проводят горизонтальную линию. Отрезки этой линии между заданной точкой и точками, определяющими составы фаз, обратно пропорциональны количествам этих фаз.
Вопрос 18
Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов
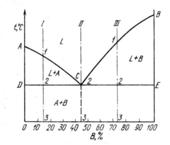
жидкость L, кристаллы А и кристаллы В (максимальное значение f= 3).
Линия АСВ является линией ликвидус (начало кристаллизации), линияDCE— линией солидус (конец кристаллизации). На линии АС начинают (при охлаждении) выделяться кристаллы A, а на линии СВ — кристаллы В. На линии DCEиз жидкости концентрации С одновременно выделяются кристаллы А и В.
