
- •1. Взаимодействие фотонов оптического излучения с молекулами. Квантово-механические основы и последствия.
- •1.1. Основные характеристики оптического излучения
- •1.2. Основные квантово-механические механизмы взаимодействия оптического излучения с атомами и молекулами
- •1.3. Электронные переходы в атомах и молекулах при поглощении квантов оптического излучения.
- •2. Законы поглощения света веществом. Спектрофотометрический анализ. Особенности спектрофотометрии биологических объектов. Некоторые специальные методы спектрофотометрического анализа.
- •2.1. Количественное описание поглощения света растворами. Закон Бугера-Ламберта-Бера.
- •2.2. Условия выполнения закона Бугера-Ламберта-Бера.
- •2.3. Качественный и количественный спектрофотометрический анализ.
- •2.3.1. Качественный спектрофотометрический анализ.
- •2.3.2. Количественный спектрофотометрический анализ.
- •2.4. Некоторые специальные методы спектрофотометрии
- •2.5. Особенности спектрофотометрии биологических объектов
- •Оптические неоднородности
- •3. Вторичное излучение света молекулами объекта. Люминесцентный анализ и особенности его использования для исследования биологических объектов.
- •3.1. Явление фотолюминесценции
- •3.2. Электронные переходы в возбужденной молекуле. Законы люминесценции.
- •3.3. Зависимость интенсивности фотолюминесценции от концентрации люминесцирующих молекул. Люминесцентный анализ.
- •3.4. Методы регистрации фотолюминесценции. Спектрофлуориметры. Особенности флуориметрии биологических объектов.
- •3.5. Время жизни возбужденного состояния молекул. Связь между временем жизни возбужденных состояний и квантовым выходом фотолюминесценции.
- •3.6. Влияние окружения люминесцирующих молекул на параметры фотолюминесценции. Флуоресцентные зонды и метки.
- •3.7. Причины снижения интенсивности фотолюминесценции в биологических объектах. Тушение фотолюминесценции. Миграция энергии электронного возбуждения.
- •3.8. Поляризация фотолюминесценции.
- •3.9. Замедленная флуоресценция и фосфоресценция.
- •3.10. Хемилюминесценция биологических систем. Хемилюминесцентный анализ.
- •3.11. Проточная цитофлуориметрия.
- •3.12. Влияние размера люминесцирующей полупроводниковой частицы на ее свойства как люминофора. Квантовые точки.
- •В обычных полупроводниках радиус экситона Бора (ах) определяет размер областей электронного возбуждения.
- •Применение квантовых точек в качестве флуорофоров в медицине и биологии
- •Молекулярные сенсоры
- •Молекулярная диагностика
- •Гибридные молекулярные устройства
- •4.Биофизические основы некоторых фотобиологических процессов. Применение оптического излучения в медицине.
- •4.1. Общие закономерности фотохимических процессов в биомолекулах.
- •4.1.1. Кинетика однофотонных необратимых фотохимических реакций
- •4.1.2. Кинетика однофотонных обратимых фотохимических реакций
- •4.1.2. Кинетика многофотонных фотохимических реакций
- •4.2. Спектры действия фотопревращений молекул и фотобиологических процессов.
- •4.2.1 Спектры действия фотобиологических эффект при небольшой постоянной дозе облучения
- •4.2.2.Спектры действия при постоянной величине фотобиологического эффекта.
- •4.2.3.Спектры действия биологических ответов, зависящих от скорости фотопревращения активных молекул.
- •4.3. Фотомодификация олигомерных и однокомпонентных белков под действием ультрафиолетового излучения.
- •4.3.1. Естественное (солнечное) ультрафиолетовое излучение.
- •4.3.2. Кинетика фотоинактивации белковых молекул.
- •4.3.3. Природа первичных продуктов фотолиза аминокислот и их остатков в белках.
- •Значения для
- •4.4. Действие ультрафиолетового излучения на биологические мембраны.
- •4.5. Действие ультрафиолетового излучения на нуклеиновые кислоты.
3.9. Замедленная флуоресценция и фосфоресценция.
Измерение времен жизни возбужденных состояний в ряде фотолюминесцирующих объектов позволило выявить тип вторичного свечения, спектральные характеристики которого указывали на то, что это – флуоресценция, а величина времени жизни возбужденного состояния излучающих молекул – на то, что это триплетные возбуждения. Далее было показано, что вклад этого типа вторичного свечения в общую интенсивность флуоресценции нарастает по мере увеличения температуры образца. На основании этих данных было предположено, что подобный вид вторичного свечения связан с тем, что часть электронов с триплетного уровня Т1 (см. рис. 15) попадает не на основной синглетный уровень S0, а на возбужденную синглетную орбиталь S1, откуда и осуществляется излучательный переход. Иными словами, электронные переходы в молекуле люминофора при рассматриваемом типе фотолюминесценции могут быть описаны следующей схемой:
![]()
В этой схеме Е – величина энергии, которую должен затратить электрон при переходе с Т1 на S1, поскольку триплет-синглетный переход (интеркомбинационная конверсия) требует от электрона изменения спина, а в данном случае – еще и попадания на наиболее высокий колебательный подуровень орбитали Т1. Последнее обстоятельство объясняет тот факт, что вклад данного вторичного свечения в общую интенсивность флуоресценции образца возрастает с ростом температуры.
Рассмотренный тип фотолюминесценции носит название замедленная флуоресценция. Как и в случае фосфоресценции, интенсивность замедленной флуоресценции в обычных условиях (в жидких растворах и в присутствии кислорода) очень мала, поскольку большая часть триплетно-возбужденных молекул люминофора в такой ситуации инактивируется безизлучательно.
У большинства способных к фотолюминесценции соединений в замороженных растворах при низкой температуре (например, при 77о К) помимо флуоресценции выявляется более длинноволновая полоса вторичного свечения (рис. 24). Эта полоса связана с излучательным электронным переходом с триплетной орбитали Т1 на основной синглетный уровень S0 (рис. 15). Обусловленная таким переходом фотолюминесценция, как уже указывалось выше, носит название фосфоресценция. Её характерной особенностью является относительно медленное затухание после прекращения возбуждения молекул в объекте. В некоторых случаях регистрируемая фосфоресценция может сохраняться в течение нескольких секунд.
Поскольку переход Т1 S0 требует от электрона преодоления энергетического барьера, связанного с необходимостью изменения спина, строго говоря, он является запрещенным. Поэтому молекулы с электроном, находящимся на триплетном уровне, могут пребывать в возбужденном состоянии достаточно долго. Например, истинное время жизни триплетно-возбужденных молекул триптофана составляет около 4 секунд (для сравнения истинное время жизни синглетных возбуждений у этой аминокислоты – 10-9 секунды).
Из-за большого истинного времени жизни триплетных возбуждений с ростом температуры вероятность безизлучательного их тушения растет намного быстрее, чем у синглетных. Соответственно, квантовый выход фосфоресценции в обычных условиях очень мал. При 20-25оС лишь изредка в молекулах крупных белков можно зарегистрировать фосфоресценцию ароматических аминокислотных остатков в виде «плеча» на длинноволновом склоне полосы флуоресценции с помощью флуориметров обычного типа.
J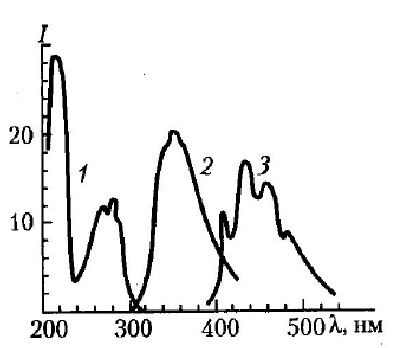
Рисунок 24. Спектры возбуждения фотолюминесценции (1), флуоресценции (2) и фосфоресценции (3) триптофана. J – регистрируемая интенсивность вторичного свечения.
Публикуется с модификациями по: Владимиров Ю.А., Потапенко А.Я. Физико-химические основы фотобиологических процессов. М.: «Дрофа», 2006, с. 77.
Поскольку времена затухания вторичного свечения после прекращения генерации новых возбужденных состояний у флуоресценции и фосфоресценции сильно различаются, для измерения параметров фосфоресценции удобно применять специальные оптические приборы – фосфороскопы (рис. 25). Принцип работы этих устройств состоит в том, что фотолюминесценция образца в них регистрируется после перекрывания возбуждающего излучения.
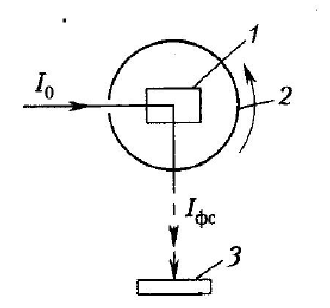
Рисунок 25. Схема устройства фосфороскопа. 1 – кювета с образцом; 2 – вращающийся цилиндр с прорезями; 3 – фотодетектор; J0 – возбуждающее излучение; Jфс – фосфоресценция образца.
Публикуется с модификациями по: Владимиров Ю.А., Потапенко А.Я. Физико-химические основы фотобиологических процессов. М.: «Дрофа», 2006, с. 78.
Фосфороскоп позволяет регистрировать спектры фосфоресценции при комнатной температуре, несмотря на ее низкую интенсивность. Особенно значимы оказались измерения характеристик этого вида фотолюминесценции у мембранных белков, которые, как оказалось, являются весьма чувствительны к состоянию мембранных структур.
Поскольку в большинстве случаев реальное время жизни у триплетно-возбужденных молекул при низких температурах (порядка 77о К) достаточно велико, проводить измерение этого показателя значительно проще, чем в случае синглетного возбуждения: удается прямо регистрировать кинетики затухания фосфоресценции после прекращения возбуждения в режиме реального времени. Лишь в некоторых случаях приходится прибегать к специальным приемам. Например, при определении величины у порфиринов (она составляет порядка 10-4 с) возбуждение молекул образца осуществлялось короткой вспышкой высокоинтенсивного излучения, а для регистрации затухания свечения применялись быстродействующие осциллографы. В таблице 3 приведены величины времен жизни фосфоресценции для некоторых белков при разной температуре.
Таблица 3. Времена жизни фосфоресценции ряда белков (в секундах) в буферном растворе при разной температуре.
Публикуется с модификациями по: Владимиров Ю.А., Потапенко А.Я. Физико-химические основы фотобиологических процессов. М.: «Дрофа», 2006, с. 84.
|
Температура, оС |
Рибонуклеаза Т1 (фосфоресцируют остатки тирозина) |
Лактатдегидрогеназа (фосфоресцируют остатки триптофана) |
Щелочная фосфатаза (фосфоресцируют остатки триптофана) |
|
1 |
0,093 |
1,40 |
3,3 |
|
10 |
0,050 |
0,97 |
2,61 |
|
20 |
0,031 |
0,59 |
1,76 |
|
30 |
0,025 |
0,29 |
1,22 |
|
40 |
- |
0,15 |
0,75 |
Обратите внимание на то, что измерения величины для фосфоресценции этих протеинов осуществлялись при достаточно высоких температурах. Это оказалось возможным вследствие применения высокочувствительных фосфороскопов и благодаря тому, что ароматические аминокислотные остатки располагаются в этих белках внутри белковых глобул, где их подвижность и доступность для тушителей снижены.
Сопоставление величины для триплетных возбуждений в разных белках позволило установить, что микровязкость окружения ароматических аминокислотных остатков внутри белковых глобул сильно (в пределах от 0,1 до 106 Пас) варьирует. Оказалось также, что изменение конформации белковых молекул (например, вследствие связывания субстрата с активным центром у ферментов) весьма сильно сказывается на величине фосфоресценции остатков ароматических аминокислот в их составе.
Следует заметить, что в живых клетках фосфоресценция ароматических аминокислотных остатков в цитоплазматических протеинах значительно ослаблена из-за наличия кислорода. Для кислорода триплетное состояние является основным, поэтому его молекулы очень эффективно тушат триплетно-возбужденные молекулы других веществ. Основной вклад в регистрируемую клеточную фосфоресценцию клеток вносят поэтому мембранные белки, доступ кислорода к ароматическим аминокислотным остаткам которых ограничен.
