
- •1. Взаимодействие фотонов оптического излучения с молекулами. Квантово-механические основы и последствия.
- •1.1. Основные характеристики оптического излучения
- •1.2. Основные квантово-механические механизмы взаимодействия оптического излучения с атомами и молекулами
- •1.3. Электронные переходы в атомах и молекулах при поглощении квантов оптического излучения.
- •2. Законы поглощения света веществом. Спектрофотометрический анализ. Особенности спектрофотометрии биологических объектов. Некоторые специальные методы спектрофотометрического анализа.
- •2.1. Количественное описание поглощения света растворами. Закон Бугера-Ламберта-Бера.
- •2.2. Условия выполнения закона Бугера-Ламберта-Бера.
- •2.3. Качественный и количественный спектрофотометрический анализ.
- •2.3.1. Качественный спектрофотометрический анализ.
- •2.3.2. Количественный спектрофотометрический анализ.
- •2.4. Некоторые специальные методы спектрофотометрии
- •2.5. Особенности спектрофотометрии биологических объектов
- •Оптические неоднородности
- •3. Вторичное излучение света молекулами объекта. Люминесцентный анализ и особенности его использования для исследования биологических объектов.
- •3.1. Явление фотолюминесценции
- •3.2. Электронные переходы в возбужденной молекуле. Законы люминесценции.
- •3.3. Зависимость интенсивности фотолюминесценции от концентрации люминесцирующих молекул. Люминесцентный анализ.
- •3.4. Методы регистрации фотолюминесценции. Спектрофлуориметры. Особенности флуориметрии биологических объектов.
- •3.5. Время жизни возбужденного состояния молекул. Связь между временем жизни возбужденных состояний и квантовым выходом фотолюминесценции.
- •3.6. Влияние окружения люминесцирующих молекул на параметры фотолюминесценции. Флуоресцентные зонды и метки.
- •3.7. Причины снижения интенсивности фотолюминесценции в биологических объектах. Тушение фотолюминесценции. Миграция энергии электронного возбуждения.
- •3.8. Поляризация фотолюминесценции.
- •3.9. Замедленная флуоресценция и фосфоресценция.
- •3.10. Хемилюминесценция биологических систем. Хемилюминесцентный анализ.
- •3.11. Проточная цитофлуориметрия.
- •3.12. Влияние размера люминесцирующей полупроводниковой частицы на ее свойства как люминофора. Квантовые точки.
- •В обычных полупроводниках радиус экситона Бора (ах) определяет размер областей электронного возбуждения.
- •Применение квантовых точек в качестве флуорофоров в медицине и биологии
- •Молекулярные сенсоры
- •Молекулярная диагностика
- •Гибридные молекулярные устройства
- •4.Биофизические основы некоторых фотобиологических процессов. Применение оптического излучения в медицине.
- •4.1. Общие закономерности фотохимических процессов в биомолекулах.
- •4.1.1. Кинетика однофотонных необратимых фотохимических реакций
- •4.1.2. Кинетика однофотонных обратимых фотохимических реакций
- •4.1.2. Кинетика многофотонных фотохимических реакций
- •4.2. Спектры действия фотопревращений молекул и фотобиологических процессов.
- •4.2.1 Спектры действия фотобиологических эффект при небольшой постоянной дозе облучения
- •4.2.2.Спектры действия при постоянной величине фотобиологического эффекта.
- •4.2.3.Спектры действия биологических ответов, зависящих от скорости фотопревращения активных молекул.
- •4.3. Фотомодификация олигомерных и однокомпонентных белков под действием ультрафиолетового излучения.
- •4.3.1. Естественное (солнечное) ультрафиолетовое излучение.
- •4.3.2. Кинетика фотоинактивации белковых молекул.
- •4.3.3. Природа первичных продуктов фотолиза аминокислот и их остатков в белках.
- •Значения для
- •4.4. Действие ультрафиолетового излучения на биологические мембраны.
- •4.5. Действие ультрафиолетового излучения на нуклеиновые кислоты.
4.3.3. Природа первичных продуктов фотолиза аминокислот и их остатков в белках.
После поглощения кванта ультрафиолетового излучения часть ароматических аминокислот (и их остатков в белках) фотоионизируется. При этом формируется катион-радикал соответствующей аминокислоты и свободный электрон. В водной среде свободный электрон быстро окружается ориентированными молекулами растворителя, формирующими вокруг него сольватационную оболочку. Эта оболочка тормозит взаимодействие электрона с молекулами объекта, увеличивая время его пребывания в свободном виде. Такой электрон, окруженный сольватационной оболочкой, принято называть сольватированным. Ход событий, следующих за поглощением кванта излучения ароматической аминокислотой (тирозином, триптофаном или фенилаланином), может, таким образом, описан следующим уравнением:
![]()
В замороженных образцах, при температуре жидкого азота (-196о С), появление сольватированных электронов в растворах ароматических аминокислот при их УФ облучении может быть обнаружено по появлению фиолетовой окраски. Эта окраска связана с тем, что сольватированные электроны обладают способностью к поглощению света, а максимум в их спектре поглощения приходится на 600 нм. Сольватированные электроны могут также быть выявлены с помощью ЭПР.
Интересно, что при освещении замороженных облученных растворов ароматических аминокислот красным излучением (вблизи 600 нм) наблюдается обратная фотоионизации фотохимическая реакция:
![]()
Как видно из приведенного уравнения, при обратной реакции часть получившихся в результате нее молекул аминокислоты пребывает в электронно-возбужденном состоянии. Как следствие, в таких случаях при освещении замороженного образца красным излучением можно наблюдать его свечение в синефиолетовой и ультрафиолетовой областях спектра (соответствующее фосфо- и флуоресценции изучаемой ароматической аминокислоты):

Указанное явление получило название индуцированной светом люминесценции.
При достаточно высокой температуре сольватированный электрон может разрушить и за счет тепловой энергии. Следующая за этим обратная рекомбинация свободных электронов и катион-радикалов ароматических аминокислот приводит к появлению триплетно-возбужденных молекул. Часть таких молекул затем высвечивает кванты фосфоресценции. В результате нагревание ранее охлажденного облученного УФ излучением раствора ароматической аминокислоты приводит к его свечению, которое соответствует спектру фосфоресценции изучаемой аминокислоты и носит название термолюминесценция:
![]()
Из написанного выше видно, что генерируемые после поглощения кванта ультрафиолетового излучения фотофизические и фотохимические сдвиги в молекулах ароматических аминокислот в принципе обратимы. Если бы все первичные фотопродукты этих аминокислот всегда рекомбинировали, никаких необратимых фотопревращений не наблюдалось бы. Но это не так. Значительная часть сольватированных электронов и катион-радикалов аминокислот не рекомбинирует, а вступает в другие реакции.
В частности, известно, что катион-радикал ароматической амнокислоты сам является очень сильной кислотой и при температурах от 77 до 140о К легко диссоциирует с высвобождением протона и формированием нейтрального радикала:
![]()
На основании анализа спектров фотолюминесценции и возбуждения фотолюминесценции продуктов фотолиза ароматических аминокислот в различных условиях постулировано существование следующих форм их нейтральных радикалов:
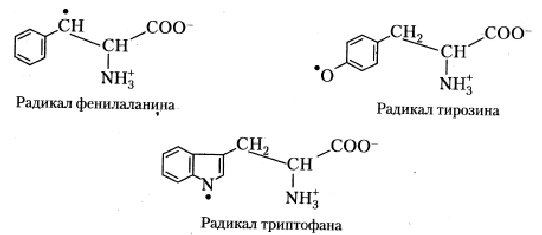
В отличие от нейтральных радикалов тирозина и фенилаланина, нейтральный радикал триптофана весьма нестабилен и быстро меняет свою структуру с формированием соединения следующего типа:
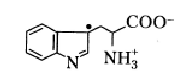
Неспаренный электрон в этом соединении локализован на 3-м углеродном атоме индольного кольца.
Вообще говоря, все нейтральные радикалы ароматических аминокислот – очень нестабильные и химически активные соединения. При температурах выше 160-200о К эти радикалы активно вступают в дальнейшие взаимодействия. Эти взаимодействия можно условно разделить на 2 типа: протекающие в присутствии кислорода и не требующие его участия.
В присутствии кислорода наблюдается фотоокисление ароматических аминокислот, которое, вероятно, протекает следующим образом:
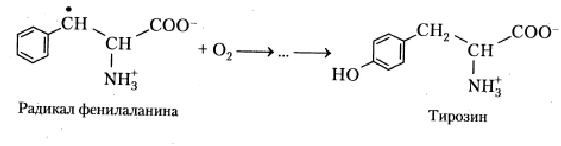

Хотя подробно механизмы взаимодействия между нейтральными радикалами аминокислот и конечными продуктами их фотоокисления еще не изучены, изучение кинетик хемилюминесценции облученных аминокислотных растворов показывает, что, скорее всего, процесс протекает через стадию формирования перекисей:
цепное
окисление
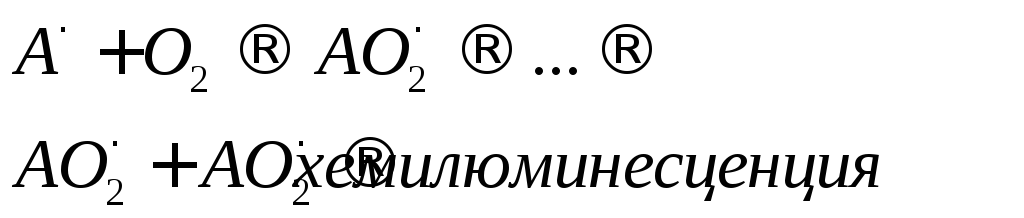
Значительный вклад в фотохимическую модификацию белковых молекул вносят реакции с участием сольватированного электрона. Особенно чувствительны к его действию остатки цистина и цистеина. Взаимодействие выбитых из остатков ароматических аминокислот сольватированных электронов с данными остатками приводит к их быстрому разрушению:
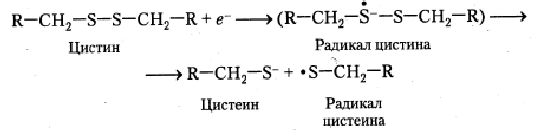
Рекомбинация радикалов цистеина приводит к формированию цистина:
![]()
Если же в системе имеется кислород, цистеиновые радикалы могут взаимодействовать и с ним, формируя цистеинсульфоновую кислоту:

Сольватированные электроны могут также вступать во взаимодействие с некоторыми алифатическими аминокислотными остатками, например, с остатком глицина, хотя этот процесс протекает существенно менее эффективно, чем разрушение под их влиянием цистина и цистеина:
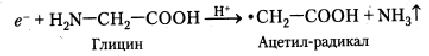
Наконец, в присутствии алифатических дипептидов (например, глицил-глицина) фотоионизация ароматических аминокислотных остатков может привести к появлению анион-радикалов пептидных групп. Дальнейшие превращения этих радикалов заканчиваются разрушением пептидных связей следующим путём:
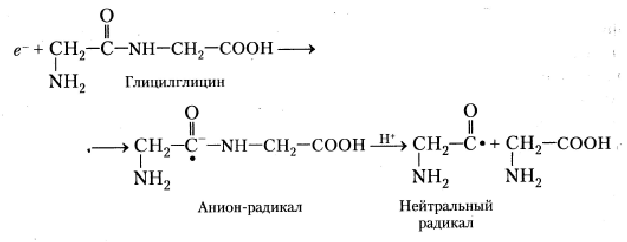
В заключение этого раздела приведем величины квантовых выходов () фоторазрушения ряда аминокислот и аминокислотных (табл. 5) и общую схему процессов, сопровождающих фотохимическую модификацию белковых молекул.
Таблица 5. Квантовые выходы () фотолиза для некоторых аминокислот и их остатков составе белков.
Публикуется с модификациями по: Владимиров Ю.А., Потапенко А.Я. Физико-химические основы фотобиологических процессов. М.: «Дрофа», 2006, с. 131.
