
- •Физическая и термодинамическая характеристика воды, связанной биомакромолекулами.
- •2. Свободная и связанная вода в пшеничном тесте. Методы определения связанной воды.
- •3.Взаимодействие воды с углеводами.
- •Взаимодействие воды с белками. Гидротация.
- •Роль воды в развитии микроорганизмов на сырье и пищевых продуктах.
- •Классификация белков. Биологические функции белков.
- •Биологические функции белков.
- •8. Биологическая ценность белков как компонентов пищи. Аминокислотный скор.
- •9. Суточная потребность организма человека в белках и аминокислотах. Степень усвоения белка. Азотный баланс.
- •Азотный баланс.
- •Переваривание белков в желудке
- •12.Переваривание белков в тонком кишечнике
- •Основные пути метаболизма аминокислот в печени.
- •13.Гидротация белков.
- •3. Пенообразование.
- •14. Пищевые аллергии.
- •Белково-коллоидная недостаточность или квашиоркор.
- •Основные свойства ферментов. Номенклатура и активность ферментативных препаратов.
- •Номенклатура ферментативных препаратов.
- •Ферментные препараты, используемые в отраслях пищевой промышленности перерабатывающих растительное сырье.
- •Биологические функции и пищевая ценность углеводов. Классификация углеводов, нормы потребления
- •21. Превращения углеводов в технологических процессах (клейстеризация и гидролиз крахмала, карамелизация сахаров и меланоидинообразование)
- •22. Гликозиды растений
- •Состав, свойства и функции липидов в организме
- •Простые и сложные липиды
- •1.Превращение липидов и их влияние на качество продуктов при хранении и переработке
- •27. Переваривание жиров
- •28. Метаболизм жирных кислот в печени
13.Гидротация белков.
Белки связывают воду, то есть проявляют гидрофильные свойства, при этом они набухают, увеличивается их масса и объём. Набухание белка сопровождается его частичным растворением. Гидрофильность отдельных белков зависит от их строения.
Благодаря наличию на поверхности белковых глобул, групп несущих положительный или отрицательный заряд, вокруг молекулы белка образуется гидратная оболочка, которая препятствует агрегации, а следовательно способствует устойчивости растворов белка и препятствует их осаждению. В ИЭТ белки обладают наименьшей способностью связывать
воду, происходит разрушение гидратной оболочки, поэтому преобразуются крупные агрегуты белковых молекул. Агрегация белка происходит и при обезвоживании с помощью некоторых органических растворителей . При изменении рН среды макромолакулы белка становятся заряжены и его гидротационная способность меняется. При ограниченном набухании концентрированные белковые растворы образуют сложные системы называемые студнями. Они не обладают текучестью, упруги, пластичны, обладают определённой механической прочностью и способны сохранять свою форму. Глобулярные белки могут полностью гидротироваться, растворяясь в воде, образуя растворы с невысокой концентрацией, например белки молока. Гидрофобные свойства белков, то есть их способность набухать, образовывать студни, стабилизировать эмульсии, суспензии и пены, имеет большое значение в биологии и пищевой промышленности при хранении и переработке зерна , выпечке хлеба, производства макаронных изделий и т.д.различная гидрофильность белков – один из важнейших признаков зерна сильной и слабой пшеницы. Сильно гидротированным студнем является сырая клейковина, выделенная из пшеничного теста. Она содержит до 65% воды. Различная гидрофильность клейковинных белков один из признаков, характеризующих качество зерна и полученной из него муки.
Денатурация белков- это сложный процесс при котором под влиянием внешних факторов происходит изменение двоичной, третичной и четвертичной структуры белковой макромолекулы, то есть её нативной пространственной структуры. Первичная структура, а значит и химический состав балка не меняются. Денатурация изменяет первоначальные свойства белковых веществ. При этом увеличивается реактивность некоторых химических групп, входящих в состав молекулы, пояпляются свободные группы(сульфгидрильные и др.), уменьшается растворимость, гидрофильность, ферментативная активность, изменяется форма или величина белковой молекулы, увеличивается её ассиметрия, облегчается воздействие на белки протеолитических ферментов, а следовательно он легче гидролизуется.в пищевой технологии особое практическое значение имеет тепловая денатурация белков. Нагревание вызывает разрыв водородных связей и нарушает взаимодействие гидрофобных групп. Тепловая денатурация белков наиболее часто наблюдается при сушке зерна, если она ведётся с нарушением установленных правил, а также в результате самосогревания.
При нагреве до
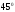 всхожесть зерна не меняется. При
температуре
всхожесть зерна не меняется. При
температуре снижаются хлебопекарные свойства,
особенно зерна пшеницы. Степень тепловой
денатурации зависит от температуры,
продолжительности нагрева и влажности.
Это необходимо помнить при разработке
режимов термообработки пищевого сырья,
полуфабрикатов, а иногда и готовых
продуктов. Особую роль в процессе
тепловой денатурации играет при
бланшировании растительного сырья,
выпечке хлеба, получении макаронных
изделий. Физические, химические и
биологические способы денатурации
широко используются в пищевой
промышленности и биотехнологии.
снижаются хлебопекарные свойства,
особенно зерна пшеницы. Степень тепловой
денатурации зависит от температуры,
продолжительности нагрева и влажности.
Это необходимо помнить при разработке
режимов термообработки пищевого сырья,
полуфабрикатов, а иногда и готовых
продуктов. Особую роль в процессе
тепловой денатурации играет при
бланшировании растительного сырья,
выпечке хлеба, получении макаронных
изделий. Физические, химические и
биологические способы денатурации
широко используются в пищевой
промышленности и биотехнологии.
