
- •Конспект лекций
- •От авторов
- •Введение
- •Лекция 1. Электростатика в вакууме и веществе. Электрическое поле
- •1.1. Предмет классической электродинамики
- •1.2. Электрический заряд и его дискретность. Теория близкодействия
- •1.3. Закон Кулона. Напряженность электрического поля. Принцип суперпозиции электрических полей
- •1.3.1. Границы применимости закона Кулона
- •1.3.2. Принцип суперпозиции электрических полей. Электрическое поле диполя
- •1.4. Поток вектора напряженности электростатического поля
- •1.5. Теорема Остроградского-Гаусса для электрического поля в вакууме
- •1.6. Работа электрического поля по перемещению электрического заряда. Циркуляция вектора напряженности электрического поля
- •1.7. Энергия электрического заряда в электрическом поле
- •1.8. Потенциал и разность потенциалов электрического поля. Связь напряженности электрического поля с его потенциалом
- •1.8.1. Потенциал и разность потенциалов электрического поля
- •1.8.2. Связь напряженности электрического поля с его потенциалом
- •1.9. Эквипотенциальные поверхности
- •1.10. Основные уравнения электростатики в вакууме
- •1.11. Некоторые примеры электрических полей, порождаемых простейшими системами электрических зарядов
- •1.11.1. Электрическое поле, порождаемое бесконечно длинным, равномерно заряженным стержнем
- •1.11.2. Поле бесконечно протяженной, однородно заряженной плоскости
- •1.11.3. Поле двух бесконечно протяженных, равномерно заряженных плоскостей
- •1.11.4. Поле заряженной сферической поверхности
- •1.11.5. Поле объёмно заряженного шара
- •Лекция 2. Проводники в электрическом поле
- •2.1. Проводники и их классификация
- •2.2. Электростатическое поле в полости идеального проводника и у его поверхности. Электростатическая защита. Распределение зарядов в объеме проводника и по его поверхности
- •2.3. Электроемкость уединенного проводника и ее физический смысл
- •2.4. Конденсаторы и их емкость
- •2.4.1. Емкость плоского конденсатора
- •2.4.2. Емкость цилиндрического конденсатора
- •2.4.3. Емкость сферического конденсатора
- •2.5. Соединения конденсаторов
- •2.5.1. Последовательное соединение конденсаторов
- •2.5.2. Параллельное и смешанное соединения конденсаторов
- •2.6. Классификация конденсаторов
- •Лекция 3. Статическое электрическое поле в веществе
- •3.1. Диэлектрики. Полярные и неполярные молекулы. Диполь в однородном и неоднородном электрических полях
- •3.1.1. Диполь в однородном электрическом поле
- •3.1.2. Диполь в неоднородном внешнем электрическом поле
- •3.2. Свободные и связанные (поляризационные) заряды в диэлектриках. Поляризация диэлектриков. Вектор поляризации (поляризованность)
- •3.4. Условия на границе раздела двух диэлектриков
- •3.5. Электрострикция. Пьезоэлектрический эффект. Сегнетоэлектрики, их свойства и применение. Электрокалорический эффект
- •3.6. Основные уравнения электростатики диэлектриков
- •Лекция 4. Энергия электрического поля
- •4.1. Энергия взаимодействия электрических зарядов
- •4.2. Энергия заряженных проводников, диполя во внешнем электрическом поле, диэлектрического тела во внешнем электрическом поле, заряженного конденсатора
- •4.3. Энергия электрического поля. Объемная плотность энергии электрического поля
- •4.4. Силы, действующие на макроскопические заряженные тела, помещенные в электрическое поле
- •Лекция 5. Постоянный электрический ток
- •5.1. Постоянный электрический ток. Основные действия и условия существования постоянного тока
- •5.2. Основные характеристики постоянного электрического тока: величина /сила/ тока, плотность тока. Сторонние силы
- •5.3. Электродвижущая сила (эдс), напряжение и разность потенциалов. Их физический смысл. Связь между эдс, напряжением и разностью потенциалов
- •Лекция 6. Классическая электронная теория проводимости металлов. Законы постоянного тока
- •6.1. Классическая электронная теория электропроводности металлов и ее опытные обоснования. Закон Ома в дифференциальной и интегральной формах
- •6.2. Электрическое сопротивление проводников. Изменение сопротивления проводников от температуры и давления. Сверхпроводимость
- •6.3. Соединения сопротивлений: последовательное, параллельное, смешанное. Шунтирование электроизмерительных приборов. Добавочные сопротивления к электроизмерительным приборам
- •6.3.1. Последовательное соединение сопротивлений
- •6.3.2. Параллельное соединение сопротивлений
- •6.3.3. Шунтирование электроизмерительных приборов. Добавочные сопротивления к электроизмерительным приборам
- •6.4. Правила (законы) Кирхгофа и их применение к расчету простейших электрических цепей
- •6.5. Закон Джоуля-Ленца в дифференциальной и интегральной формах
- •6.6. Энергия, выделяющаяся в цепи постоянного тока. Коэффициент полезного действия (кпд) источника постоянного тока
- •Лекция 7. Электрический ток в вакууме, газах и жидкостях
- •7.1. Электрический ток в вакууме. Термоэлектронная эмиссия
- •7.2. Вторичная и автоэлектронная эмиссия
- •7.3. Электрический ток в газе. Процессы ионизации и рекомбинации
- •7.3.1. Несамостоятельная и самостоятельная проводимость газов
- •7.3.2. Закон Пашена
- •7.3.3. Виды разрядов в газах
- •7.3.3.1. Тлеющий разряд
- •7.3.3.2. Искровой разряд
- •7.3.3.3. Коронный разряд
- •7.3.3.4. Дуговой разряд
- •7.4. Понятие о плазме. Плазменная частота. Дебаевская длина. Электропроводность плазмы
- •7.5. Электролиты. Электролиз. Законы электролиза
- •7.6. Электрохимические потенциалы
- •7.7. Электрический ток через электролиты. Закон Ома для электролитов
- •7.7.1. Применение электролиза в технике
- •Лекция 8. Электроны в кристаллах
- •8.1. Квантовая теория электропроводности металлов. Уровень Ферми. Элементы зонной теории кристаллов
- •8.2. Явление сверхпроводимости с точки зрения теории Ферми-Дирака
- •8.3. Электропроводность полупроводников. Понятие о дырочной проводимости. Собственные и примесные полупроводники. Понятие о p-n – переходе
- •8.3.1. Собственная проводимость полупроводников
- •8.3.2. Примесные полупроводники
- •8.4. Электромагнитные явления на границе раздела сред
- •8.4.2. Фотопроводимость полупроводников
- •8.4.3. Люминесценция вещества
- •8.4.4. Термоэлектрические явления. Закон Вольта
- •8.4.5. Эффект Пельтье
- •8.4.6. Явление Зеебека
- •8.4.7. Явление Томсона
- •Заключение
- •Библиографический список Основной
- •Дополнительный
7.5. Электролиты. Электролиз. Законы электролиза
Электролиты – это жидкие или твердые вещества и системы, в которых присутствуют в заметной концентрации ионы, обусловливающие прохождение по ним электрического тока (ионную проводимость).
Надо отметить, что в общем случае электролитами являются не только растворы кислот, солей и щелочей, но и ряд химических соединений как в жидком, так и в твердом состоянии. Примером твердого электролита может служить стекло, которое по своей физической природе является сильно переохлажденной жидкостью с очень большой вязкостью.
М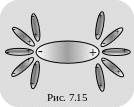 олекулы
электролита и растворителя являются
дипольными. Поэтому в растворе каждую
молекулу электролита окружает группа
молекул растворителя, приблизительно
так как показано на рис. 7.15.
олекулы
электролита и растворителя являются
дипольными. Поэтому в растворе каждую
молекулу электролита окружает группа
молекул растворителя, приблизительно
так как показано на рис. 7.15.
Молекулы растворителя стремятся как бы разорвать молекулу электролита на две части. Этому способствует также тепловое движение – колебание атомов в молекуле электролита. В результате большинство молекул электролита распадается на положительные ионы (катионы) и отрицательные ионы (анионы).
Процесс распада веществ в растворе под влиянием электрического поля на отдельные положительно и отрицательно заряженные ионы называется электролитической диссоциацией.
О братному
процессу – воссоединению (рекомбинации)
ионов электролита в нейтральные молекулы
– препятствует образующаяся на ионах
сольватная оболочка, состоящая из
молекул растворителя (рис. 7.16).
братному
процессу – воссоединению (рекомбинации)
ионов электролита в нейтральные молекулы
– препятствует образующаяся на ионах
сольватная оболочка, состоящая из
молекул растворителя (рис. 7.16).
По способности к электролитической диссоциации электролиты условно делятся на сильные ( ~ 1) и слабые ( близка к нулю).
К сильным электролитам относятся соли, некоторые органические кислоты и основания, к слабым – органические кислоты и основания.
Степень диссоциации зависит от природы растворителя, температуры, давления и других факторов.
Совокупность электрохимических процессов, проходящих на электродах, погруженных в электролит, при прохождении по нему электрического тока, называется электролизом.
Согласно первому закону электролиза (Фарадея), масса m выделившегося на аноде вещества пропорциональна времени t прохождения через электролит тока и силе тока I:
![]() , (7.46)
, (7.46)
где k – коэффициент пропорциональности, называемый электрохимическим эквивалентом данного вещества.
Второй
закон Фарадея устанавливает связь
электрохимического эквивалента с
химическим эквивалентом вещества (![]() ):
):
![]() ,
(7.47)
,
(7.47)
где – молярная (или атомная) масса;
n – заряд иона (в единицах величины заряда электрона e);
F – постоянная Фарадея, численно равная заряду, который должен пройти через электролит, чтобы на электроде выделилась масса вещества, численно равная k.
Заряд
переносят ионы, количество которых в
массе вещества численно равно химическому
эквиваленту
![]() ,
где NA
– число Авогадро (число молекул в
грамм-молекуле). Поэтому
,
где NA
– число Авогадро (число молекул в
грамм-молекуле). Поэтому
![]() ,
(7.48)
,
(7.48)
где qn – заряд одного иона.
Так как заряд иона qn = ne, то F = eNA = 96 500 Кл/моль.
7.6. Электрохимические потенциалы
Если какой-либо металл соприкасается с электролитом, то на металле и в электролите появляются заряды противоположного знака. При этом металл приобретает относительно электролита определенный электрический потенциал, который называют электрохимическим потенциалом. Возникновение электрохимических потенциалов было объяснено Нернстом.
Электрохимический потенциал зависит от рода металла и концентрации электролита. При этом имеет значение только концентрация в растворе ионов самого металла, так как только ионы могут переходить между металлом и раствором. Наличие же других ионов в электролите не оказывает влияния на электрохимический потенциал.
Если концентрацию ионов металла в растворе поддерживать постоянной, то электрохимический потенциал будет зависеть только от рода металла и будет характеризовать его способность насыщать раствор ионами.
Любой гальванический элемент имеет два электрода. ЭДС гальванического элемента (напряжение при разомкнутой цепи) равна разности электрохимических потенциалов его электродов (1 - 2).
Зная электрохимические потенциалы металлов, из которых состоят электроды, можно найти ЭДС химического источника тока.
ЭДС гальванического элемента это – максимальная работа химических реакций, рассчитанная на единицу заряда. Для приближенной оценки предполагается, что максимальная работа равна полной энергии, освобождаемой при химических реакциях. Тогда
![]() ,
(7.49)
,
(7.49)
где p1 и p2 – тепловые эффекты реакций на обоих электродах (рассчитанные на 1 кг вещества электрода);
k1 и k2 – электрохимические эквиваленты вещества электродов.
Тепловые эффекты реакций на обоих электродах p1 и p2 и электрохимические эквиваленты вещества электродов k1 и k2 можно представить в виде
![]() ;
;
![]() ;
;
![]() ;
;
![]() ,
(7.50)
,
(7.50)
где Q1 и Q2 – тепловые эффекты реакций на 1 килограмм-атом;
A1 и A2 – атомные веса материалов электродов;
Z1 и Z2 – валентности;
F – число Фарадея.
Тогда для ЭДС химического источника тока, будем иметь
![]() .
(7.51)
.
(7.51)
Надо отметить, что в гальванических элементах энергия, выделяемая в химических реакциях, непосредственно превращается в энергию электрического тока. Этот процесс обладает большим коэффициентом полезного действия, чем применяемый на обычных электростанциях. Поэтому гальванические элементы (химические источники тока) представляют большой принципиальный интерес.
Однако стоимость электроэнергии, получаемой от гальванических элементов, значительно выше стоимости энергии, вырабатываемой на обычных электростанциях, так как в элементах расходуется не дешевое топливо (например, уголь), а дорогостоящие вещества (например, цинк). В связи с этим химические источники тока (гальванические элементы) применяют только в тех случаях, где требуется небольшая энергия (где стоимость ее не играет роли), но важны портативность и простота источника тока.
При замыкании химического источника тока на внешнюю цепь сила тока в цепи не постоянна, а уменьшается с течением времени.
