
- •1. Общий порядок оформления работ по синтезу органических соединений
- •2. Порядок заполнения таблицы «Расчет синтеза»
- •3. Порядок заполнения таблицы «Сводная таблица результатов синтеза»
- •4. Галогенирование
- •4.1. Бромистый этил (бромэтан)
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция галогенпроизводных
- •Контрольные вопросы
- •4.2. Бромистый бутил (1-бромбутан)
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция галогенпроизводных
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция галогенпроизводных
- •Контрольные вопросы и задания
- •5. Нитрование
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •5.2. Нитрометан
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •6. Сульфирование
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •6.3. Сульфаниловая кислота
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •7. Ацилирование
- •7.1. Ацетанилид
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •7.2. Аспирин (о-ацетоксибензойная кислота)
- •Посуда и приборы
- •Методика синтеза
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •7.4. Этилформиат
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •9. Диазотирование
- •9.1. Фенол
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •9.2. Йодбензол
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •10. Красители
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Контрольные вопросы
- •10.2. Метиловый оранжевый
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •10.3. Малахитовый зеленый
- •Посуда и приборы
- •Химизм получения малахитового зеленого
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •10.4. Фенолфталеин
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •10.5. Флуоресцеин
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •11. Щелочное плавление
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •12. Реакции Канниццаро
- •12.1. Бензойная кислота и бензиловый спирт
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •12.2. Бензиловый спирт
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •13. Окисление
- •13.1. Ацетон
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •Библиографический список
- •Лабораторный практикум по органическому синтезу
- •1 70026, Тверь, наб. Афанасия Никитина, 22
Методика синтеза
Обращаться с изоамилацетатом следует осторожно, так как он легко воспламеняется (температура вспышки 36оС).
В колбу Вюрца (или круглодонную колбу с насадкой Вюрца) емкостью 250 мл (см. рис. 30) помещают 25 г безводного уксусно-кислого натрия, растертого в порошок.
В конической колбе емкостью 100 мл при перемешивании и охлаждении содержимого колбы проточной холодной водой к 25 г изоамилового спирта осторожно (!) добавляют 25 г концентрированной серной кислоты. Полученную смесь переливают через воронку в капельную воронку и приливают по каплям в реакционную колбу, которую непрерывно нагревают на воздушной бане при 150С.
По окончании реакции и прекращении отгонки дистиллята верхний слой дистиллята (смесь уксусно-изоамилового эфира и изоамилового спирта) отделяют в делительной воронке, промывают 10%-ным раствором углекислого натрия, затем два раза водой, высушивают хлористым кальцием и перегоняют из колбы с дефлегматором (см. рис. 31), отбирая фракции до 138оС и при 138–140оС.
Вторая фракция – 138–140оС – уксусно-изоамиловый эфир.
Получают 24 г изоамилацетата.
Синтез можно проводить в трехгорлой колбе, тогда термометр погружают непосредственно в реакционную смесь, температура которой должна быть 120–130оС.
Физические свойства
Изоамилацетат (уксусно-изоамиловый эфир, грушевая эссенция) – бесцветная жидкость с фруктовым запахом; в 100 мл воды при 25оС растворяется 0,16 г; смешивается со спиртом, эфиром, хлороформом:
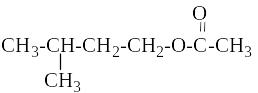
Молярная
масса 130,19; Тпл
= –78,5С;
Ткип
= 142,5С
(чистого изоамилацетата);
![]() = 0,8699;
=
1,4054.
= 0,8699;
=
1,4054.
Применяется как растворитель нитроцеллюлозы, а также в пищевой промышленности под названием грушевой эссенции. Кроме того, используется как растворитель в аналитической химии. Наркотически действует на организм, раздражает слизистые оболочки глаз, носа и дыхательных путей.
Отличительная реакция
В пробирку помещают 2–3 мл изоамилацетата, 3 мл 1%-ного раствора хлорного железа в 10н соляной кислоте. После сильного встряхивания пробирки происходит расслаивание. Верхний слой эфира окрашен в яркий буро-желтый цвет вследствие перехода в него почти всей соли железа. Нижний слой окрашен лишь в бледно-желтоватый цвет.
Контрольные вопросы
1. Написать уравнения реакции: а) спирта с серной кислотой, б) уксусно-кислого натрия с серной кислотой, в) спирта с полученным в предыдущей реакции веществом, механизм реакции, г) суммарное уравнение реакции, д) внутри- и межмолекулярной дегидратации спирта в присутствии серной кислоты (по стадиям) [1–11].
2. Учитывая агрегатное состояние каждого вещества (исходного, побочного и основного продукта), перечислить, из каких веществ состоит реакционная смесь, если реакция прошла примерно на 90%? Написать реакцию всех этих веществ с углекислым натрием.
3. При промывке карбонатом натрия учесть растворимость эфира в воде при комнатной температуре.
7.4. Этилформиат
Сведения о веществах, принимающих участие в реакции синтеза этилформиата, и вспомогательных материалах, представлены в табл. 15.
Таблица 15. Вещества, принимающие участие в реакции синтеза этилформиата, и вспомогательные материалы
Реактив |
Плотность, г/см3 |
Концентрация, % |
Количество |
|
г |
мл |
|||
Этанол |
0,812 |
96,0 (об.) |
– |
27,0 |
Муравьиная кислота |
1,220 |
86,5 |
24,8 |
рассчитать |
Кальций хлористый (безводный) |
– |
96,5 |
5,0 |
– |
Карбонат натрия |
– |
99,5 |
3,0 |
– |
Дистиллированная вода |
– |
– |
– |
– |
Примечание. Перед началом синтеза уточнить концентрации имеющихся в лаборатории реактивов.
