
- •Рецензенты:
- •Содержание
- •Введение
- •1. Основные этапы выполнения курсовой работы и порядок предоставления материалов к защите
- •2. Структура курсовой работы
- •3. Содержание введения
- •4. Содержание экспериментальной части
- •4.1. Спектральные методы исследования
- •Люминесцентный анализ
- •4.2. Хроматографическое исследование
- •5. Оформление пояснительной записки курсовой работы
- •5.1. Порядок представления текстового, табличного и иллюстративного материала
- •5.2. Оформление библиографического аппарата
- •5.3. Оформление приложений
- •Рекомендуемая литература Основная:
- •Дополнительная:
- •Нормативные документы
- •Приложение 1
- •Приложение 2
- •Санкт-Петербург
- •Приложение 3 Характеристические полосы поглощения различных функциональных группировок Алканы
- •Ароматические углеводороды
- •Форма полос в области 1600-2000 см-1 и полосы неплоских деформационных колебаний (900-700 см-1)
- •Хлорсодержащие соединения
- •Карбонильные и простые эфирные группы
- •Лист регистрации изменений
4. Содержание экспериментальной части
Данная часть курсовой работы состоит из двух подразделов, каждый из которых выполняется в течение семестра по мере изучения дисциплины «Физико-химические методы экспертного исследования».
4.1. Спектральные методы исследования
В соответствии с тематическим планом по дисциплине «Физико-химические методы экспертного исследования» последовательно изучаются следующие спектральные методы исследования:
ИК-спектроскопия
Люминесцентная спектроскопия
При изучении соответствующих тем проводятся лабораторные работы, в процессе которых обучаемые проводят экспериментальную часть курсовой работы.
Каждый из применяемых методов исследования оформляется в виде отдельного подраздела, содержащего краткое описание метода, характеристики применяемого лабораторного оборудования, условия проведения эксперимента, полученные спектры и их обработку, представляются полученные результаты качественного и количественного анализа и краткие выводы по подразделу.
ИК-спектроскопия
Возбуждения атомов и атомных групп, составляющих молекулу, может вызвать их колебания. Колебательная энергия молекул дискретна (квантована). Спектры, соответствующие колебательным переходам, наблюдаются в инфракрасной (ИК) области (1013 – 1014 Гц ≈ 102 - 5∙103 см-1).
Колебательные спектры обладают высокой специфичностью и широко используются для идентификации веществ. Каждому веществу присущ свойственный только ему набор полос и не существует двух веществ, которые имели бы одинаковые колебательные спектры. В настоящее время имеются атласы ИК-спектров для различных классов органических, элементоорганических и неорганических веществ, в которых указаны условия подготовки образцов и регистрации спектров, а также модели спектрометров.
ИК-спектроскопия нашла широкое применение в различных сферах пожарно-технической и криминалистической экспертизы.
Колебательные спектры обладают высокой специфичностью и широко используются для идентификации веществ. Каждому веществу присущ свойственный только ему набор полос и не существует двух веществ, которые имели бы одинаковые колебательные спектры. В настоящее время имеются атласы ИК-спектров для различных классов органических, элементоорганических и неорганических веществ, в которых указаны условия подготовки образцов и регистрации спектров, а также модели спектрометров.
Идентификация неизвестного вещества по ИК-спектру заключается в сопоставлении спектра исследуемого вещества с эталонным спектром, приведенным в атласе. Учитывая, что колебательные спектры, зарегистрированные на различных спектрометрах или в различных условиях, могут отличаться между собой, важнейшим условием сравнения спектров является стандартизация условий их регистрации.
Совпадение спектральной кривой исследуемого вещества со спектральной кривой эталона свидетельствует об идентичности двух веществ. Отсутствие в спектре исследуемого вещества полос, наблюдаемых в спектре образца сравнения, однозначно указывает на то, что эти вещества различны. Присутствие в спектре исследуемого вещества большего числа полос по сравнению со спектром эталона может быть объяснено как загрязнением исследуемого вещества, так и различием обоих веществ.
При идентификации молекул органических веществ особое внимание уделяют области спектра 1300 – 600 см-1. В эту область попадают полосы, отвечающие колебаниям связей C–C, C–N, C=O, а также многие деформационные колебания. В результате сильного взаимодействия этих колебаний отнесение полос к отдельным связям невозможно, однако весь набор полос в этой области спектра является характеристикой ядерного состава (скелета) молекулы в целом. Эту область называют областью отпечатков пальцев (фингерпринтов). По колебательным спектрам в этой области можно идентифицировать даже изомеры.
Колебательную спектроскопию используют также для количественного определения органических веществ. Определение одного вещества методом ИК-спектроскопии базируется на основном законе светопоглощения, а анализ смесей веществ использует, кроме того, закон аддитивности оптических плотностей. Пределы обнаружения веществ методом ИК-спектроскопии достаточно высоки.
С помощью колебательных спектров можно проводить качественный анализ смесей веществ неизвестного или частично известного состава. Анализ с помощью ИКС требует малого количества вещества. Анализ инфракрасных спектров поглощения позволяет выявить функциональный состав веществ в исследуемой пробе. Принадлежность частот поглощения к тем или иным группам атомов или связей устанавливают с помощью таблиц характеристических частот.
В ряде случаев можно выделить такие колебания, при которых изменяются преимущественно длины связей или углы между связями. Тогда первое колебание называют валентным, а второе – деформационным (рисунок 1).
ИК-спектры измеряют для газообразных, жидких и твердых соединений, а также их растворов в различных растворителях.
В наиболее высокочастотной области располагаются колебания групп Х–Н. Увеличение массы присоединенного к углероду атома приводит к появлению полос поглощения в более низкочастотной области. Так, частоты колебаний С–Н-группы находятся около 3000 см–1, колебания С–С в области 1100–900 см–1, а С–Br – около 600 см–1. Увеличение кратности связи вызывает повышение частот.
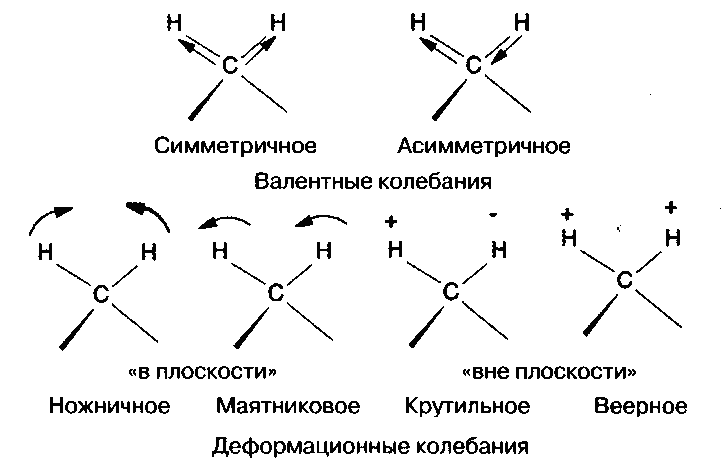 Рис.
1. Валентные и деформационные колебания
метиленовой группы
Рис.
1. Валентные и деформационные колебания
метиленовой группы
Типичный ИК-спектр, такой, как спектр н-гексана CH3(CH2)4CH3 (рисунок 2), проявляется в виде серии полос поглощения различной формы и интенсивности. Почти все органические соединения обнаруживают пик или группу пиков близ 3000 см–1. Поглощение в этой области обусловлено валентными колебаниями С-Н. Поглощение в области 1460, 1380 и 725 см-1 обусловлено различными деформационными колебаниями С–Н-связей.
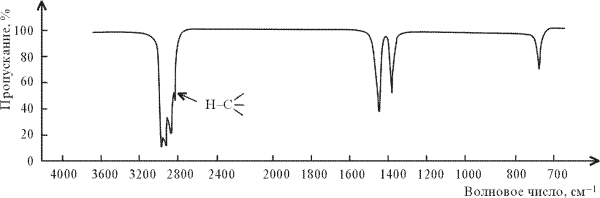 Рис.
2. ИК-спектр н-гексана СН3(СН2)4СН3
Рис.
2. ИК-спектр н-гексана СН3(СН2)4СН3
Для иллюстрации влияния строения молекулы на ИК-спектр можно сравнить спектры н-гексана и гексена-1 (рисунок 3). Они весьма отличаются один от другого.
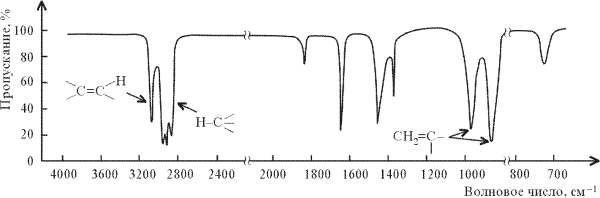 Рис.
3. ИК-спектр гексена-1 СН2=СН(CH2)3СН3
Рис.
3. ИК-спектр гексена-1 СН2=СН(CH2)3СН3
В районе валентных колебаний С–Н гексена-1 наблюдается пик при 3095 см–1, тогда как все колебания С–Н гексана проявляются ниже 3000 см–1. Пик поглощения выше 3000 см–1 обусловлен атомами водорода при sp2-гибридизованном атоме углерода. ИК-спектр гексена-1 содержит также полосу поглощения при 1640 см–1, связанную с валентными колебаниями кратной связи С=С. Пики около 1000 и 900 см–1 в спектре гексена-1, отсутствующие в спектре гексана, относятся к деформационным колебаниям атомов водорода при двойной связи С=С.
Кроме валентных колебаний sp2 С–Н-групп известны другие группировки, проявляющиеся при частотах выше 3000 см–1. Наиболее важная из них это О–Н-группа спиртов. На рисунке 4 представлен ИК-спектр гексанола-2.
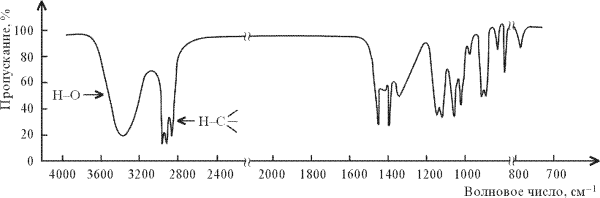 Рис.
4. ИК-спектр гексанола-2 СН3(CH2)3СН(ОН)СН3
Рис.
4. ИК-спектр гексанола-2 СН3(CH2)3СН(ОН)СН3
Спектр содержит широкий сигнал при 3300 см–1, приписываемый валентным колебаниям О–Н-групп спиртов, связанных межмолекулярной водородной связью. В разбавленных растворах спиртов в инертном растворителе (хлороформе CHCl3, четыреххлористом углероде ССl4), где водородное связывание типа
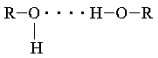
|уменьшается, наряду с полимолекулярными ассоциатами (ROH)n присутствуют индивидуальные спиртовые молекулы ROH. В этом случае проявляется дополнительный пик приблизительно при 3600 см–1.
Карбонильная группа принадлежит к наиболее легко различимым структурным фрагментам молекул, обнаруживаемым методом ИК-cпектроскопии. Валентные колебания двойной связи C=O проявляются интенсивным сигналом в интервале 1800–1650 см–1. Этот пик ярко выражен в спектре гексанона-2, приведенном на рисунке 5.
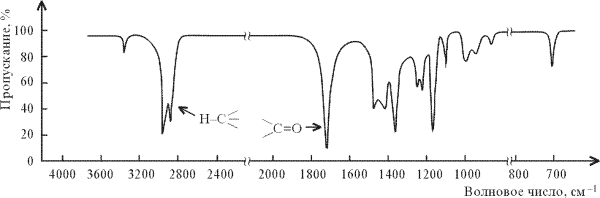 Рис.
5. ИК-спектр гексанона-2 СН3(CH2)3С(О)СН3
Рис.
5. ИК-спектр гексанона-2 СН3(CH2)3С(О)СН3
Положение карбонильной полосы поглощения в спектре зависит от природы заместителей при карбонильной группе C=O.
Ароматическое кольцо проявляется в ИК-спектре умеренным пиком валентных колебаний С–Н в районе 3030см–1. Другая характерная особенность – валентные колебания ароматических углерод-углеродных связей наблюдаются обычно при 1600 и 1475 см–1. Наконец, ароматическое кольцо обнаруживает интенсивное поглощение в диапазоне 800–690 см–1, обусловленное деформационными колебаниями С–Н. Все эти особенности ароматического кольца наблюдаются в ИК-спектре толуола (рисунок 6).
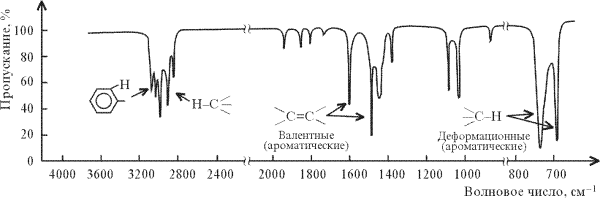 Рис.
6. ИК-спектр толуола
Рис.
6. ИК-спектр толуола
![]()
Инфракрасный Фурье-спектрометр «ИнфраЛЮМ ФТ-02», применяемый при выполнении курсовой работы, предназначен для регистрации спектров поглощения или пропускания жидких, твердых и газообразных веществ в средней инфракрасной области, т.е. в диапазоне 400 ...7500 см-1.
При использовании специальных приставок спектрометр может быть использован для регистрации спектров диффузного и зеркального отражения, нарушенного полного внутреннего отражения и спектров поверхностного поглощения в инфракрасной области.
Основой оптического блока Фурье-спектрометра является оригинальный кольцевой интерферометр, в котором при движении светоделителя происходит изменение разности хода между интерферирующими лучами. Прибор непосредственно регистрирует световой поток на выходе интерферометра в зависимости от разности хода (интерферограмму). Управление процессом измерения осуществляется от внутреннего контроллера и компьютера. Оптический спектр (в шкале волновых чисел) получается после обратного преобразования Фурье зарегистрированной интерферограммы в связанном с прибором персональным компьютере.
Области применения данного ИК-спектрометра:
экологический контроль воздушной и водной среды,
контроль производственных процессов в химической, нефтехимической, фармацевтической и пищевой промышленности,
минералогия,
геохимия,
криминалистика,
научные исследования.
Для анализа на инфракрасном Фурье-спектрометре «ИнфраЛЮМ ФТ-02» жидкостей используются сборные кюветы позволяющие варьировать толщину от 0,01 до 1 мм. Заполнение осуществляется стеклянным шприцем объемом 2 мл через два специальных отверстия, расположенных на металлическом корпусе кюветы. При наполнении кювета держится так, чтобы отверстия были установлены друг над другом. Конус шприца вставляется в нижний патрубок и легким нажимом на поршень шприца кювета медленно наполняется. После этого верхнее отверстие закрывается пробкой. Затем шприц вынимается, и нижнее отверстие тоже закрывается. При этом кюветы малой толщины заполняются без нажатия на поршень шприца за счет действия капиллярных сил.
При регистрации спектров поглощения чистых жидкостей используются кюветы с очень тонкими поглощающими слоями, при выполнении курсовой работы применяется кювета толщиной 0,02 мм.
Анализ на Инфракрасном Фурье-спектрометре осуществляется под контролем преподавателя в соответствии с руководством по эксплуатации прибора при следующем режиме измерения.
Границы диапазона
Верхняя 400 см-1
Нижняя 4000 см-1
Разрешение 4 см-1
Время накопления 60.00 с
Количество сканов 40.
Полученные спектры распечатываются на принтере и анализируются.
На полученных спектрах отмечаются характеристические полосы поглощения, по ним, в соответствии с данными, приведенными в таблицах характеристических частот (приложение 3), определяются функциональные группы, имеющиеся в изучаемых образцах. На основании полученных данных делается вывод о функциональном составе образца.
Для большей наглядности полученных данных все результаты рекомендуется записывать в форме таблицы 1.
Таблица 1 Результаты спектрального анализа
Волновое число, см-1 |
Интенсивность аналитической линии |
Колебания |
|
|
|
