Определение жесткости воды
Было первым
практически важным применением ЭДТА.
Жесткость воды характеризуется молярной
концентрацией эквивалентов кальция и
магния (f-
1/2) и выражается в моль/л Содержание
этих элементов определяют прямым
титрованием пробы воды в аммонийном
буфере в присутствии индикатора эриохром
черный
Тяжелые металлы
предварительно осаждают в виде сульфидов
или маскируют цианидами. Жесткость ,
обусловленную солями кальция можно
определить титрованием с мурексидом в
щелочной среде и далее по разщности
рассчитать жесткость связанную с
присутствием солей магния.
Комплексонометрический метод позволяет
определять жэти соли в морской воде.
Т. Расчет ведут по
формуле
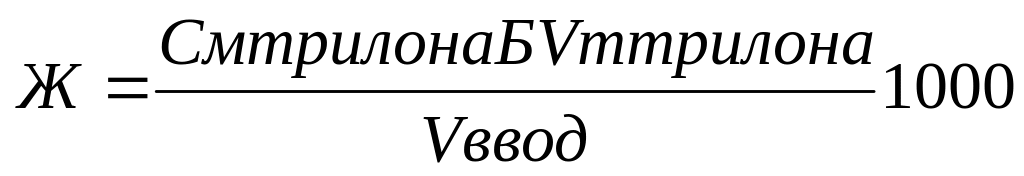
Обратное титрование соли алюминия по гф
Навеску препарата,
содержащую 0,02-0,035 г Аl
растворить в 2 мл HCl
(1м/л) добавить 50 мл воды, 50 мл 0,05 м раствора
трилона Б, раствор нейтрализовать NaOH
по метиловому красному нагреть, охладить,
внести индикатор ксиленовый оранжевый,
5 г ГМТА. Избыток трилона оттитровывают
раствором нитрата свинца до
розового-фиолетового окрашивания.
Общая оценка
метода.
Среди
комплексометрических методов наибольшее
значение имеют методы комплексонометрические
Устойчивые
координационные комплексы образуют
практически все катионы (исключая
щелочные)
Рабочие растворы
устойчивы и готовятся по точной навеске.
Имеется широкий
выбор индикаторов, позволяющих вести
титрование при различных рян, Т.Э можно
фиксировать фотометрическими и
электрохимическими методами (автоматизация
процесса)
Точность метода
0,2-0,3%
Метод совершенствуется:
новые индикаторы, новые титранты-комплексоны,
новые области применения.

