- •Методические указания
- •Содержание
- •1 Техника безопасного проведения работ химической лаборатории
- •2 Очистка и подготовка химической посуды
- •3 Техника выполнения основных операций
- •4 Общие указания к работе в лаборатории
- •5 Неорганическая химия (Качественный анализ)
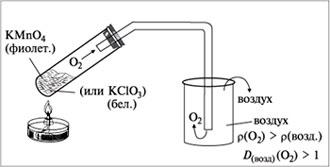
- •Получение и собирание кислорода
- •5.2 Скорость химических реакций. Химическое равновесие
- •5.3 Электролитическая диссоциация
- •5.4 Произведение растворимости
- •5.5 Гидролиз солей
- •5.6 Карбонаты. Жесткость воды
- •5.7 Окислительно-восстановительные реакции
- •5.8 Комплексные соединения
- •5.9 Коррозия металлов
- •6. Аналитическая химия (Количественный анализ)
- •6.1 Определение металлов в растворе комплексонометрическим методом
- •6.3 Определение содержания щавелевой кислоты в растворе перманганатометрическим методом
- •6.6 Определение содержания кислот в растворе методом нейтрализации
- •7.2 Лабораторная работа №2
- •7.3 Лабораторная работа №3
- •8 Размерность
- •9.1 Расчеты массы навески вещества
- •9.2 Щелочи
- •9.3 Кислоты
- •Растворение серной кислоты в воде
- •9.4 Органические вещества
- •9.5 Различные смеси
- •10 Индикаторы
- •11 Демонстрационные опыты Синергетика – теория самоорганизации
- •11.1 «Жук бомбардир»
- •11.2 Реакция Бриггса-Раушера «Йодные часы»
- •11.3 Твёрдофазная колебательная реакция:
- •11.4 Реакция Белоусова-Жаботинского «Химический маятник»
- •11.5 «Фейерверк в жидкости»
- •11.6 Красные призмы.
- •11.7 «Живые капли ртути»
- •11.8 Получение оксалата железа.
- •11.9 "Замерзание" воды при комнатной температуре
- •11.10 Получение оксида хрома (III)
- •11.11 Реакция «Серебряного зеркала»
- •12 Регенерация химических остатков
- •12.1 Регенерация остатков серебра в нитрат серебра
- •12.2 Регенерация остатков серебра в гранулы
- •13 Упаковка и хранение токсичных веществ
- •Список некоторых веществ
- •14 Кристаллография
- •14.1 Кристаллы металлической меди
- •Подсказка
4 Общие указания к работе в лаборатории
Непременным условием успешной работы в химической лаборатории является серьезное, внимательное отношение к работе, тщательное выполнение всех операций анализа, точное соблюдение условий выполнения химических реакций.
При выполнении всех видов работы следует всегда обращать внимание на чистоту рабочего места, а также склянок, в которых хранятся реактивы. Пролитый раствор следует немедленно вытереть тряпкой, промыть водой и снова тряпкой. Необходимо сохранять один и тот же порядок размещения реактивов в лаборатории. Для того чтобы использовать реагент, необходимо взять сосуд с ним в руку, пипеткой отобрать необходимое количество реактива, а затем вернуть ее на свое место. Не следует касаться стенок пробирки, в которой выполняется реакция, пипеткой для отбора реагента. Каждой склянке с реактивом должна соответствовать отдельная пипетка. Следует строго следить, чтобы пипетка из одной склянки не попадала в другую. Со временем склянки покрываются налетом солей. Необходимо время от времени протирать их мягкой тряпкой. Некоторые реагенты разлагаются при хранении, поэтому их заменяют свежеприготовленными.
К работе следует приступать только после тщательного ознакомления с ее
содержанием, методикой выполнения, подготовки рабочего места.
Работу в лаборатории нужно организовать так, чтобы во время длительных операций одновременно выполнять другую работу. Например, в то время, когда производится нагревание растворов, можно проводить исследование по обнаружению отдельных ионов или оформлять записи в лабораторном журнале.
С ядовитыми и дурно пахнущими газами нужно работать под тягой!!!
Все результаты и наблюдения сразу же записываются в лабораторный журнал. Нельзя делать записи на листочках.
При выполнении контрольных задач каждый ион должен быть открыт с помощью нескольких реакций. Результаты анализа сдают преподавателю, только убедившись в их достоверности.
5 Неорганическая химия (Качественный анализ)
5.0 Получение различных газов в лабораторных условиях
5.01 Получение кислорода
1. Нагревание нитратов КNO3, NaNO3.
2KNO3 =(нагрев.) 2KNO2 + O2↑
2. Нагревание перманганат калия
2KMnO4 =(нагрев.) K2MnO4 + MnO2+ O2↑
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании:
5KMnO4=(нагрев.) K2MnO4 +K3MnO4 + 3MnO2+ 3O2↑
3. Разложение пергидроли водорода
2Н2О2 =(нагрев.) 2Н2О + О2↑
В перекись надо добавить катализатор, любую соль железа, даже нагрев не потребуется (осторожно, возможно сильное "вскипание" раствора)
4. Нагревание бертолетовой соли. Может произойти взрыв, если бертолетова соль и/или посуда грязная, особенно со следами органики или любых восстановителей.
2KClO3= (нагрев) 2KCl + 3O2↑
5.02 Получение водорода
1. Реакция алюминия и щелочи
На дно колбы насыпают щелочи, бросают несколько кусочков алюминия и добавляют немного воды. Колбу закрывают пробкой с газоотводной трубкой.
После того, как водород полностью вытеснит из колбы весь воздух его можно поджечь. Водород горит бесцветным, почти незаметным пламенем, но брызги едкого натра придают пламени желтый цвет. Водород можно собрать в различные сосуды путем вытеснения воздуха.
2. Аппарат Киппа. В этом приборе можно получать водород из цинка и соляной кислоты, сероводород из сернистого железа, углекислый газ из мрамора. В позиции, а прибор находится в рабочем состоянии, кран открыт. Крепкий раствор соляной кислоты устремляется в нижнюю часть прибора, заполняет его и смачивает металлический цинк, лежащий на медной сетке. Цинк растворяется в кислоте, реагирует с ней, образующийся водород устремляется в среднюю сферу прибора, вытесняет воздух, смешиваясь с ним. Поэтому выходящий газ надо проверить на чистоту. Распределение физических сил в приборе показано на рисунке при помощи стрелок.
|
|
|
Работа аппарата Киппа: а – начало работы; б – остановка |
Закрываем кран. Водород продолжает образовываться, его количество увеличивается. Поскольку выход газу перекрыт, внутри сферы увеличивается давление. Оно и выдавливает кислоту из средней сферы до тех пор, пока кислота перестанет покрывать поверхность цинка. Химическая реакция прекращается (смоченный кислотой цинк продолжает некоторое время реагировать с ней). Внутреннее давление в приборе, создаваемое водородом, и давление, создаваемое гидравлическим затвором, уравновешиваются.