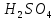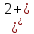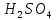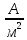- •Материальный баланс ванны электроэкстракции никеля пояснительная записка курсовая работа
- •1.Электродные процессы и режим электролиза
- •2. Составы электролитов для электроэкстракции никеля
- •2.1 Электролиты электроэкстракции никеля
- •2.2Сульфатный электролит
- •2.3 Хлоридный электролит
- •2.4 Аммонийный электролит
- •2.5 Выбор электролита
- •3.Расчет материального баланса ванны электроэкстракции
- •3.1 Исходные данные для расчета материального баланса и нахождение параметров ванны. Расчет материального баланса
- •3.2 Расчет коэффициентов в уравнении, определяющем плотность электролита как функцию состава
- •3.3 Расчет плотности поступающего электролита
- •3.4 Расчет интенсивностей источников вещества за счет электродных реакций
- •3.5 Расчет интенсивностей источников вещества за счет перехода его из одного агрегатного состояния в другое
- •3.6 Расчет суммарных источников вещества в катодной и анодной зонах
- •3.8 Расчет материального баланса изменения состава электролита во времени
3.1 Исходные данные для расчета материального баланса и нахождение параметров ванны. Расчет материального баланса
Таблица 2 – Состав электролита на входе в ванну, г/л
|
Ионы
никеля |
130 |
|
Серная
кислота
|
2,66 |
Таблица 3 – Состав электролита на выходе из ванны, г/л
|
Ионы
никеля |
100 |
|
Серная
кислота
|
0.574 |
Таблица 4 - Параметры технологического процесса
|
Температура электролита, °С |
65 |
|
Плотность
тока,
|
300 |
|
Катодный выход по току, % |
96 |
|
pH |
2,5 |
|
Длина ванны, мм |
6010 |
|
Ширина ванны, мм |
1160 |
|
Высота ванны, мм |
1390 |
|
Объем ванны, м3 |
9,691 |
Таблица 5 – Параметры катодов
|
Высота катода, мм |
1020 |
|
Ширина катода, мм |
1020 |
|
Толщина катода, мм |
30 |
|
Количество катодов, шт |
2 |
|
Расстояние между катодами, мм |
110 |
Таблица 6 – Параметры анодов
|
Высота анода, мм |
1000 |
|
Ширина катода, мм |
1000 |
|
Толщина анода, мм |
10 |
|
Количество анодов, шт |
1 |
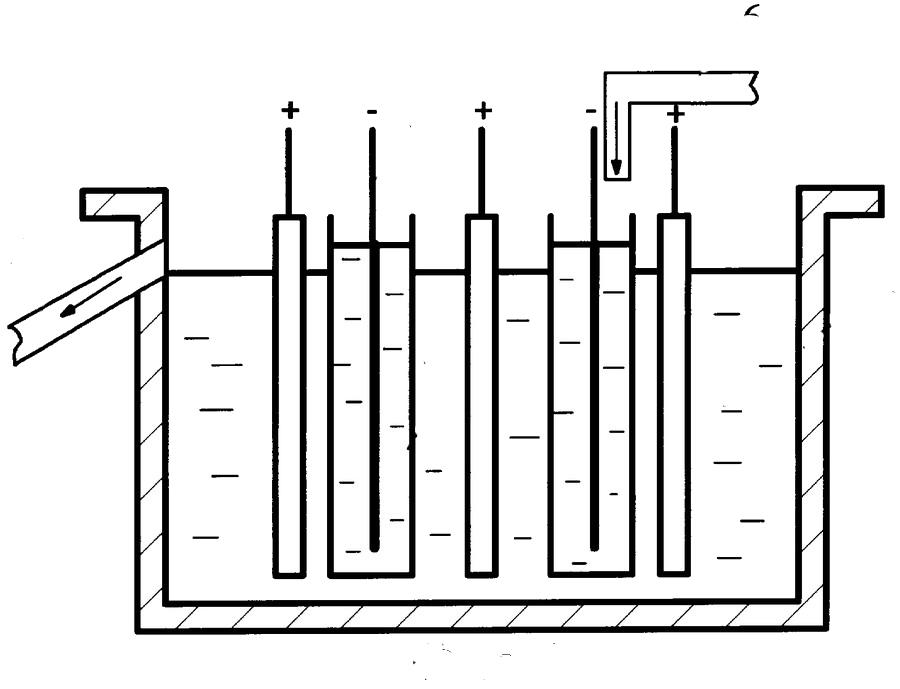
Рисунок 1 – Ванна электроэкстракции никеля
Электролизная ванна представляет собой железобетонную конструкцию с внутренней футеровкой из ПВХ.
Расчет концентрации соли NiSO4 по ионным концентрациям:
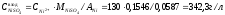
Расчет площади стороны катода:
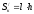 ,
,
где
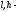 ширина и высота катода соответственно,
м.
ширина и высота катода соответственно,
м.
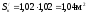
Общая формула для расчета площади одного электрода:
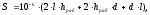
где
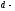 толщина
электродов соответственно, м.
толщина
электродов соответственно, м.
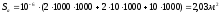
Расчет токовой нагрузки ячейки:
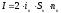
где
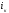 - катодная плотность тока, А/м2
- катодная плотность тока, А/м2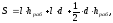
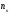 - число катодов,
шт.
- число катодов,
шт.
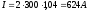
Общая формула для расчета объема погруженной части электрода:
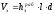
где
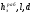 -
рабочая высота, ширина и толщина
электрода, м.
-
рабочая высота, ширина и толщина
электрода, м.

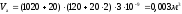
Расчет объема электролита катодной области:
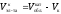
где
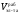 -
рабочий объем ванны, м3
-
рабочий объем ванны, м3
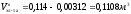
Расчет объема электролита анодной области:
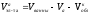
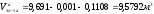
Расчет катодного зеркала электролита:
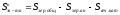
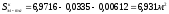
Расчет анодного зеркала электролита:
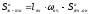
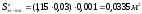
3.2 Расчет коэффициентов в уравнении, определяющем плотность электролита как функцию состава
Плотность раствора линейно и аддитивно зависит от состава раствора. Вначале необходимо найти коэффициент bi, учитывающий влияние отдельного компонента на плотность раствора. Для этого воспользуемся справочными данными [7] зависимости плотности раствора отдельных компонентов от их концентрации для сульфата никеля (таблица 2) и для серной кислоты (таблица 3).
Таблица 2 – Зависимость плотности раствора сульфата никеля от концентрации при температуре 200С [7]
|
c, г/л |
10,09 |
20,4 |
41,68 |
63,78 |
86,8 |
110,9 |
135,96 |
162,1 |
189,4 |
217,6 |
|
ρ(20), г/л |
1009 |
1020 |
1042 |
1063 |
1085 |
1109 |
1133 |
1158 |
1184 |
1209 |
|
ρ-1000, г/л |
9 |
20 |
42 |
63 |
85 |
109 |
133 |
158 |
184 |
209 |
Таблица 3 – Зависимость плотности растворов серной кислоты от концентрации при температуре 200С [7]
|
c, г/л |
9,96 |
17,49 |
25,45 |
33,07 |
41,99 |
48,87 |
56,85 |
64,86 |
72,69 |
80,92 |
88,8 |
|
ρ(20), г/л |
1005 |
1010 |
1015 |
1020 |
1025 |
1030 |
1035 |
1040 |
1045 |
1050 |
1055 |
|
ρ-1000, г/л |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
45 |
50 |
55 |
По данным таблиц строим графики зависимости плотности вещества без учета растворителя от их концентрации для сульфата никеля (рисунок 4) и для серной кислоты (рисунок 5)
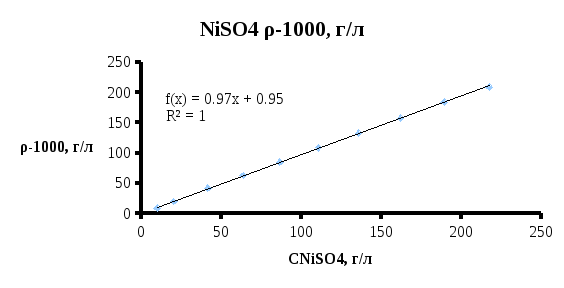
Рисунок 4 – Зависимость плотности сульфата никеля от концентрации
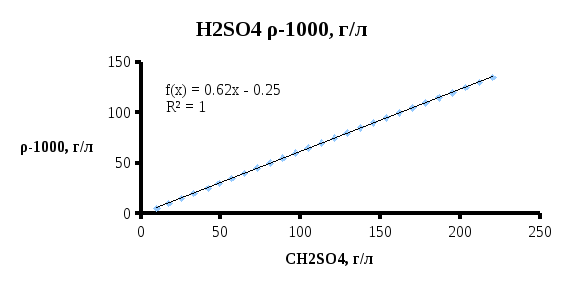
Рисунок 5 – Зависимость плотности серной кислоты от концентрации
Из графиков находим поправочные коэффициенты для сульфата никеля и серной кислоты, представленные в таблице 4.
Таблица 4 – Поправочные коэффициенты компонентов
|
Компонент |
b |
|
NiSO4 |
0,965 |
|
H2SO4 |
0,617 |