
- •Материальный баланс ванны электроэкстракции никеля пояснительная записка курсовая работа
- •1.Электродные процессы и режим электролиза
- •2. Составы электролитов для электроэкстракции никеля
- •2.1 Электролиты электроэкстракции никеля
- •2.2Сульфатный электролит
- •2.3 Хлоридный электролит
- •2.4 Аммонийный электролит
- •2.5 Выбор электролита
- •3.Расчет материального баланса ванны электроэкстракции
- •3.1 Исходные данные для расчета материального баланса и нахождение параметров ванны. Расчет материального баланса
- •3.2 Расчет коэффициентов в уравнении, определяющем плотность электролита как функцию состава
- •3.3 Расчет плотности поступающего электролита
- •3.4 Расчет интенсивностей источников вещества за счет электродных реакций
- •3.5 Расчет интенсивностей источников вещества за счет перехода его из одного агрегатного состояния в другое
- •3.6 Расчет суммарных источников вещества в катодной и анодной зонах
- •3.8 Расчет материального баланса изменения состава электролита во времени
3.3 Расчет плотности поступающего электролита
Плотность электролита при нормальных начальных условиях (200С, 760 мм.рт.ст.) рассчитывается по формуле:
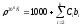
где Сi - концентрация i-го компонента (кроме воды), кг/м3;
bi – поправочный коэффициент для i-го компонента.
Плотность электролита при рабочей температуре t:
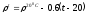
где 0,6 – температурный коэффициент плотности.
Для входящего потока:
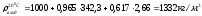
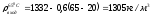
3.4 Расчет интенсивностей источников вещества за счет электродных реакций
На электродах идут
следующие электрохимические реакции
со следующими выходами по току: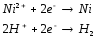
К: Вт = 90 % (1)
Вт = 10 %
(2) 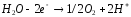
А: Вт = 100 % (3)
Расчет интенсивностей вещества за счет электродных реакций рассчитывается по следующей формуле:
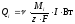 ,
,
где ν – стехиометрический коэффициент;
z – количество электронов, участвующих в реакции;
Mi – молярная и атомная массы компонентов, кг/моль;
F – постоянная Фарадея, равная 96500 Кл/моль;
I – токовая нагрузка, А;
Вт – выход по току электрохимической реакции.
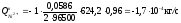 ,
,
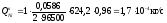 ,
,
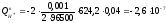 кг/с,
кг/с,
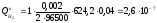 кг/с,
кг/с,
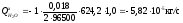 ,
,
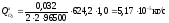 ,
,
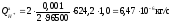 .
.
3.5 Расчет интенсивностей источников вещества за счет перехода его из одного агрегатного состояния в другое
Испарение воды в электрохимических системах возможно за счет равновесного испарения и за счет конвективного уноса паров.
Равновесное испарение имеет место, когда газ насыщается парами воды до равновесного значения. Этот механизм реализуется в случае выделения газообразных продуктов на электродах. Интенсивности источников вещества за счет равновесного испарения рассчитывается по следующей формуле:
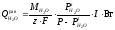 ,
,
где
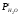 - парциальное давление паров воды над
электролитом при заданной температуре
электролита находим по справочнику
[8], мм.рт.ст.,
- парциальное давление паров воды над
электролитом при заданной температуре
электролита находим по справочнику
[8], мм.рт.ст.,
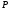 - атмосферное
давление, равное 760 мм.рт.ст.,
- атмосферное
давление, равное 760 мм.рт.ст.,
Sэ - площадь зеркала электролита.
- анодная:
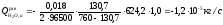 ,
,
- катодная:
 .
.
Для расчета интенсивности испарения за счет конвективного уноса используют эмпирическую формулу:
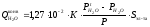
где 1,27.10-2
– коэффициент, характеризующий плотность
потока испарения при температуре кипения
раствора в сухой воздух,
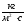 ,
,
К – безразмерный коэффициент, величина которого зависит от скорости движения воздуха, для данного примера принимаем 0,2,
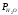 -
парциальное давление паров воды при
температуре внешней среды и данной
влажности находим в справочнике [8],
мм.рт.ст.
-
парциальное давление паров воды при
температуре внешней среды и данной
влажности находим в справочнике [8],
мм.рт.ст.
- анодная
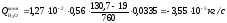 ,
,
- катодная
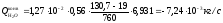
3.6 Расчет суммарных источников вещества в катодной и анодной зонах
Суммарные интенсивности источников вещества определяются суммированием различных интенсивностей по компонентам. Результаты для катодной и анодной зон сведены в таблицы 5 и 6.
Таблица 5 – Суммарные источники вещества в катодной зоне
|
QΣNiSO4 |
-4,8E-04 |
кг/с |
|
QΣH2SO4 |
-1,27E-05 |
кг/с |
|
QΣH2O |
-4,55E-05 |
кг/с |
|
QΣH2 |
2,59E-07 |
кг/с |
|
QΣNi |
1,82E-04 |
кг/с |
Таблица 6 – Суммарные источники вещества в анодной зоне
|
QΣNiSO4 |
0 |
кг/с |
|
QΣH2SO4 |
3,17E-04 |
кг/с |
|
QΣH2O |
-1,19E-04 |
кг/с |
|
QΣО2 |
5,18E-05 |
кг/с |
