
Азот
.pdf
Элементы VA-подгруппы
Общая характеристика
периоды |
|
группы |
ряды |
V |
|
|
|
|
N |
7 |
II |
2 |
азот |
|
|
|
14,007 |
|
|
|
P |
15 |
III |
3 |
фосфор |
|
|
|
30,974 |
|
|
|
23 |
V |
|
4 |
ванадий |
|
|
|
50,942 |
|
IV |
|
As |
|
|
|
33 |
|
|
5 |
мышьяк |
|
|
|
74,922 |
|
|
|
41 |
Nb |
|
6 |
ниобий |
|
|
|
92,906 |
|
V |
|
Sb |
|
|
|
51 |
|
|
7 |
сурьма |
|
|
|
121,75 |
|
|
|
73 |
Ta |
|
8 |
тантал |
|
VI |
|
180,948 |
|
|
Bi |
|
|
|
|
83 |
|
|
9 |
висмут |
|
|
|
208,98 |
|
|
|
105 |
Db |
VII 10 |
дубний |
||
|
|
[262] |
|
VА-подгруппу образуют р-элементы: азот N, фосфор
Р, мышьяк As, сурьма Sb и висмут Bi.
Элементы N, P – типичные неметаллы,
у неметаллов As и Sb появляются некоторые свойства,
присущие металлам, у висмута металлические свойства
преобладают, хотя типичным металлом он не является.
Общая формула валентных электронов у элемен-
тов VА-группы – ns2np3.
ns |
|
|
np |
|
Атомы этих элементов имеют |
|
|
|
|
|
три неспаренных валентных элек- |
|
|
|
|
|
|
|
|
|
|
|
трона. За счет трех неспаренных электронов все элементы в простых веществах образуют три ковалентные связи, но у азота три связи объединяют 2 атома, образуя очень проч-
ную молекулу N N, а у других элементов – каждый атом связан с тремя другими с образованием молекул типа Э4 (бе-
лый фосфор и желтый мышьяк) или полимерных структур.
У азота простое вещество в любом агрегатном состоянии состоит из отдельных молекул, при обычных условиях это газ. У всех остальных элементов простые вещества
– твердые.
Степень окисления (–3) для элементов VА-группы является минимальной. Наиболее устойчива она у N, при
переходе к Bi с увеличением числа электронных слоев ее устойчивость па-
дает. Элементы N, P, As, Sb с водородом образуют гидриды типа ЭН3,
проявляющие основные свойства, наиболее ярко они выражены у аммиа-
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

ка NH3. В подгруппе устойчивость соединений ЭН3 и их основные свойст-
ва уменьшаются.
Все элементы VА-группы проявляют высшую степень окисления +5.
Все они образуют оксиды типа Э2O5 ( оксид Bi2О5 – неустойчив), которым соответствуют кислоты, сила кислот ослабевает при движении вниз по под-
группе.
Степень окисления +5 наиболее устойчива у Р. Соединения Bi(+5) –
очень сильные окислители. Сильные окислительные свойства проявляет азотная кислота, особенно концентрированная.
У висмута более устойчива степень окисления (+3), которая также достаточно устойчива у Sb и As. Соединения N(+3), и особенно
Р(+3), проявляют сильные восстановительные свойства.
В степени окисления +3 все элементы VА-группы образуют оксиды
типа Э2О3. Оксидам N и P соответствуют слабые кислоты. Оксиды и гидрокси-
ды As и Sb – амфотерны, основной характер преобладает у оксида и гидрокси-
да Bi(+3). Таким образом, в подгруппе кислотный характер оксидов и гид-
роксидов элементов в степени окисления (+3) ослабевает, и усиливаются
основные свойства, более характерные для гидроксидов металлов.
Элементы VА-группы, помимо перечисленных степеней окисления
+5, +3, –3, проявляют и другие промежуточные степени окисления.
Для азота известны все степени окисления от –1 до +5.
Азот, как и все элементы второго периода, существенно отличается от своих электронных аналогов. По этой причине, а также из-за большого числа степеней окисления и многообразия соединений, химия азота рассматри-
вается отдельно от других элементов VА–подгруппы.
Наиболее распространенным в природе элементом VА-группы явля-
ется фосфор. Его содержание в земной коре – 0,09 масс. %; фосфор находит-
ся главным образом в виде фосфата кальция. Содержание азота – 0,03%, ос-
новная его доля сосредоточена в атмосфере в виде N2. Содержание азота в
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

воздухе по объему составляет ~ 78 %. В очень малых количествах в зем-
ной коре встречаются нитраты натрия и калия (селитры). Мышьяк, сурьма и висмут относятся к редким элементам с содержанием в земной коре 10–5 5 .10–
4 %; в природе они находятся, в основном, в виде сульфидов.
Азот и фосфор – очень важные элементы биосферы, поэтому значи-
тельная часть производимых в химической промышленности нитратов и фос-
фатов используется в качестве удобрений, которые необходимы для жизнедея-
тельности растений. В организме человека N и Р играют важную роль, – азот
входит в состав аминокислот, являющихся составной частью белков, фосфор в
форме Ca5[(PO4)3OH] входит в состав костей. В человеческом организме нахо-
дится в среднем около 1,8 кг N.
Некоторые характеристики атомов элементов VА-группы приведены в
таблице.
Таблица
Важнейшие характеристики атомов элементов VА-группы
Эле- |
Орби- |
Электроот- |
Энергия |
|
мент |
тальный |
рицатель- |
иониза- |
|
|
радиус |
ность (по |
ции, |
|
|
атома, нм |
Поллингу) |
кДж/моль |
|
N |
0,052 |
3,0 |
1402 |
увеличение числа элек- |
P |
0,092 |
2,2 |
1012 |
тронных слоев; |
|
0,100 |
2,2 |
945 |
увеличение размера атома; |
As |
||||
Sb |
0,119 |
2,0 |
829 |
уменьшение энергии иони- |
Bi |
0,129 |
2,0 |
705 |
зации |
|
|
|
|
уменьшение электроотри- |
|
|
|
|
цательности; |
|
Для сравнения – электроотрицательность Н – 2,2; О – 3,44. |
|||
Азот от других элементов подгруппы отличается очень маленьким орби-
тальным радиусом и высокой электроотрицательностью, N – третий по элек-
троотрицательности элемент, после F и О.
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Азот
|
|
|
|
|
|
|
Валентные электроны N –2s22p3. |
|||||
|
7 |
N 2s |
2 3 |
|
|
|
||||||
|
|
|
ns |
|
|
|
np |
|
|
|||
|
|
|
|
|
|
|
|
|
||||
|
|
2p |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
Азот |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
14,007 |
|
|
|
Азот, подобно другим элементам второго периода, |
||||||
|
|
|
|
|
|
|||||||
|
|
|
||||||||||
заметно отличается от элементов своей подгруппы: |
||||||||||||
|
|
атом N имеет всего 4 валентные орбитали и в соединениях может обра- |
||||||||||
|
|
зовать только 4 ковалентные связи; |
||||||||||
|
|
из-за очень маленького атомного радиуса азот образует очень прочные |
||||||||||
|
|
-связи; |
|
|
|
|
|
|
|
|
||
|
|
простое вещество в любом агрегатном состоянии состоит из отдельных |
||||||||||
|
|
очень прочных молекул N |
N и отличается высокой инертностью; |
|||||||||
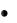 по электроотрицательности N уступает только F и О;
по электроотрицательности N уступает только F и О;
 азот проявляет все возможные степени окисления: -3, –2, -1, 0, +1, +2, +3, +4, +5.
азот проявляет все возможные степени окисления: -3, –2, -1, 0, +1, +2, +3, +4, +5.
Большое число степеней окисления и многообразие соединений делает
химию азота весьма сложной. Сложность усугубляется также характерными для многих окислительно-восстановительных реакций кинетическими затруд-
нениями, обусловленными очень прочными кратными связями между атомами
N и атомами N и О. Поэтому электродные потенциалы мало помогают в опре-
делении продуктов ОВР.
Наиболее устойчивым соединением N является простое вещество.
В водных растворах, особенно кислых, очень устойчив ион NH4+.
Азот является составной частью воздуха, из которого N2 и получают.
Основное количество N2 используется для синтеза аммиака, из которого затем получают другие соединения азота. Среди соединений азота самое широкое практическое применение находят аммиак, азотная кислота и их соли.
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Ежегодное мировое производство NH3 составляет ~ 97 млн. т/год, азотной ки-
слоты – 27 млн. т/год. Химия этих важнейших соединений N будет рассмот-
рена в первую очередь, после обсуждения свойств простого вещества.
Простое вещество
Молекула N2 – самая прочная из всех двухатомных молекул простых веществ. Три общие электронные пары в молекуле N N располагаются на свя-
зывающих орбиталях, на разрыхляющих орбиталях электронов нет, – это при-
водит к очень высокой энергии химической связи – 944 кДж/моль (для срав-
нения, энергия связи в молекуле О2 равна – 495 кДж/моль). Прочная связь обусловливает высокую инертность молекулярного азота. С химической инертностью азота связано название этого элемента. По-гречески «азот» озна-
чает "безжизненный".
При обычных условиях N2 – это бесцветный газ без запаха и вкуса.
Температуры кипения и плавления N2 близки: –196ОС, и –210ОС.
Азот получают фракционной перегонкой воздуха, – для этого воздух
при низких температурах сжижают, а затем начинают повышать температуру.
Из компонентов воздуха азот имеет самую низкую температуру кипения и
образует самую легкокипящую фракцию. При фракционной перегонке одно-
временно получают кислород и инертные газы.
Основное количество N2 идет на производство аммиака, кроме того,
азот применяют для создания инертной атмосферы, в том числе при производ-
стве некоторых металлов; жидкий азот используют также в качестве охлаж-
дающего агента в лаборатории и в промышленности.
При комнатной температуре азот медленно реагирует только с Li с обра-
зованием Li3N. При горении на воздухе магния, вместе с оксидом MgO образу-
ется и Mg3N2.
Нитриды. Бинарные соединения азота с элементами, менее элек-
троотрицательными, чем N, называют нитридами.
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Ионные нитриды содержат анион N3–. Ионные нитриды образуют Li,
металлы II и IБ-группы; в водных растворах они подвергаются необратимо-
му гидролизу.
Mg3N2 + 6H2O = 2NH3 + 3 Mg(OH)2
С металлами р-блока и некоторыми легкими неметаллами азот об-
разует ковалентные нитриды, например, AlN, BN.
Большинство d-металлов образуют с азотом при высоких температурах нестехиометрические продукты внедрения, в которых атомы N занимают пус-
тоты в кристаллических решетках металлов. Поэтому такие нитриды по внеш-
нему виду, по электро- и теплопроводности напоминают металлы, но отлича-
ются от них высокой химической инертностью, твердостью и тугоплавкостью.
Например, нестехиометрические нитриды Ta и Ti плавятся при температурах выше 3200оС.
Азот непосредственно не реагирует с галогенами, а с кислородом взаимодействует только в экстремальных условиях (при электрическом
разряде).
Наиболее важной в практическом отношении является реакция азота с H2, в результате которой получается аммиак.
N2 + 3H2 2NH3; H0 = –92 кДж/моль.
Экзотермичность этой реакции указывает на то, что суммарная прочность связей в молекулах аммиака выше, чем в исходных молекулах. Повышение температуры в соответствии с принципом Ле-Шателье, приводит к смещению равновесия в сторону эндотермической реакции, т.е. в направлении разложения аммиака. Однако при нормальных условиях реакция идет чрезвычайно медлен-
но, слишком велика энергия активации, необходимая для ослабления прочных связей в молекулах азота и водорода. Процесс поэтому процесс приходится вести при температуре около 5000С. Для смещения равновесия при высокой температуре вправо повышают давление до 300 – 500 атм., при этом равнове-
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

сие смещается в направлении реакции, идущей с уменьшением числа молекул газа, т.е. в направление образования аммиака. Повышения скорости достигают за счет применения катализаторов. Эффективен плавленый катализатор на ос-
нове Fe3O4 с добавками Al2O3 и SiO2 и катализатор на основе металлического
Fe. Синтез аммиака из азота и водорода является важнейшей реакцией про-
мышленной химии азота.
Соединения азота
Аммиак и соли аммония
Азот в аммиаке и солях аммония находится в минимальной степени окисления (–3). Степень окисления (–3) достаточно устойчива у азота.
Аммиак при обычных условиях – бесцветный газ с характер-
ным резким запахом, знакомым по запаху «нашатырного спирта» (10% рас-
твора аммиака в воде). Этот газ легче воздуха, поэтому его можно собирать в перевернутые вверх дном сосуды. Аммиак легко переходит в жидкость. Для этого его достаточно при обычном давлении охладить до –33,5оС. Того же эф-
фекта можно достигнуть при комнатной температуре, но повышая давление до
7 – 8 атм. При повышенном давлении жидкий аммиак хранят в стальных балло-
нах. Испаряясь, жидкий аммиак вызывает охлаждение в окружающей среде. На этом основано его применение в холодильной технике. Легкая сжижаемость аммиака обусловлена водородными связями между его молекулами. Прочность водородных связей между молекулами аммиака обусловлена очень высокой электроотрицательностью азота.
Жидкий аммиак бесцветен, подвергается автопротолизу:
2NH3 NH4+ + NH2–
Константа этого равновесия равна 2 .10– 23 (при –50оС). Жидкий аммиак
является хорошим ионизирующим растворителем. Соли аммония и слабые
кислоты, например, H2S, растворенные в жидком аммиаке, становятся сильны-
ми кислотами.
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Аммиак хорошо растворим в воде. Высокую растворимость аммиака в воде (до 700 объемов NH3 в одном объеме воды) также объясняют образовани-
ем водородных связей, но уже с молекулами воды. Концентрированный рас-
твор содержит 25 массовых % аммиака и имеет плотность 0,91 г/см3. Молярная концентрация NH3 в концентрированных водных растворах достигает ~13
моль/л.
Молекула NH3 имеет пирамидальное строение, которое объясняют sp3-
гибридизацией валентных атомных орбиталей азота. Одна из вершин тетраэд-
ра занята неподеленной парой электронов. Связь N –– H довольно прочная,
энергия связи составляет 389 кДж/моль, длина связи – 0,1 нм, угол между свя-
зями –108,3о. При присоединении катиона H+ за счет неподеленной электрон-
ной пары N, образуется тетраэдрический очень устойчивый ион аммония
NH4+.
Наличие неподеленной электронной пары у N в молекуле NH3, обу-
славливает многие характерные для аммиака свойства.
Молекула NH3 является хорошим донором электронной пары (ДЭП),
т.е. основанием по Льюису, и очень хорошим акцептором протонов A(Н+),
т.е. основанием по Бренстеду:
NH3 + H+ NH4+. NH3 акцептирует протон, подобно ионам ОН–: OH– + H+ H2O
Акцепторные свойства NH3 слабее, чем у аниона OH–. Константа протолиза для NH3 равна 1,8 .109, а для иона OH– – 1014.
Реакции с кислотами – это наиболее характерные для NH3 реакции.
Способность аммиака к образованию донорно-акцепторных связей на-
столько велика, что он может отрывать ионы водорода от такого прочного со-
единения, как вода.
NH3 + H––OH NH4+ + OH–
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Однако в этом случае реакция протекает в малой степени, поскольку ОН–
– более сильный А(Н+), и количество продуктов NH4+ и OH– мало по сравнению с равновесной концентрацией аммиака. Водные растворы аммиака ведут себя подобно слабым основаниям. По устоявшейся традиции аммиак часто обозна-
чают формулой NH4OH и называют гидроксидом аммония, однако молекул
NH4OH в растворе нет. Щелочную реакцию водного раствора NH3 часто опи-
сывают не приведенным выше равновесием, а как диссоциацию молекул
NH4OH:
NH4OH NH4+ + OH–
Константа этого равновесия равна 1,8 .10–5. В одном литре одномолярно-
го раствора аммиака концентрация ионов NH4+ и OH– составляет 3,9.10–3
моль/л, рН = 11,6.
Равновесие между аммиаком и OH– способны сильно сместить вправо катионы некоторых металлов, образующие с ионами OH– нерастворимые гидроксиды.
FeCl3 + 3NH3 + 3Н–ОН Fe(OH)3 + 3NH4Cl.
Аммиак можно использовать для получения нерастворимых оснований.
При действии кислот на водные растворы аммиака образуются соли аммония.
NH3 + HCl = NH4Cl
Почти все соли аммония бесцветны и растворимы в воде.
Равновесие NH3 + H+ NH4+ сильно смещено вправо (К = 1,8 .109),
это означает, что, NH3 является сильным акцептором протонов, а катион NH4+
является слабым донором H+, т.е. кислотой по Бренстеду. При добавлении щелочи к солям аммония образуется аммиак, который легко определить по за-
паху.
NH4Cl + NaOH = NH3 + H2O + NaCl.
Этой реакцией обычно пользуются для обнаружения ионов аммония в растворе.
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Подобные реакции можно использовать для лабораторного получения
NH3.
Хлорид аммония (его называют «нашатырь») при высоких температурах реагирует с оксидами на поверхности металлов, как кислота, обнажая чистый металл. На этом же основано использование твердой соли NH4Cl при пайке металлов. «Кислотный» H+ из иона NH4+ способен окислять очень активные металлы, например, Mg.
Mg + 2NH4Cl = H2 + MgCl2 + 2NH3
Характерным свойством солей аммония является их термическая неус-
тойчивость. При нагревании они довольно легко разлагаются. Продукты раз-
ложения определяются свойствами кислотного аниона. Если анион проявляет окислительные свойства, то происходит окисление NH4+ и восстановление аниона-окислителя.
NH4NO2 = N2 + 2H2O
NH4NO3 = N2О + 2H2O или 2NH4NO3 = N2 + O2 + 4H2O
(NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O
Из солей летучих кислот выделяется аммиак и кислота (или ее ангид-
рид), а в случае нелетучих кислот (например, Н3РО4) – только NH3. NH4 HCO3 = NH3 + H2 O + CO2
Гидрокарбонат аммония NH4HCO3 применяют в хлебопекарной про-
мышленности, образующиеся газы придают тесту необходимую пористость.
Соли аммония используют в производстве взрывчатых веществ и в
качестве азотных удобрений . Аммонал, применяемый в практике взрывных работ, представляет собой смесь соли NH4NO3 (72%), порошка Al (25%) и уг-
ля (3%). Эта смесь взрывается только после детонации.
Второй тип реакций, в которых NH3 проявляет свойства донора элек-
тронной пары – это образование амминных комплексов. Аммиак в роли лиганда присоединяется к катионам многих d-элементов, образуя химиче-
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
