
- •Министерство образования и науки Российской Федерации
- •Предисловие
- •Введение
- •Часть 1. Современные представления о строении различных групп материалов
- •Глава 1. Основные различия в свойствах групп материалов
- •Типы химической и физической связей в материалах
- •В материалах:
- •1.2. Материалы с различным типом химической связи
- •1.2.1. Металлы и сплавы (металлический тип связи)
- •1.2.2. Полимеры (ковалентный и молекулярно - ковалентный типы связи)
- •1.2.3. Керамика (ковалентный и ионный типы связи)
- •1.2.4. Карбиды и интерметаллиды (ковалентно - металлический тип связи)
- •1.2.5. Композиционные материалы (смешанный тип связей)
- •Pис. 1.2. Схематическое представление вклада разных типов связи в материалах
- •Вопросы для самопроверки
- •Часть 2. Металлические материалы
- •Глава 2. Строение и свойства металлов и сплавов
- •2.1. Кристаллическое строение металлов и сплавов
- •Кристаллические структуры переходных металлов 4-го периода*
- •Внедрения; б – твердый раствора замещения со статистическим распределением атомов; в – упорядоченный твердый раствор замещения
- •Из сплавов (деформируемых)
- •2.2. Несовершенства кристаллической структуры
- •Линейные и точечные несовершенства кристаллической структуры
- •2.3. Основные свойства и характеристики металлов и сплавов
- •Характеристики механических свойств
- •Характеристики физических свойств
- •Характеристики химических свойств
- •Характеристики технологических свойств.
- •2.4. Пластическая деформация
- •Пластической деформации [с.В. Грачев, в.Р. Бараз и др.]
- •В зависимости от степени холодной деформации: ρ – удельное электросопротивление; Ηс – коэрцитивная сила; μ – магнитная проницаемость;
- •Температуры отжига холоднодеформированного металла
- •Температура начала рекристаллизации, интервал температур рекристаллизационного отжига и горячей обработки давлением
- •2.5. Термическая обработка
- •Технологические параметры термообработки
- •Время нагрева τн, температура выдержки tв, время выдержки τ в, скорость охлаждения V охл
- •Скорости охлаждения при различных видах термической обработки
- •Скорость охлаждения при каждом виде термообработки предопределяет равновесность или неравновесность получаемых продуктов фазовых превращений.
- •И отпуске (б). Исходное состояние: пересыщенный при закалке твердый раствор (а); мартенсит углеродистый (б)
- •Термообработка – отжиг
- •Типы отжигов для сплавов разного состава
- •Отжиги первого рода
- •Типы отжигов первого рода
- •Отжиги второго рода
- •Отжиги второго рода. Отжиги углеродистых сталей
- •Общепринятые обозначения линий и критических точек на диаграмме железо-цементит
- •Эвтектоид носит название перлит (п). Перлит – это структура, состоящая из двух фаз: феррита и цементита, частицы которых имеют пластинчатое строение (рис. 2.22, а).
- •Фазовый состав сталей после отжига в зависимости от содержания углерода
- •Технологические параметры специальных отжигов сталей
- •Микроструктура пластинчатого (б) и сферического(зернистого) (в) цементита
- •Для доэвтектоидной стали с 0,45 % углерода; скорости охлаждения: V 1 – с печью; v2 – на воздухе; v3 – в масле; v4 – в воде
- •Продукты диффузионного распада переохлажденного аустенита
- •Перлит может быть получен при охлаждении с печью, сорбит – при охлаждении на воздухе, а троостит–при больших скоростях охлаждения и даже при закалке.
- •Упрочняющая термическая обработка: закалка и старение
- •От температуры (а) и времени (б) старения: t1 ‹ t2 ‹ t3; о – максимум твердости;
- •Закалка и отпуск сталей
- •Закалка сталей на мартенсит
- •Технология закалки
- •Образца(Vц), перлитную структуру на поверхности(Vп) – мартенситную
- •Отпуск сталей
- •От температуры отпуска (и.И. Новиков) Виды отпуска и применение
- •Виды отпуска и структуры сталей
- •2.6. Термомеханическая обработка сталей
- •Рекристаллизации
- •2.7. Поверхностная обработка сталей и сплавов
- •Химико-термическая обработка сплавов.
- •Хто с диффузионным насыщением углеродом и азотом
- •Нитроцементация (азотонауглероживание)
- •Параметры процессов хто, характеристики слоя и свойства сталей
- •Химико-термическая обработка с диффузионным насыщением металлами (диффузионная металлизация)
- •Поверхностная закалка сталей
- •Поверхностная лазерная обработка
- •Виды поверхностной лазерной обработки
- •Поверхностное пластическое деформирование
- •Способы ппд
- •2.8. Обеспечение служебных характеристик и повышение технико-экономической эффективности применения металлических материалов
- •2.8.1. Статическая прочность сплавов
- •Обеспечение статической прочности сплавов композиционных и гетерофазных материалов
- •2.8.2. Циклическая прочность
- •Факторы, влияющие на предел выносливости
- •2.8.3. Контактная выносливость
- •Способы обеспечения контактной выносливости:
- •Коэффициент вязкости разрушения различных материалов
- •2.8.5. Износостойкость
- •Стали и сплавы для работы в контакте с рабочей средой
- •Твердость и модуль упругости карбидов
- •2.8.6. Жаропрочность
- •2.8.7. Термостойкость
- •2.8.8. Поверхностная стойкость
- •Обеспечение жаростойкости
- •Вопросы для самопроверки
- •Глава 3. Сплавы на основе железа
- •3.1. Машиностроительные конструкционные стали
- •3.1.1. Классификация конструкционных сталей
- •Классификация сталей по химическому составу
- •Классификация и маркировка в зависимости от качества стали
- •3.1.2. Углеродистые стали
- •3.1.3. Легированные стали
- •Влияние легирующих элементов на структуру и свойства сталей
- •Влияние легирующих элементов на феррит
- •Влияние легирующих элементов на аустенит и мартенсит
- •Цементуемые легированные стали
- •Улучшаемые легированные стали
- •Механические свойства некоторых улучшаемых сталей
- •Критический диаметр легированных сталей
- •Характеристика высокопрочных сталей
- •Комплекс механических свойств среднеуглеродистых легированных сталей, упрочняемых закалкой с последующим низким отпуском
- •Н18к9м5т от температуры старения
- •Механические свойства мартенситно-стареющих сталей системы Fe–Ni–Co–Mo–Ti
- •3.1.4. Стали для подшипников качения
- •Требования к подшипниковым сталям и пути обеспечения необходимых свойств
- •Термическая обработка подшипниковых сталей типа шх
- •3.1.5. Стали рессорно-пружинные
- •Предел текучести рессорно-пружинных сталей общего назначения*
- •Марки и применение рессорно-пружинных сталей
- •3. 2. Стали специального назначения
- •3.2.1. Коррозионностойкие стали
- •3.2.2. Жаростойкие стали
- •3.2.3. Жаропрочные стали
- •Двс и пути их обеспечения
- •Условия эксплуатации:
- •3.3. Чугуны
- •Химический состав конструкционных чугунов
- •Форма графита и названия чугунов
- •Зависимость механических свойств чугунов от формы графита и структуры металлической части
- •3.3.1. Серые чугуны
- •Применение серых чугунов
- •3.3.2. Высокопрочные чугуны
- •Применение высокопрочных чугунов
- •Применение чугунов с вермикулярным графитом
- •3.3.4.Ковкие чугуны
- •Применение ковких чугунов
- •Применение специальных чугунов
- •3.4. Порошковые конструкционные и легированные стали
- •3.4.1. Классификация порошковых сталей
- •Марки и применение пористых конструкционных материалов
- •3.4.2. Применение порошковых сталей
- •Вопросы для самопроверки
- •Глава 4. Цветные металлы и сплавы
- •4.1. Алюминиевые сплавы
- •Удельная прочность конструкционных сплавов
- •4.1.1. Классификация и маркировка алюминиевых сплавов
- •Соответственно
- •Условные обозначения видов термической обработки деформируемых сплавов
- •4.1.2. Деформируемые сплавы
- •Разрыву и относительное удлинение в мягком состоянии
- •Подготовленная для плакировки
- •Характеристики надежности сплава в95
- •Механические свойства алюминиевых деформируемых сплавов, упрочняемых термообработкой
- •4.1.3. Литейные алюминиевые сплавы Сплавы на основе системы Al – Si
- •Сплавы на основе системы Al – Cu
- •Сплавы на основе системы Al – Mg
- •4.2. Медь и медные сплавы
- •И зависимость механических свойств от содержания цинка (б)
- •(Кроме бериллиевых бронз)
- •4.2.1. Латуни
- •Механические свойства *и назначение литейных латуней
- •4.2.2. Бронзы
- •Механические свойства*деформируемых (гост 5017–74) и литейных (гост 613–79) оловянных бронз
- •Механические свойства* деформируемых и литейных алюминиевых бронз
- •Механические свойства бериллиевой бронзы БрБ2 в зависимости от состояния сплава
- •4.3. Титановые сплавы
- •4.3.1. Легирующие элементы титановых сплавов
- •4.3.2.Фазовые превращения в титановых сплавах
- •Сплавов (легированных β - стабилизаторами)
- •4.3.3. Термическая обработка титановых сплавов
- •4.3.4. Классификация промышленных титановых сплавов
- •4.3.5. Деформируемые сплавы
- •Химические составы и свойства после отжига титановых деформируемых сплавов
- •Применение и свойства титановых деформируемых сплавов
- •4.3.6.Литейные сплавы
- •4.4. Магниевые сплавы
- •4.5. Антифрикционные (подшипниковые) сплавы на оловянной, свинцовой и цинковой основах
- •Критериями оценки антифрикционных материалов являются:
- •Требуемые свойства сплавов для подшипников скольжения
- •Темное поле – твердый раствор сурьмы в олове; светлые крупные частицы – химическое соединение SnSb, мелкие частицы – Cu3Sn (справа – схематическое изображение микроструктуры)
- •Вопросы для самопроверки
- •Часть 3. Неметаллические материалы
- •Глава 5. Общая характеристика неметаллических материалов
- •5.1. Классификация, строение и способы получения полимеров
- •5.2. Фазовые состояния и надмолекулярная структура полимеров
- •Надмолекулярная структура аморфных полимеров
- •5.3. Физические состояния полимеров
- •Термомеханические кривые кристаллических полимеров
- •Термомеханические кривые сетчатых полимеров
- •5.4. Способы управления структурой и свойствами полимерных материалов
- •Вопросы для самопроверки
- •Глава 6. Основные свойства неметаллических материалов
- •6.1. Механические свойства
- •6.2. Теплофизические свойства
- •6.3. Диэлектрические свойства
- •Классификация диэлектриков по диэлектрической проницаемости
- •Классификация диэлектриков по диэлектрическим потерям
- •Вопросы для самопроверки
- •Глава 7. Пластические массы
- •7.1. Основные виды модифицирующих добавок
- •7.2. Термопластичные полимеры и материалы на их основе
- •Полиэтилен
- •Полипропилен
- •Полиизобутилен
- •Полистирол
- •Политетрафторэтилен (ф-4)
- •Политрифторхлорэтилен (ф-3)
- •Поливинилхлорид
- •Полиакрилаты
- •Полиамиды
- •Полиуретаны
- •Поликарбонаты
- •Полиимиды
- •Полиэтилентерефталат
- •Полиформальдегид
- •Пентапласт
- •Марочный ассортимент и области применения термопластов
- •7.3. Термореактивные полимеры и материалы на их основе
- •Фенолоформальдегидные смолы
- •Эпоксидные смолы
- •Полиэфирные смолы
- •Кремнийорганические смолы
- •Марочный ассортимент и области применения основных термореактивных пресс-материалов и литьевых пм
- •7.4. Термоэластопласты
- •7.5. Методы получения изделий из пластических масс
- •7.5.1. Прессование
- •7.5.2. Литье под давлением
- •7.5.3. Экструзия
- •7.5.4. Термоформование
- •7.5.5. Механическая обработка пластмасс
- •7.6. Газонаполненные пластики
- •Вопросы для самопроверки
- •Глава 8. Волокнистые полимерные композиционные материалы
- •Типичные классификационные модели ап
- •8.1. Стеклопластики
- •8.2. Углепластики
- •8.3. Органопластики
- •Свойства элементарных волокон
- •8.4. Базальтопластики
- •8.5. Термопластичные композиционные материалы
- •8.6. Методы формования изделий из армированных пластиков
- •8.6.1. Контактное формование и напыление
- •8.6.2. Формование под давлением
- •8.6.3. Формование прессованием и пропиткой в замкнутой форме
- •8.6.4.Формование намоткой
- •8.6.5. Пултрузия
- •Вопросы для самопроверки
- •Глава 9. Природные полимеры и их производные Эфиры целлюлозы
- •Вопросы для самопроверки
- •Глава 10. Резиновые материалы
- •10.1. Классификация каучуков
- •10.2. Компоненты резиновых смесей
- •10.3. Способы получения резинотехнических изделий
- •10.4. Прорезиненные ткани
- •10. 5. Применение резинотехнических изделий
- •Вопросы для самопроверки
- •Глава 11. Клеевые материалы
- •11.1.Клеи на основе термопластичных полимеров
- •11.2. Клеи на основе эластомеров
- •11.3. Клеевые (липкие) ленты
- •11.4. Клеи на основе термореактивных смол
- •Вопросы для самопроверки
- •Глава 12. Герметики
- •Вопросы для самопроверки
- •Глава 13. Лакокрасочные материалы
- •13.1. Требования к лакокрасочным материалам
- •13.2. Классификация и виды лакокрасочных материалов
- •13.3. Полимерные порошковые композиции и покрытия на их основе
- •Способы нанесения порошковых покрытий
- •Вопросы для самопроверки
- •Глава 14. Обивочные, прокладочные, уплотнительные и электроизоляционные материалы
- •Вопросы для самопроверки
- •Глава 15. Неорганические материалы
- •15.1. Технические керамики
- •Гексагональными слоями ( а и в) атомов кислорода
- •15.2. Неорганические стекла
- •Стекла с особыми свойствами
- •Стекла в автомобилестроении
- •15.3. Стеклокристаллические материалы
- •15.4. Слюда и слюдяные материалы
- •15.5. Асбест и материалы на его основе
- •Вопросы для самопроверки
- •Глава 16. Жидкокристаллические материалы
- •16.1. Классификация, структура и свойства жидких кристаллов
- •16.2. Жидкокристаллические композиты
- •Вопросы для самопроверки
- •Список литературы Основные литературные источники
- •Дополнительные литературные источники
Типы отжигов первого рода
|
Вид отжига |
Объект |
Цель |
|
Гомогенизационный (диффузионный) |
Слиток, отливка |
Устранение междендритной ликвации |
|
Рекристаллизационный
|
Деформированный полуфабрикат |
Устранение наклепа: разупрочнение, повышение пластичности |
|
Отжиг для уменьшения напряжений |
Полуфабрикаты после прокатки, ковки, правки,механической обработки, сварные соединения |
Снятие остаточных упругих напряжений |
Отжиги второго рода
Отжиг цветных сплавов разупрочняющий (гетерогенизационный) проводится для получения структуры с однородным распределением частиц промежуточных фаз и разупрочнения.
В этих сплавах в процессе изготовления изделия при технологических операциях, включающих высокотемпературный нагрев (литье, горячая деформация или сварка), возможен неконтролируемый распад твердого раствора. Это может приводить как к частичному упрочнению, так и к неравномерному распределению частиц промежуточных фаз (ПФ). Особенно неблагоприятным является образование частиц по границам зерен.
Для устранения неблагоприятного структурного состояния необходим нагрев сплава, чтобы произошло два фазовых превращения – растворение частиц ПФ и выделение этих частиц при медленном охлаждении в виде крупных равномерно распределенных частиц. Результатом отжига являются равномерное распределение частиц ПФ, снижение прочности, повышение пластичности. Гетерогенизационный отжиг широко применяют для алюминиевых, медных, магниевых, никелевых и других сплавов.
Отжиги второго рода. Отжиги углеродистых сталей
Сплавы железа с углеродом при содержании его до 2,14 % без других легирующих элементов носят название «углеродистые стали».
К сталям применяют как универсальные отжиги (отжиги I рода), так и отжиги II рода: перекристаллизационный (полный), сфероидизирующий (неполный), нормализацию. При отжигах II рода в сталях происходят равновесные фазовые превращения.
Равновесные фазовые превращения в сплавах обычно изображаются графически на диаграммах состояния. Диаграммы состояния (или фазовые диаграммы) двойных сплавов строятся в координатах «температура – концентрация второго компонента».
Диаграмма состояния отражает равновесные фазовые превращения, потому что строится для условия очень медленного охлаждения сплавов из жидкого состояния до комнатной температуры.
Фазовые превращения в сталях можно проследить на части диаграммы «железо – углерод». Эта диаграмма показывает фазовый состав сплавов железа с углеродом с концентрацией от чистого железа до первого промежуточного соединения – карбида железа Fe3C, который традиционно называется «цементит». Цементит образуется при концентрации углерода 6,67 % (рис. 2.20).

Рис. 2.20. Фрагмент диаграммы состояния «железо-цементит»
На диаграмме «железо-цементит» (Fe - Fe3C) изображены:
– линии, они являются границами фазовых областей; «пересечение» фазовой границы при изменении температуры (при нагреве или охлаждении) означает фазовое превращение одной фазы в другую;
– линия ликвидуса – самая верхняя линия на диаграмме, при пересечении которой во время охлаждения сплава начинается образование твердой фазы;
– линия солидуса, показывает температуры, при которых заканчивается образование твердой фазы;
– фазовые области; двухфазные области соседствуют с однофазными.
Компонентами данной системы являются железо и углерод.
Железо – металл с температурой плавления 1539°С. Железо полиморфно, имеет три модификации: α, γ, δ. Модификации α и δ имеют объемноцентрированную решетку (ОЦК). Высокотемпературная модификация δ - Fe существует от температуры 1392°С до температуры плавления. Она не играет роли в твердофазных превращениях железоуглеродистых сплавов. Модификация α - Fe (или Feα) существует при температурах до 911°С. До температуры 768°С (точка Кюри) оно ферромагнитно, выше – парамагнитно. Модификация γ - Fe (Feγ) существует в интервале температур 911 - 1392°С. Кристаллическая решетка γ - железа – гранецентрированная (ГЦК); оно парамагнитно.
Углерод – металлоид. В сталях и чугунах углерод присутствует либо в твердых растворах внедрения, либо в виде химического соединенияFe3C.
Фазами системы Fe – Fe3C в твердом состоянии являются: твердые растворы – феррит (Ф или α) и аустенит (А или γ), и промежуточная фаза, химическое соединение – цементит Fe3C (Ц).
Феррит (Ф) – твердый раствор внедрения углерода в α-железе. Различают низкотемпературный α-феррит с растворимостью углерода до 0,02 % и высокотемпературный δ-феррит с предельной растворимостью углерода 0,1 %. В дальнейшем будет рассматриваться только α - феррит, который обозначается просто «феррит» (Ф). Протяженность ферритной области на диаграмме Fe-Fe3C, обозначенная точкамиGPQ, по концентрации незначительна: содержание углерода в феррите при комнатной температуре составляет всего 0,006 %.
Механические свойства (феррит подобен чистому железу) – это мягкая, пластичная фаза со следующими характеристиками: σв = 250 - 300 МПа; δ = 45 - 50 %; НВ 80 - 90.
Аустенит (А) – твердый раствор внедрения углерода в γ - железе. Нижняя часть аустенитной области ограничена точками GSE. Фазовая область аустенита существенно больше феррита как по концентрации, так и по температуре. Предельная растворимость углерода в аустените составляет 2,14 % (при температуре 1147ºС).
Механические свойства: при повышенной температуре аустенит имеет высокую пластичность (δ = 40 – 50 %); при охлаждении до комнатной температуры его твердость составляет 170 - 200 НВ.
Цементит (Ц) – это химическое соединение железа с углеродом (при 6,67 % С), карбид железа с формулой Fe3C; имеет сложную ромбическую решетку. Температура плавления цементита 1250°С.
Механические свойства. Цементит – соединение с ковалентно-металлической связью, имеет высокую твердость (800 НВ) и почти нулевую пластичность, а также высокую хрупкость. Влияние цементита на свойства железоуглеродистых сплавов зависит от его количества в структуре и формы его частиц. В общем случае, чем больше цементита содержит сплав, тем большую твердость он имеет.
Цементит, в зависимости от реакции образования при охлаждении сплавов системы Fe - Fe3C, подразделяют на первичный, вторичный и третичный. Первичный ЦI образуется из жидкой фазы ниже линии DC. Вторичный ЦII выделяется из аустенита (ниже линии ES). Третичный ЦIII выделяется из феррита.
Точка Р показывает предельную концентрацию углерода при температуре 727 ºС – 0,02 % С. Точка Q соответствует растворимости углерода при комнатной температуре – 0,006 %. Сплавы, содержащие менее 0,02 % С (левее точки Р), называюттехническим железом.
На рис. 2.21 показан фрагмент диаграммы Fe - Fe3C в области с сталей.
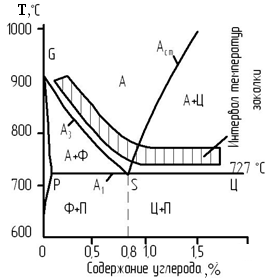
Рис. 2.21. Часть диаграммы, область сталей
Фазовые области в стальной части диаграммы:
– однофазные: феррит – область GPQ; аустенит – областьNJESG;
– двухфазные: аустенит + цементит – область SEFK; феррит + аустенит – областьGPS; феррит + цементит – область ниже линииPSK.
При выборе температур отжигов ориентируются на линии этой диаграммы, ограничивающие однофазные и двухфазные области. В практике термообработки сталей эти линии имеют специальное обозначение (табл. 2.6). Эти линии являются геометрическим местом критических точек сталей. Критические точки на диаграмме железо - цементит – температуры, при которых в сталях устанавливается фазовое равновесие.
Таблица 2.6
