
- •Министерство образования и науки Российской Федерации
- •Оглавление
- •Общие указания
- •1. Техническое, программное и библиографическое обеспечение практикума.
- •2. Организация работы
- •3.Основные требования к отчету
- •4.Принятые обозначения
- •Лабораторная работа №1. Оптимизация температурного режима в реакторе идеального вытеснения.
- •1.1. Объект исследования и эксперимент.
- •1.2. Обработка результатов эксперимента
- •1.3. Обсуждение результатов.
- •Лабораторная работа №2. Получение кинетических характеристик химической реакции на основе результатов эксперимента.
- •2.1. Объект исследования и эксперимент.
- •2.2. Обработка результатов эксперимента
- •2.3. Обсуждение результатов 2-й лабораторной работы.
- •Работа 3. Моделирование и исследование протекания сложной реакции в аппаратах с различными гидродинамическими режимами
- •3.1. Объект исследования и эксперимент.
- •3.2. Реактор идеального смешения.
- •Обработка результатов
- •3.3. Реактор идеального вытеснения План исследования.
- •Подготовка к расчету.
- •Обработка результатов
- •3.4. Каскад реакторов идеального смешения План исследования
- •Подготовка к расчету.
- •Обработка результатов
- •3.5. Обсуждение полученных результатов
- •Работа 4. Определение гидродинамического режима реактора на основе функции распределения времени пребывания.
- •4.1. Постановка задачи
- •4.2. Исходные данные
- •4.3. Порядок работы
- •Работа 5. Оптимизация химического процесса.
- •5.1. Формулирование задачи оптимизации.
- •5.2. Выполнение работы
- •5.3. Обсуждение результатов
- •Литература
- •Приложение. Краткие сведения о языке Бейсик.
- •«Математическое моделирование химико-технологических процессов» Методические указания к практикуму
Лабораторная работа №2. Получение кинетических характеристик химической реакции на основе результатов эксперимента.
2.1. Объект исследования и эксперимент.
Цель работы такова. Сделав небольшое число опытов, получить исходные данные и по ним рассчитать параметры уравнения Аррениуса для каждой из стадий сложной реакции. Это позволит в дальнейшем моделировать протекание данной реакции при различных температурах. Уравнение Аррениуса связывает константу скорости реакции с температурой:
![]() (2.1)
(2.1)
где k0 – предэкспоненциальный множитель (предэкспонента), Ea – энергия активации, R – универсальная газовая постоянная.
Следует учесть следующие особенности изучаемой реакции. Все ее стадии – первого порядка, вне зависимости от стехиометрии стадий (это принято для упрощения расчета и анализа объекта и практически не влияет на смысл данного цикла работ). Для простоты расчета принимается, что реакция в работе 2 проводится в аппарате идеального смешения. Это следует учитывать при вводе исходной информации – числа ступеней (ячеек) ячеечной модели, на которую рассчитана программа.
Для проведения численного эксперимента задаются температура и среднее время пребывания в реакторе, результатом эксперимента являются концентрации всех веществ на выходе из реактора. Вы должны задать условия таким образом, чтобы по результатам эксперимента определить значения энергий активации и предэкспоненциального множителя для каждой стадии реакции. Для этого нужно провести серию опытов при разных температурах. Для расчета энергии активации и предэкспоненты по уравнению Аррениуса минимальный объём серии – два опыта при двух как можно больше различающихся температурах (можно – по краям заданного интервала). Значение среднего времени пребывания не влияет на константы скорости и может быть задано на любом уровне. Чтобы обеспечить достаточную точность расчета, нужно следить, чтобы концентрации, получаемые в результате опытов, имели достаточно значащих цифр. Если вы видите, что значащих цифр мало (меньше трех), можете поменять время пребывания. Можно порекомендовать брать маленькое время пребывания при большой температуре и наоборот, в этом случае будет обеспечена близкая глубина превращения в двух рассматриваемых опытах.
Результаты эксперимента сводятся в таблицу вида:
|
N |
T |
t |
c1 |
c2 |
c3 |
c4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2.2. Обработка результатов эксперимента
Обработка результатов эксперимента начинается с решения системы уравнений математического описания реактора с целью определить значения констант скоростей всех стадий реакции при двух температурах Таким образом, на первом этапе расчета вы должны записать уравнения математического описания заданной вам реакции для условий: поток – идеальное смешение, режим стационарный. Математическое описание записывается в стандартной форме:
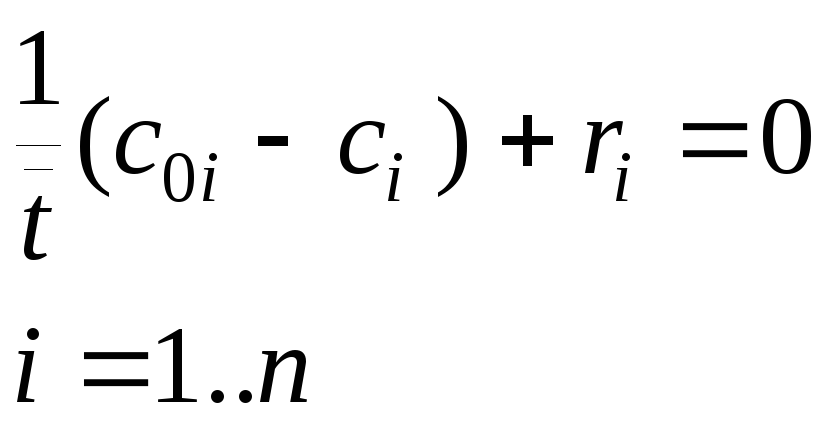 (2.4)
(2.4)
где: i – номер вещества, t – среднее время пребывания, c0i , ci – концентрации i-того вещества на входе и выходе из реактора, ri –скорость реакции по i-тому веществу.
Число уравнений равно числу веществ, участвующих в реакции (четырем). Если теперь для каждого из опытов подставить в эти уравнения значения t и концентраций – начальных, заданных в таблице исходных данных, и конечных, полученных в опыте, - то окажется, что уравнения содержат лишь три неизвестных: константы скорости трех стадий. При их расчете можно исключить любое из четырех уравнений. (Обратите внимание, что в исходных данных приведена начальная концентрация только первого компонента; начальные концентрации других веществ считаются равными 0).
В результате этой стадии расчета вы получаете значения констант скорости k1, k2 и k3, которые целесообразно свести в таблицу:
|
T, K |
k1 |
k2 |
k3 |
|
|
|
|
|
|
|
|
|
|
Затем вы переходите ко второму этапу расчета. Для расчета параметров уравнения Аррениуса это уравнение приводится к линейному виду:
![]() (2.5)
(2.5)
Уравнение (2.5) записывается для двух температур:
![]()
![]()
Вычитая из первого уравнения второе получаем:

Окончательно:
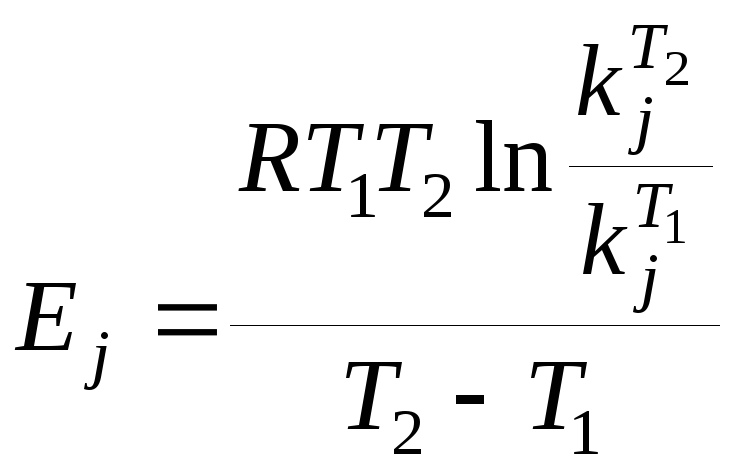 ,
, ![]()
Нужно иметь в виду, что все промежуточные расчеты нужно делать с возможно большей точностью, иначе ошибка расчета параметров может оказаться неприемлемой.
Рассчитав энергии активации и предэкспоненты для всех стадий реакции и проверив правильность расчета, вы имеете весь набор исходной информации для проведения следующих работ цикла.
