
Краткий курс органической химии. Часть 4
.pdf
31
Этот катион с отщеплением молекулы азота превращается в карбокатион, с которым могут происходить различные превращения: присоединение воды с образованием спирта, присоединение хлорид-аниона с образованием пропилхлорида, отщепление протона с образованием пропена, а также изомеризация в изопропилкатион и образование изопропилового спирта и изопропилхлорида. В качестве основного продукта при взаимодействии первичных алифатических аминов с азотистой кислотой получаются спирты, поскольку реакция проходит в большом избытке воды.
H2O |
|
|
H2O |
OH |
|
CH3CH2CH2 |
CH3CHCH3 |
CH3CHCH3 |
|||
CH3CH2CH2OH |
Cl |
||||
Cl |
_H |
_H |
|
||
CH3CH2CH2Cl |
CH3CHCH3 |
||||
|
CH3CH=CH2 |
|
Cl |
||
Первичные ароматические амины реагируют с азотистой кислотой аналогично первичным алифатическим аминам, однако образующиеся катионы арилдиазония в отличие от соответствующих алифатических катионов достаточно устойчивы, особенно при низкой температуре. Таким образом, при взаимодействии первичного ароматического амина с азотистой кислотой при 5-10О С в качестве продукта реакции образуется соль арилдиазония. Эта реакция получила название реакции диазотирования. Для анилина уравнение этой реакции выглядит следующим образом:
NH2 + NaNO2 + 2HCl |
N N + NaCl + 2H2O |
|
Cl |
хлорид фенилдиазония
Вторичные амины любого строения с азотистой кислотой вступают в реакцию, которая заканчивается на стадии нитрозирования атома азота. При этом образуются Ν- нитрозоамины.
NH CH3 NaNO2 |
N N=O |
HCl |
CH3 |
Ν-метиланилин Ν-метил-Ν-нитрозоанилин
Третичные алифатические амины с азотистой кислотой не взаимодействуют. Но третичные ароматические амины вступают с азотистой кислотой в реакцию электрофильного замещения в бензольное кольцо, причем электрофильной частицей в этой реакции является нитрозил-катион. В результате образуется продукт замещения атома водорода в пара- положении на нитрозогруппу, т.е. происходит нитрозирование по атому углерода ароматического кольца. Так, например, при взаимодействии Ν,Ν-диметиланилина с нитритом натрия в соляной кислоте образуется пара-нитрозо-Ν,Ν-диметиланилин:
N(CH3)2 NaNO2 |
N(CH3)2 |
HCl |
O=N |
www.mitht.ru/e-library
32
2.3. Особенности химического поведения ароматических аминов
2.3.1. Реакции электрофильного замещения
Выше уже отмечались некоторые особенности ароматических аминов:
взаимодействие с азотистой кислотой первичных ароматических аминов в отличие от первичных алифатических аминов приводит к образованию солей арилдиазония;
взаимодействие третичных ароматических аминов с азотистой кислотой протекает как электрофильное нитрозирование в ароматическое ядро.
Кроме реакции нитрозирования, ароматические амины легко вступают и в обычные
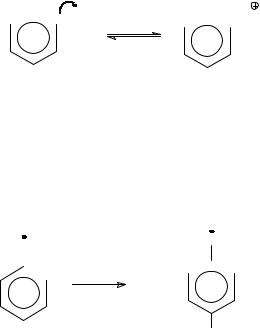
реакции электрофильного замещения в ароматическое ядро. Аминогруппа, обладая положительным мезомерным эффектом, который превышает воздействие отрицательного индуктивного эффекта, является одним из самых сильных электронодонорных заместителей, активируя молекулу и направляя замещение в орто- и пара-положения. Реакционная способность ароматических аминов в реакциях электрофильного замещения настолько высока по сравнению с бензолом и его гомологами, что некоторые реакции могут быть осуществлены в более мягких условиях и не требуют катализа. Однако, основный характер и склонность первичных ароматических аминов к окислению делает условия проведения некоторых реакций ароматического электрофильного замещения для них неприемлемыми, так как некоторые реагенты являются сильными кислотами и окислителями. Кислоты, протонируя аминогруппу, превращают ее из активирующего заместителя в сильный дезактивирующий заместитель:

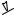 NH2 H
NH2 H
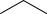
 NH3
NH3
+М>-I |
только –I-эффект |
(активирущий, 1-го рода) |
(дезактивирующий, 2-го рода) |
Бромирование. При взаимодействии анилина с бромной водой происходит электрофильное бромирование, причем реакционная способность анилина при введении одного атома брома, который является электроноакцепторным заместителем, в бензольное кольцо понижается незначительно, так что бромирование идет дальше до образования 2,4,6- триброманилина.
NH2 NH2 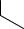 3Br2, H2O Br
3Br2, H2O Br
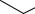 Br
Br
_3HBr
Br
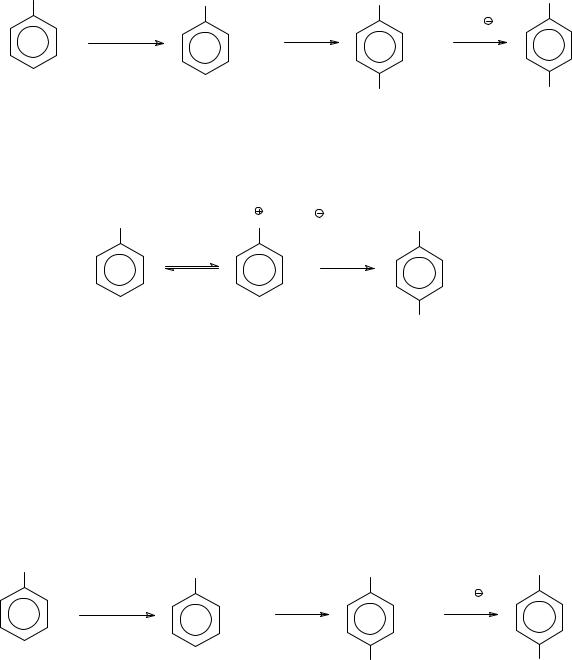
Для понижения реакционной способности анилина и получения монобромзамещенного анилина используют предварительное ацетилирование до ацетанилида, в котором сохраняется ориентирующее действие заместителя (+М-эффект по-прежнему больше –I-эффекта), но из-за сопряжения неподеленной пары электронов на атоме азота не только с бензольным кольцом, но и с карбонильной группой донорные свойства заместителя уменьшаются. Ацетанилид подвергают действию бромной воды, при этом образуется практически только один продукт – пара-бромацетанилид, который гидролизом (в кислой или щелочной среде) может быть превращен в пара-броманилин.
www.mitht.ru/e-library
33
NH2 |
NHCOCH |
NHCOCH |
NH2 |
|
3 |
3 |
|
|
(CH3CO)2O |
Br2 |
H2O, OH |
|
|
H2O |
|
|
|
Br |
Br |
Сульфирование. Анилин при взаимодействии с концентрированной серной кислотой превращается в гидросульфат фениламмония, который при нагревании до 200О С в результате электрофильного сульфирования превращается в пара-аминобензолсульфокислоту, или
сульфаниловую кислоту.
NH2 |
NH3 HSO4 |
NH2 |
H2SO4 |
|
200oC |
|
|
_H O |
|
|
2 |
|
|
SO3H |
Нитрование. Нитрование ароматических соединения обычно осуществляют смесью концентрированных азотной и серной кислот. Анилин в такой смеси существует практически полностью в виде соли фениламмония, поэтому его нитрование, если и происходит, то идет очень медленно и приводит к продукту мета-замещения. Однако при этом взаимодействии весьма существенными оказываются процессы деструктивного окисления анилина, что бывает заметно по обильному выделению оксидов азота. Поэтому нитрование анилина производят, предварительно «защитив» аминогруппу от воздействия кислой среды и окислителя ацетильной группой, которая резко понижает основность атома азота и предотвращает протонирование и окисление. После нитрования в обычных условиях образующийся как основной продукт пара-нитроацетанилид гидролизуют в кислой или щелочной среде до пара- нитроанилина.
NH2 |
NHCOCH |
NHCOCH |
NH2 |
|
3 |
3 |
|
|
(CH3CO)2O |
HNO3 |
H2O, OH |
|
|
H2SO4 |
|
|
|
NO2 |
NO2 |
2.3.2. Превращения первичных ароматических аминов через соли арилдиазония
Соли арилдиазония, которые легко получаются из первичных ароматических аминов реакцией диазотирования, являются чрезвычайно реакционноспособными соединениями. Их химические свойства используются для введения в бензольное кольцо различных функциональных групп.
Реакции, в которые вступают соли арилдиазония, разделяют на два типа: а) с выделением азота и б) без выделения азота.
а) Реакции солей арилдиазония с выделением азота.
www.mitht.ru/e-library
34
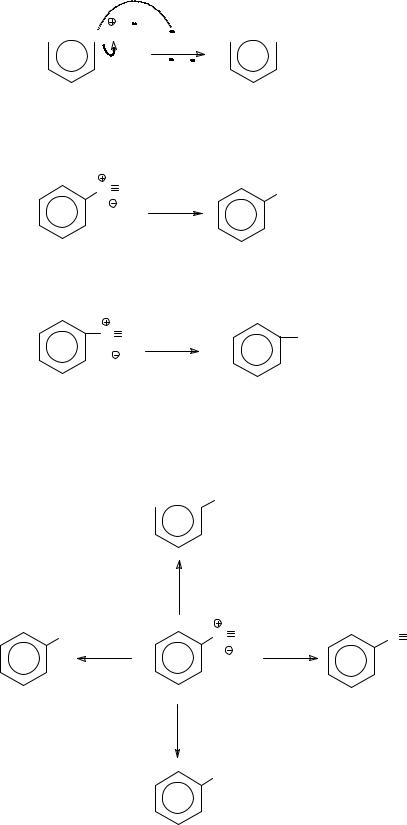
Эти превращения представляют собой реакции нуклеофильного замещения, при которых вместо уходящей в виде молекулы азота диазониевой группы в бензольное кольцо вводится нуклеофильная частица.

 N
N N Z
N Z





 Z
Z
_N









 N
N
Нагревание водных растворов солей арилдиазония приводит к замещению диазониевой группы на гидроксил с образованием фенолов.
N N |
OH |
|
X |
H2O, t |
|
_N2, |
||
|
||
|
_HX |
Замещение диазониевой группы на иод при взаимодействии с раствором иодида калия:
N N |
KI, t |
I |
Cl |
-N2 |
|
Замещение диазониевой группы на хлор, бром, цианогруппу или нитрогруппу при взаимодействии с соответствующими солями меди (I) (реакция Зандмейера).
 Cl
Cl
|
хлорбензол |
|
|
_ N |
CuCl |
|
|
2 |
|
|
|
Br |
N N |
CuCN |
C N |
CuBr |
X |
|
|
_ N2 |
_ N2 |
|
|
|
|
||
бромбензол |
|
|
бензонитрил |
_ N |
CuNO2 |
|
|
2 |
|
|
|
|
NO2 |
|
|
нитробензол
www.mitht.ru/e-library
35
Замещение диазониевой группы на фтор при нагревании тетрафторборатов арилдиазония
(реакция Шимана).
N N |
t |
F |
BF4 |
-N ,-BF |
|
|
2 |
3 |
Замещение диазониевой группы на водород при действии фосфорноватистой кислоты.
N N |
H3PO2 |
H |
X |
_N2 |
|
б) Реакции солей арилдиазония без выделения азота
Восстановление до арилгидразинов с помощью сульфита натрия или дихлорида олова в соляной кислоте.
N N H |
NH NH2 фенилгидразин |
X |
|
H : Na2SO3 |
|
SnCl2/HCl |
|
Реакция азосочетания – взаимодействие солей диазония с фенолами и ароматиче-
скими аминами, протекающее как электрофильное замещение, с образованием азосоединений, например, при реакции хлорида фенилдиазония с фенолом образуется 4- гидроксиазобензол.
N N |
+ |
N=N |
Cl |
|
|
OH |
|
|
|
OH |
Аналогично протекает и взаимодействие между хлоридом пара-нитрофенилдиазония и N,N-диметиланилином.
N N |
+ |
|
N N |
Cl |
|
|
|
|
|
|
|
NO2 |
N(CH3)2 |
NO2 |
N(CH3)2 |
4-(N,N-диметиламино)-4´-нитроазобензол
Реакция азосочетания находит широкое применение для синтеза разнообразных азокрасителей. Так, известный кислотно-основный индикатор метилоранж, относящийся к классу азокрасителей, получают из сульфаниловой кислоты и N,N-диметиланилина.
NH2 NaNO2 |
N N |
HCl |
O3S |
HO3S |
www.mitht.ru/e-library
|
|
|
36 |
N N |
NaOH |
|
N N |
|
+ |
|
|
O3S |
N(CH3)2 |
Na O3S |
N(CH3)2 |
метилоранж
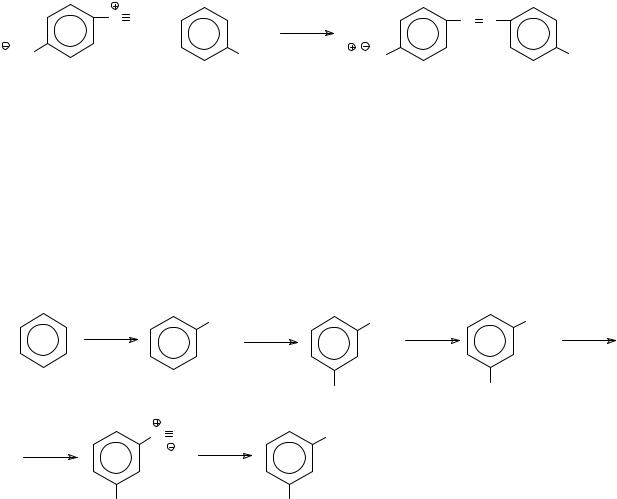
Для иллюстрации использования превращений первичных ароматических аминов в органическом синтезе приведем пример получения мета-дихлорбензола из бензола. Атомы хлора можно было бы вводить в бензольное кольцо электрофильным хлорирование, однако второе хлорирование привело бы в основном к пара- и орто-дихлорбензолам, поскольку атом хлора в хлорбензоле является ориентантом первого рода. Поэтому можно поступить следующим образом. Бензол нитруют смесью концентрированных азотной и серной кислот до нитробензола, который в условиях электрофильного замещения хлорируют до мета- нитрохлорбензола. мета-Нитрохлорбензол восстанавливают, например, сульфидом натрия, полученный мета-хлоранилин диазотируют и соль диазония вводят в реакцию Зандмейера с хлоридом меди (I).
HNO3 |
NO2 |
Cl2 |
NO2 |
NH2 |
|
|
Na2S |
||
H2SO4 |
|
AlCl3 |
|
H2O |
|
|
|
Cl |
Cl |
NaNO2 |
N N CuCl |
|
Cl |
|
HCl |
Cl |
|
|
|
|
|
|
|
Cl Cl
3. Задачи и упражнения
1.Восстановлением каких азотсодержащих соединений можно получить следующие амины: а) метиламин; б) N-метилбензиламин; в) N-этиланилин; г) анилин; д) триэтиламин; е) N,N-диметил-1-пропанамин? Напишите уравнения соответствующих реакций.
2.Алкилированием аммиака получите следующие амины: а) изопропиламин; б) бензиламин; в) 2-метил-1-бутанамин; г) втор-бутиламин; д) аллиламин.
3.Осуществите следующие превращения: а) этилен → этиламин; б) бензол → анилин; в) 1- пропанол → 1-пропанамин; г) пропен → аллиламин; д) 2-бутанон → втор-бутиламин.
4.Используя только этилен в качестве единственного органического соединения и любые неорганические вещества, предложите схему получения триэтиламина.
5.Используя только уксусный альдегид в качестве единственного органического соединения и любые неорганические вещества, предложите схему получения диэтиламина.
6.Сравните основности следующих пар аминов: а) метиламин и диметиламин; б) анилин и метиламин; в) анилин и пара-нитроанилин; г) пара-нитроанилин и пара-толуидин; д) анилин и N-этиланилин.
7.Предложите схемы следующих превращений, используя любые необходимые реагенты: а) нитробензол → Ν-фенилацетамид; б) этиламин → Ν-этилбензиламин; в) этилбромид → иодид тетраэтиламмония; г) анилин → Ν-метил-Ν-фенилбензамид.
8.Напишите уравнения следующих реакций: а) метиламин и уксусный альдегид; б) анилин и бензальдегид; в) бензиламин и ацетон; г) ацетон и диметиламин; д) циклопентанон и метилэтиламин.
www.mitht.ru/e-library

37
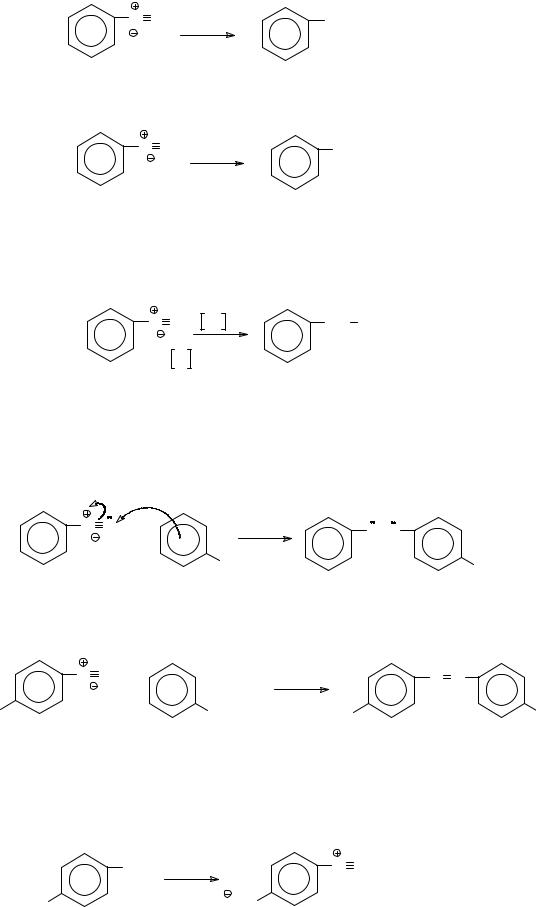
9.Изобразите механизм взаимодействия пара-толуидина с нитритом натрия в избытке соляной кислоты при 5О С.
10.Напишите уравнения реакций следующих аминов с нитритом натрия в соляной кислоте: а) 2-фенил-1-этанамин; б) изопролпиламин; в) N-метиланилин; г) пара-нитроанилин;; д) N,N-диэтиланилин.
11.Используя любые необходимые реагенты, превратите анилин в следующие соединения: а) пара-нитроанилин; б) сульфаниловая кислота; в) пара-бромфенилдиазонийхлорид.
12.Напишите уравнения следующих превращений:
|
|
|
|
Br2 |
D |
NH2 (CH3CO)2O |
HNO3 |
B |
NaOH |
HCl |
E |
A |
C |
||||
|
H2SO4 |
|
H2O |
NaNO2 F |
|
|
|
|
|
||
|
|
|
|
HCl |
|
13.Предложите схемы следующих превращений, используя любые необходимые реагенты и свойства ароматических солей диазония: а) анилин → бензонитрил; б) анилин → пара- нитрофенол; в) бензол → фторбензол; г) анилин → пара-гидроксиазобензол; д) бензол → иодбензол; е) анилин → фенилгидразин.
14.Напишите уравнения реакций азосочетания, с помощью которых можно получиь следующие вещества: а) 4-бром-4’-гидроксиазобензол; б) 4-(Ν,Ν-диметиламино)-2’- хлоразобензол; в) 4-гидрокси-4’-метилазобензол; г) 2,4-дигидрокси-4’-нитроазобензол.
www.mitht.ru/e-library
