
Поведение КС в растворах (билет 32)
.docxБИЛЕТ №32
Поведение комплексных соединений в растворах. Первичная и вторичная диссоциация. Константа нестойкости. Образование и разрушение комплексных соединений.
Поведение КС в растворах.
Для растворов комплексных соединений характерно четыре вида равновесий:
а) диссоциация на комплексный и внешнесферный ионы;
б) диссоциация комплексного иона (или замещение лигандов молекулами растворителя);
в) диссоциация лигандов;
г) окислительно-восстановительное равновесие (в случае, когда атом комплексообразователь проявляет переменную валентность).
Ниже приводятся схемы этих видов равновесий:
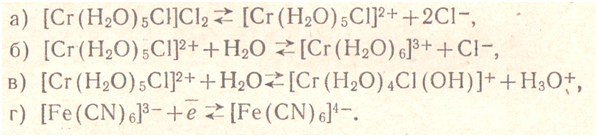
1. Ионные равновесия
Равновесия диссоциации комплексных соединений на комплексный и внешнесферный ноны называют ионными равновесиями. Ионные равновесия подчиняются закономерностям поведения в растворах сильных электролитов:
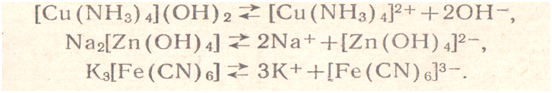
Диссоциации по такой схеме не подвергаются только комплексные соединения — неэлектролиты:
![]()
Химическими методами анализа в растворе легко обнаруживают комплексные и внешнесферные ионы. Составные же части комплексного нона обычными химическими методами анализа не обнаруживаются.
Благодаря ионным равновесиям можно определить природу внешнесферных ионов и количество их в молекуле комплексного соединения.
Диссоциация.
Для комплексных соединений характерна первичная и вторичная диссоциация.
Первичная диссоциация комплексных соединений на комплексный ион и противоположно заряженные ионы внешней сферы протекает полностью, как у сильных электролитов.
K2[Zn(CN)4] = 2K+ +[Zn(CN)4]2-
[Co(NH3)6](NO3)2 = [Co(NH3)6]2+ +2NO3-
Поэтому, соединения, содержащие комплексные ионы, могут вступать в реакции обмена с электролитами с образованием малорастворимых веществ.
2CuSO4
+ K4[Fe(CN)6]
= Cu2[Fe(CN)6]
+ 2K2SO4;
2Cu2+
+ [Fe(CN)6]4-
= Cu2[Fe(CN)6]
Однако, в отличие от “простых” ионов, комплексные ионы сами способны к диссоциации, которая называется вторичной диссоциацией. Она характеризует диссоциацию самого комплексного иона и протекает ступенчато, как у слабых электролитов, подчиняясь закону действия масс. Количественно каждая ступень характеризуется константой диссоциации.
I ступень: [Ag(NH3)2]+ = [AgNH3]+ +NH3
[AgNH3]+ [NH3]
Кд(I) =
[Ag(NH3)2]+
II ступень: [AgNH3]+ = Ag+ + NH3
[Ag+] [NH3]
Кд(II) =
[AgNH3]+
В целом устойчивость комплексного иона в растворе характеризуется величиной константы нестойкости Кн , обратная константе устойчивости:
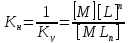
где M – центральный атом или ион; L – лиганд.
Общая константа нестойкости Кн является константой равновесия полной диссоциации комплекса:
[Ag(NH3)2]+ = Ag+ + 2NH3
[Ag+] [NH3]2
Kд=
[Ag(NH3)2]+
Чем меньше константа нестойкости, тем прочнее комплексный ион.
Комплексные соединения, в частности соли, очень сходны с двойными солями.
Отличаются комплексные соли от двойных прежде всего величиной константы нестойкости: у типичных двойных солей константа нестойкости очень велика, у типичных комплексных солей она, наоборот, очень мала.
Образование и разрушение комплексных соединений.
Образование и разрушение комплекса объясняется смещением равновесия его диссоциации и объясняется принципом Ле Шателье. Равновесие диссоциации иона [Ag(NH3)2]+ = Ag+ + 2NH3 смещается в сторону образования комплекса (влево) при увеличении концентрации ионов Ag+ и NH3. При этом образуются соединения, в которых центральный атом или лиганд связаны более прочно, чем в исходном комплексе. Многие комплексные соединения хорошо растворимы в воде, поэтому комплексообразование используется для перевода в раствор труднорастворимых соединений.
Хлорид серебра растворяется в избытке цианида калия:
AgCl + 2KCN = K[Ag(CN)2] + KCl
AgCl + 2CN- = [Ag(CN)2]- + Cl-
Это связано с тем, что ион серебра в ионе [Ag(CN)2]- связан более прочно, чем в AgCl.



AgCl = Cl- + Ag+ + 2CN = [Ag(CN)2]-
ПР(AgCl) = 5∙10-8 Кн[Ag(CN)2]- = 1∙10-21
При
избытке CN-

При добавлении азотной кислоты к [Ni(NH3)6]Cl2 происходит разрушение комплекса, о чём свидетельствует изменения окраски раствора. Это связано с образованием катиона аммония, в котором аммиак связан с катионом водорода более прочно, чем с катионом никеля.



[Ni(NH3)6]2+ = Ni2+ + 6NH3 + 6H+ = 6NH4+ + Ni2+
Кн[Ni(NH3)6]2+ = 1∙10-8 Кн[NH4]+ = 6∙10-10
При
избытке Н+

