
химия с 30 по 50
.doc-
Какие функции в организме выполняет витамин В12? Назовите комплексообразователь в молекуле В12. Что общего в структурах молекул гемоглобина и витамина В12? Общая масса кобальта в организме взрослого человека примерно 1,2 мг, что составляет менее 2∙10-6 %. Около 100 мг из этой массы находится в форме цианокобаламина (жирорастворимый витамин B12) и его аналогов. Это вещество, как и гем, представляет собой макроциклическое комплексной соединение.
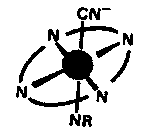 В
качестве макроциклического лиганда
выступает тетрадентатное соединение
— порфин. R
представляет собой сложный органический
заместитель. В аналогах цианокобаламина
вместо аниона СN-
выступают различные органические
заместители.
В
качестве макроциклического лиганда
выступает тетрадентатное соединение
— порфин. R
представляет собой сложный органический
заместитель. В аналогах цианокобаламина
вместо аниона СN-
выступают различные органические
заместители.
Наиболее важную роль витамин В12 играет в развитии и формировании эритроцитов (эритропоэз). Дефицит витамина В12 (поступление менее 3 мкг в сутки) приводит к тяжелому заболеванию — злокачественной анемии (малокровии).
Установлено, что аналоги цианокобаламина являются активаторами — кофакторами различных ферментов, участвующих в эритропоэзе. Недостаток кофакторов проявляется в дефиците гемоглобина и эритроцитов.
-
Опишите биологическую роль йода. К какому заболеванию приводит недостаток йода в пище? Основная биологическая роль йода заключается в синтезе гормонов щитовидной железы (тироксина и трийодтиронина), через которые он и реализует следующие эффекты:
-
стимулирует рост и развитие организма
-
регулирует рост и дифференцировку тканей
-
повышает артериальное давление, а также частоту и силу сердечных сокращений
-
регулирует (увеличивает) скорость протекания многих биохимических реакций
-
регулирует обмен энергии, повышает температуру тела
-
регулирует белковый, жировой, водно-электролитный обмен
-
регулирует обмен витаминов Дефицит йода
-
Увеличение щитовидной железы и формирование эндемического зоба.
-
Нарушение выработки гормонов щитовидной железы.
-
Снижение основного обмена, температуры тела.
У детей – развитие кретинизма, отсталость в физическом и умственном развитии.
32. К каким изменениям в организме приводят дефицит фтора и избыток фтора в окружающей среде и питьевой воде? Как называются возникающие в этих случаях заболевания? Причины дефицита фтора недостаточное поступление с рационом, нарушение обмена Последствия дефицита фтора: повышение риска развития кариеса зубов, повышение риска развития остеопороза .Причины избытка фтора высокое содержание фтора в питьевой воде может присутствовать в соответствующих геохимических провинциях, или рядом с соответствующими производствами (алюминий) передозировка препаратами фтора работа во вредных условиях труда , нарушение обмена Последствия избытка фтора нарушение жирового и углеводного обмена, остеопороз, остеомаляция, образование костных шпор, кальциноз сухожилий и связок, появление пятен на зубах, разрушение зубной эмали, кровоизлияния в области слизистых оболочек рта и носа, сухой удушливый кашель, потеря голоса, брадикардия, снижение давления., зуд кожи, раздражение и слущивание эпидермиса. Суточная потребность во фторе: 4,0 мг. Обогащение питьевой воды фтором, т.е. фторирования воды с целью доведения содержания в ней фтора до нормы (1мг/л), приводит к значительному снижению заболеваемости населения кариесом зубов. Фторирование питьевой воды осуществляется добавлением к ней определенного количества натрия фторида.
33. Из кристаллогидратов солей алюминия в медицинской практике находят применение алюмокалиевые квасцы (сульфат алюминия-калия, кристаллизованный с 12 молекулами воды). Напишите формулу квасцов и укажите, где они применяются в медицинской практике. Из кристаллогидратов солей алюминия в медицинской практике находят применение калий-алюминий сульфат (квасцы алюмокалиевые) КАl(SО4)2∙12Н2О и жженые квасцы КАl(SО4)2, которые получают нагреванием алюмокалиевых квасцов при температуре не выше 433 К. Эти препараты обладают вяжущим действием.
Квасцы применяют для полосканий, промываний и примочек при воспалительных заболеваниях слизистых оболочек и кожи. Кроме того, этот препарат применяют как кровоостанавливающее средство при порезах (свертывающее действие).
Жженые квасцы используют в виде присыпок как вяжущее и высушивающее средство при потливости ног. Осушающее действие связано с тем, что жженые квасцы медленно поглощают воду:
34. Охарактеризуйте токсичное действие оксида углерода (II) на организм человека и теплокровных животных. СО. Это соединение ядовито и чрезвычайно опасно, потому что не имеет запаха.
Оксид углерода (II) — угарный газ — продукт неполного окисления углерода. Как это ни парадоксально, одним из источников СО является сам человек, организм которого производит и выделяет во внешнюю среду (с выдыхаемым воздухом) за сутки около 10мл СО. Это так называемый эндогенный оксид углерода (II), который образуется в процессах кроветворения.
Проникая с воздухом в легкие, оксид углерода (II) быстро проходит через альвеолярно-капиллярную мембрану, растворяется в плазме крови, диффундирует в эритроциты и вступает в обратимое химическое взаимодействие как с окисленным НbО2, так и с восстановленным гемоглобином Нb: НbО2 + СО ⇄ НbСО + О2 Нb + СО ⇄ НbСО
Образующийся карбонилгемоглобин НbСО не способен присоединять к себе кислород. Вследствие этого становится невозможным перенос кислорода от легких к тканям.
Высокое химическое сродство оксида углерода (II) СО к двухвалентному железу является основной причиной взаимодействия СО с гемоглобином. Можно полагать, что и другие бионеорганические соединения, содержащие ионы Fе2+, должны реагировать с этим ядом.
Так как реакция взаимодействия оксигемоглобина с угарным газом обратима, то повышение в дыхательной среде парциального давления О2 будет ускорять диссоциацию карбонилгемоглобина и выделение СО из организма (равновесие смешается влево по принципу Ле Шателье): НbО2 + СО ⇄ НbСО + О2 35. Объясните, почему металлические свойства элементов III-IVA групп выражены слабее, чем у элементов I-IIA групп? По сравнению с s-элементами, имеют большее число валентных электронов и меньший радиус, и поэтому их металлические свойства выражены слабее.
36. Соли тяжелых металлов ускоряют процесс разложения пероксида водорода (Н2О2). Объясните, какое значение этот процесс имеет для организма? Какой фермент способствует утилизации Н2О2 в организме? Главная его химическая функция в организме – окисление веществ, которое всегда сопровождается выделением энергии. Биологическое окисление подразделяют на свободное окисление, при котором выделяющаяся энергия используется для протекания эндэргонических реакций. Для клетки очень важно, чтобы происходила полная утилизация кислорода:
О2 + 4е- + 4Н+ 2Н2О Если этот процесс нарушается, то образуются различные активные формы ки-
слорода: супероксидный анион – радикал .О2 , гидропероксидный радикал НО2 пе-роксид водорода Н2О2, гидроксидный радикал НО. и синглетный кислород .О2, способствующие свободнорадикальному окислению биосубстратов. Защита от вредного действия активных форм кислорода осуществляется
с помощью антиоксидантной системы, в которую входят ферменты супероксиддисмутаза и каталаза.
Под действием СОД супероксидный радикал превращается в О2 и Н2О2,
который разлагается под действием каталазы: 2O2- + 2 H+ СОД H2O2 + O2 2H2O2 H2O + O2
37. Какую роль играют соединения кремния в живом организме? По каким причинам содержание кремния в организме намного меньше, чем углерода?
Дайте обоснованный ответ.
По содержанию в организме человека (10-3 %) кремний относится к примесным микроэлементам. Больше всего кремния в печени, надпочечниках, волосах, хрусталике. Так как природный кремний диоксид плохо растворим в воде, то в организм человека он попадает не столько через пищеварительный тракт, сколько воздушным путем через легкие в виде пылеобразного SiO2:
С нарушением обмена кремния связывают возникновение гипертонии, ревматизма, язвы, малокровия.
Недавно было установлено, что кремний содержится в коже, хрящах, связках млекопитающих и входит в состав мукополи-сахаридов, где прочно связан эфирными связями, возникающими при взаимодействии ортокремниевой кислоты с гидроксильными группами углеводов: В отличие от углерода в составе биомолекул кремний связан только с атомами кислорода (связь Si—О), так как энергия этой связи существенно выше энергии связей Si—Н, Si—С, Si—S и т.д.
В медицинской практике применяют кремний (IV) карбид SiС — карборунд для шлифовки пломб и пластмассовых протезов. Диоксид кремния SiO2 входит в состав силикатных цементов.
Необходимо отметить, что пыль, состоящая из частиц угля, кремния диоксида SiO2, алюминия, при систематическом воздействии на легкие вызывает заболевание — пневмокониозы. При действии угольной пыли — это антракоз — профессиональное заболевание шахтеров. При вдыхании пыли, содержащей SiO2, возникает силикоз, при действии алюминиевой пыли — алюминоз.
38. Ежесуточная потребность в кальции составляет 0,5г, но человек должен потреблять не менее 1г. Объясните, почему? Укажите биороль кальция в организме. Кальций содержится в каждой клетке организма человека. Основная его масса находится в костной и зубной тканях. В среднем взрослый человек должен потребить 1 г кальция в сутки, хотя потребность в кальции только 0,5 г. Это связано с тем, что кальций, вводимый с пищей, всасывается в кишечнике только на 50%. Концентрацию ионов кальция в организме регулируют гормоны.
В крови, лимфе кальций находится как в ионизированном состоянии, так и неионизированном - в соединениях с белками, углеводами и др. Механизм свёртывания крови состоит из ряда этапов, многие из которых зависят от наличия ионизированного кальция. Ионы кальция принимают активное участие в передаче нервных импульсов, сокращения мышц, регуляции работы сердечной мышцы. Основное хранилище кальция в организме - скелет.
39. Пероксид водорода является термодинамически нестабильным соединением. Напишите реакцию его разложения и укажите роль в медицинской практике. пероксид водорода Н2О2, который образуется во всех клетках организма при различных окислительно- восстановительных процессах как побочный продукт метаболизма и сразу же разлагается под влиянием фермента каталазы: 2Н2О2 = 2Н2О + О2↑ в медицине один из изотопов водорода (дейтерий) в качестве меткииспользуется при исследованиях фармакокинетики лекарственных препаратов. Другой изотоп (тритий) применяется в радиоизотопной диагностике, при изучении биохимических реакций метаболизма и др. Пероксид водорода Н2О2 (3%-й раствор); дезинфицирующее средство для промываний и полосканий при воспалительных заболеваниях слизистых оболочек (стоматиты, ангины), для лечения гнойных ран, остановки носовых кровотечений и т. д.
40. Охарактеризуйте биороль калия и укажите области применения его соединений в медицине и жизнедеятельности. 1. Помогает регулировать водный и солевой баланс в жидкости организма на внутриклеточном уровне 2. Активирует ряд ферментов;3. Входит в состав транспортных систем клеточной мембраны; 4. Требуется для нормального функционирования нервных клеток мозга и всего организма. Калий в организме необходим для нормальной деятельности мышц сердца, а также для вывода излишков воды и натрия. Калий в организм должен поступать в количестве примерно 3 -4 г в сутки. Больше всего калия в организм поступает с растительными продуктами, а также с мясом и морской рыбой. Много содержится калия в сухофруктах: курага, изюм, чернослив, примерно 2 г на 100 г продукта. Затем идут бобовые, горох, картофель, яблоки, виноград. Соединения калия применяются в медицине в качестве лекарственных средств (например, калия бромид, калия йодид, калия перманганат). Калия перманганат — сильный окислитель, обладает дезинтоксикационными свойствами, применяется как дезодорирующее, обеззараживающее и антисептическое средство. Калия теллурит применяется как реактив для ранней бактериологической диагностики дифтерии (теллуритовая проба) Калия ацетат обладает диуретическим (мочегонным) действием Калия бромид назначается как успокаивающее средство, препарату свойственно вызывать незначительное замедление сердечного ритма. 41. Опишите, какое влияние оказывают нитраты и нитриты на организм. Доказано, что нитраты малотоксичны. Для взрослого человека смертельная доза нитратов составляет от 8 до 14 г при однократном приеме. Съесть такое количество нитратов – дело почти невозможное. Наш организм производит сам 25-50% нитратов от потребленных в составе продуктов и напитков. Практически все колбасные и готовые мясные изделия содержат нитраты и нитриты (пищевые добавки Е249 – Е252), которые придают им розовый цвет и защищают от порчи. Уже во рту под действием бактерий нитраты превращаются в нитриты и со слюной попадают в желудок. Считают, что основная часть нитритов вступает в реакцию с гемоглобином, окисляя двухвалентное железо гемоглобина до трехвалентного и образуется метгемоглобин (3HbFe2+ + 2NO-2 + 14H+ = 3HbFe3+ + 2NH3 + 4H2O). Таким образом, попадая в кровь, нитриты вызывают кислородную недостаточность. Аналогично действуют неорганические нитраты. Из другой части нитритов образуются не столько канцерогенные нитрозамины, сколько полезнейший для нас оксид азота (II). Нитриты являются дезаминирующими агентами, способствуют окислению аминогрупп нуклеиновых оснований.
42. Охарактеризуйте биороль воды в жизнедеятельности живых организмов. В целом организм человека состоит на 86-50% из воды (86% у новорожденного и 50% в старческом организме).
* В качестве наполнителя - вода поддерживает не только внешнюю форму отдельных органов и внешний вид человека в целом, но и обеспечивает нормальное их функционирование.
* Как универсальный растворитель - вода растворяет питательные вещества для их проникновения в клетку, участвует в химических процессах при пищеварении, а также вымывает продукты жизнедеятельности и выходит из организма через почки и кожу, унося с собой вредные вещества.
* Вода проявляет и терморегулирующие свойства - поддерживает необходимую температуру тела.
* Транспортная функция воды осуществляется
благодаря ее высокому поверхностному
натяжению. 43. Охарактеризуйте биороль натрия в организме и приведите примеры соединений натрия, применяемых в медицине. Биологическая роль натрия
-
поддерживает осмотическое давление и рН среды
-
вместе с калием формирует электрический потенциал мембран клеток, за счет которого передается сигнал в нервных клетках, мышечных клетках и пр.
-
участвует в транспорте через мембраны клеток аминокислот, сахаров, неорганических и органических анионов
-
участвует в переносе оксида углерода в крови
-
усиливает выделение почками различных продуктов метаболизма
-
участвует в гидратации белков и растворении органических кислот
-
участвует в образовании желудочного сока
-
активирует ферменты слюны и поджелудочного сока
1) Гипертонический раствор натрия хлора.
В следствии большого астматического давления обезвоживает клетки и способствует плазмолизу бактерий.
Такой раствор применяют наружно при лечении гнойных ран, воспалительных процессов полости рта и обширных ожогах.
2) Пероксид натрия. Применяют в замкнутых объектах.
3) Натрий гидрокарбонат В водном растворе в результате гидролиза по аниону возникает слабо щелочная среда,которая оказывает антимикробное действие.
Применяют для понижения кислотности и для нейтрализации кислот попавших на кожу. Также его используют как отхаркивающее средство в микстурах.
44. Чем обусловлено большое многообразие соединений углерода в живом организме? Назовите соединения. Какие типы связей образует атом углерода в организме? Между атомами углерода, а также между углеродом и другими элементами образуются прочные химические связи, которые, однако, могут быть разорваны в сравнительно мягких физиологических условиях (эти связи могут быть одинарными, двойными и тройными).Электронное строение и размер атома, среднее значение электроотрицательности объясняют прочность связи С—С и склонность атомов углерода к образованию длинных гомоцепей:
![]()
Благодаря промежуточному значению электроотрицательности углерод образует малополярные связи с жизненноважными элементами — водородом, кислородом, азотом, серой и др.
Молекулы, содержащие С—С-связи, могут иметь линейное, разветвленное и циклическое строение. Различные органические молекулы, содержащие связанные между собой атомы углерода с разнообразными заместителями, образуют громадное число биомолекул
45. Объясните, как влияют стронций и бериллий на костную ткань? Какое заболевание возникает при избытке примеси стронция в организме? В организме животных и человека в больших количествах
накапливается в костной ткани и влияет на процесс костеобразования. Избыток его вызывает ломкость костей, «стронциевый рахит». Причиной является замена кальция костного вещества стронцием. Извлечь стронций из костей практически невозможно. Повышение радиоактивного фона биосферы может вызвать появление в атмосфере продукта деления тяжелых элементов 90Sr.
Оседая в кости, последний облучает костный мозг и нарушает костномозговое кроветворение. Присутствие даже небольшого количества бериллия в окружающей среде приводит к заболеванию — бериллозу (бериллиевый рахит). Ионы Be2+ вытесняют ионы Са2+ из костной ткани, вызывая ее размягчение и подавляют активность многих ферментов, активируемых ионом Mg2+. При отравлении солями бериллия вводят избыток
солей магния, что приводит к восстановлению активности ферментов
46. Охарактеризуйте биологическую роль кислорода в организме. Кислород. По содержанию в организме человека (мас. доля 62%) кислород относится к макроэлементам. Он незаменим и принадлежит к числу важнейших элементов, составляющих основу живых систем, т.е. является органогеном. Кислород входит в состав огромного числа молекул, начиная от простейших и кончая биополимерами. Исключительно велика роль кислорода в процессах жизнедеятельности, так как окисление кислородом питательных веществ — углеводов, белков, жиров — служит источником энергии, необходимой для работы органов и тканей живых организмов. Большинство окислительно-восстановительных реакций в организме протекает при участии кислорода и его активных форм.
Фагоцитарные (защитные) функции организма также связаны с наличием кислорода, и уменьшение содержания кислорода в организме понижает его защитные свойства.
В фагоцитах (клетках, способных захватывать и переваривать посторонние тела) кислород О2 восстанавливается до супероксид-иона О2-. Ион О2- — радикал, инициирующий радикальноцепные процессы окисления инородных органических веществ RН, захваченных фагоцитами.
При недостатке кислорода эти процессы замедляются, и в результате сопротивляемость организма к инфекциям снижается.
У высших кислород проникает в кровь, соединяется с гемоглобином, образуя легко диссоциирующее соединение оксигемоглобин. С потоком крови это соединение поступает в капилляры различных органов. Здесь кислород отщепляется от гемоглобина и через стенки капилляров диффундирует в ткани.
47. Охарактеризуйте биороль углекислого газа, угольной кислоты и ее солей в организме. Диоксид углерода СО2. постоянно образуется в тканях организма в процессе обмена веществ и играет важную роль в регуляции дыхания и кровообращения. Диоксид углерода является физиологическим стимулятором дыхательного центра. Большие концентрации СО2 (свыше 10%) вызывают сильный ацидоз — снижение рН крови, бурную одышку и паралич дыхательного центра. Активированный уголь (карболен) и модифицированные активированные угли широко используются в медицинской практике. Препараты обладают большой поверхностной активностью, способные адсорбировать алкалоиды, соли тяжелых металлов, различные токсины, применяются в гемо- и
лимфосорбции. Соль угольной кислоты – гидрокарбонат натрия NaHCО3 понижает кислотность желудочного сока, а водные растворы используются для полосканий и примочек. Водородкарбонатная буферная система (Н2СО3—НСО3-) служит главной буферной системой плазмы крови, обеспечивающей поддержание кислотно-основного гомеостаза, постоянного значения рН крови порядка 7,4.
48. В состав каких биологически важных веществ входит цинк? Опишите биологическую роль цинка в организме? Обнаружен во всех органах и тканях человека и высших
животных. Наиболее богаты цинком печень, поджелудочная железа и половые железы, гипофиз и надпочечники. Физиологическая функция цинка осуществляется благодаря связи его с ферментноактивными белками. Высокое содержание цинка в эритроцитах объясняется тем, что большая часть его входит в состав угольной ангидразы (карбоангидразы), участвующей в газообмене и тканевом дыхании. Карбоангидраза катализирует реакции:
H2O + CO2 ⇄ H2CO3 ⇄ H+ + HCO-3 OH– + CO2 ⇄ HCO-3
Цинк активирует биосинтез витаминов С и В. Установлено стимулирующее влияние Zn2+ на фагоцитарную активность лейкоцитов. Многие соединения цинка используются как вяжущие, антисептические средства для наружного применения: ZnSO4 ∙ 7H2O –– глазные капли; ZnO — присыпки, мази, пасты при кожных заболеваниях; цинк-инсулин — препарат для лечения сахарного диабета.
49. Охарактеризуйте биологическую роль хлора в организме. Хлор принадлежит к весьма важным биогенным элементам. Анионы хлора С1– активно участвуют в биохимических превращениях: активируют некоторые ферменты, влияют на электропроводность клеточных мембран и т. д. Ионы С1– наряду с ионами Na+ являются основным осмотическим веществом биологических жидкостей (плазмы крови, лимфы, спинномозговой жидкости). Газообразный хлор ядовит. При недостаточной кислотности желудочного сока принимают внутрь
разведенную соляную кислоту (с массовой долей 8%) в каплях и микстурах
(часто вместе с пепсином). Хлорную (белильную) известь СаОСl2 используют в
качестве дезинфицирующего средства.
50. С чем связана токсичность соединений кадмия и ртути для живых организмов? Ответ поясните. Токсичность ртути связана с агглютинацией (склеиванием, слипанием) эритроцитов, ингибированием ферментов.
Например, сулема НgСl2 вызывает изменение размеров, осмотическую хрупкость и снижение деформируемости эритроцитов, которая необходима для их продвижения по капиллярам.
Токсичность кадмия связана с его сродством к нуклеиновым кислотам. В результате его присоединения к ДНК нарушается ее функционирование.
Хроническая интоксикация кадмием и ртутью может нарушить минерализацию костей. Это связано с близостью ионных радиусов. Поэтому токсичные элементы могут замещать кальций. Это приводит к образованию апатита несовершенной структуры вследствие искажения параметров кристаллического компонента костной ткани. В результате снижается прочность костей. Наиболее выражено химическое сродство SН-группам у ртути. Очевидно, это связано с тем, что комплексообразующие свойства ртути выше и она образует более прочные связи с серой. Токсические свойства элементов зависят от той химической формы, в какой они попадают в организм. Наиболее токсичны те формы, которые растворяются в липидах и легко проникают через мембрану в клетку.
