
- •Сборник задач
- •Общая химия:
- •1. Основные классы неорганических соединений. Номенклатура
- •2. Строение атома
- •3. Основные понятия и законы химии
- •3 Моль NaOh1 мольFeCl3
- •0,24 Моль NaOhх мольFeCl3,
- •4. Растворы
- •4.1. Концентрации растворов
- •4.2. Коллигативные свойства растворов
- •4.3. Водородный показатель
- •4.4. Гидролиз
- •4.5. Равновесия в буферных растворах
- •4.6. Равновесия в насыщенных растворах
- •5. Окислительно-восстановительные реакции
- •Приложение 1 Константы диссоциации некоторых слабых кислот и оснований
- •Приложение 2 Константы нестойкости гидроксокомплексов
- •Приложение 3 Произведения растворимости
- •Окончание прил.3
- •Содержание
4.5. Равновесия в буферных растворах
Буферныерастворы – растворы, способные поддерживать определенное значение рН при разбавлении, а также при добавлении некоторых количеств сильной кислоты или щелочи. Буферное действие основано на связывании добавляемых ионов Н+или ОНв молекулы малодиссоциированных соединений.
Различают следующие типы буферных растворов:
Смесь слабой кислоты и ее соли (например, уксусная кислота СН3СООН + ацетат натрияNaCH3COO). При добавлении сильной кислоты к этому раствору анионы соли связывают ионы Н+в молекулы малодиссоциированной уксусной кислоты:
СН3СОО+ Н+СН3СООН.
При добавлении щелочи протекает реакция нейтрализации:
СН3СООН + ОНСН3СОО+ Н2О
и раствор имеет
![]() ,
,
где pKd– показатель константы диссоциации слабой кислоты,pKd= –lgKd;СсиСк– концентрации соли и килоты соответственно, моль/л.
Смесь средней и кислой соли или двух кислых солей слабой многоосновной кислоты (например, Na2CO3+NaHCO3илиNa2HPO4 + NaH2PO4). Анионы кислой соли реагируют подобно слабой кислоте:
![]() ,
(4.22)
,
(4.22)
где СсиСк– концентрации кислой и средней соли соответственно, моль/л.
Кислые соли слабых многоосновных кислот, при добавлении к растворам которых сильных кислот или щелочей, протекают аналогичные реакции:
НСО3+ Н+Н2СО3;
НСО3+ ОНСО3+ Н2О;
![]() ,
,
где pKn– показатель константы диссоциации кислоты по соответствующей ступени.
Смесь слабого основания и его соли (например, NH4OH+ +NH4Cl). Буферное действие основано на реакциях
NH4OH + H+ NH4+ + H2O;
NH4+ + OH NH4OH.
Показатель
![]() ,
,
где pKd– показатель константы диссоциации слабого основания;СсиСосн– концентрации соли и основания соответственно, моль/л.
Соли слабых кислот и слабых оснований (например, NH4CH3COO). Буферное действие обусловлено реакциями
NH4+ + OH NH4OH;
CH3COO + H+ CH3COOH.
Емкостью буферного раствора В называют количество сильной кислоты или щелочи, которое требуется добавить к 1 л раствора для изменения его рН на единицу. Раствор утрачивает буферные свойства при добавлении сильной кислоты или щелочи в количестве, превышающем буферную емкость. Различают буферную емкость раствора по кислоте и по щелочи.
Емкость кислого буфера по щелочи вычисляют по уравнению
![]() .
.
Таким образом,
![]() (4.23)
(4.23)
Из уравнения
![]()
вычислим емкость кислого буфера по кислоте
![]() .
(4.24)
.
(4.24)
Емкости основного буфера по кислоте и по щелочи соответственно
![]()
![]() .
.
Отношение Сс/СкилиСс/Соснвыбирают в пределах 0,1Сс/Ск10. По таблицам констант диссоциации (см. прил.1) подбирают слабую кислоту сpKd = pH (или слабое основание сpKd=pOH). Исходя из заданного рН вычисляют отношение концентрацийСс/Ск(илиСс/Сосн).
Пример 22.Вычислить изменение рН ацетатного буферного раствора, содержащего по 1 моль/л кислоты и соли, после добавления к 1 л раствора 0,1 моль соляной кислоты.
Решение. Вычислим рН данного буферного раствора по формуле (4.22):
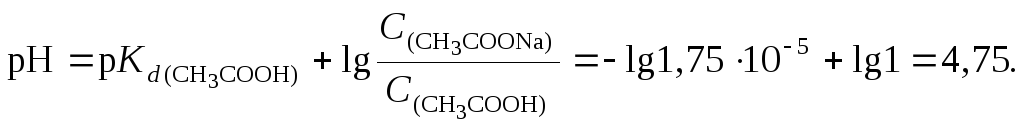
После добавления к буферному раствору соляной кислоты концентрация ацетата натрия уменьшится, а концентрация уксусной кислоты увеличится на 0,1 моль/л вследствие протекания реакции
CH3COONa + HCl CH3COOH + NaCl.
Вычислив для нового раствора

![]()
найдем ΔрН = 4,75 4,66 = 0,09.
Пример 23. К 0,8 л 0,5 М раствора НСООН (Kd = 1,8104) добавили 0,2 л 0,4 М раствора NaOH. Вычислить рН образовавшегося формиатного буфера и его буферную емкость по кислоте и щелочи.
Решение. Количество вещества НСООН и NaOH соответственно
![]()
![]()
Объем буферного раствора
![]()
Количество
вещества формиата натрия, образующегося
по реакции NaOH + HCOOH HCOONa + H2O,
![]()
![]() моль. Молярная концентрация формиата
натрия в буферном растворе
моль. Молярная концентрация формиата
натрия в буферном растворе
![]() моль/л.
моль/л.
Остаточное количество вещества муравьиной кислоты
![]()
![]() .
.
Ее молярная концентрация в буферном растворе
![]() моль/л.
моль/л.
Буферный раствор имеет
![]()
Буферная емкость по кислоте согласно уравнению (4.24)
![]()
Буферную емкость по щелочи определим при помощи уравнения (4.23):
![]()
Пример 24. Сколько граммов твердого формиата натрияHCOONaнадо добавить к 100 мл 0,2 М раствора соляной кислоты, чтобы получить буферный раствор с рН = 4,3?
Решение. При добавлении к раствору соляной кислоты формиата натрия образуется муравьиная кислота по реакцииHCOONa+HClHCOOH+NaCl. Ее концентрация
С(HCOOH) =С(HCl) = 0,2 моль/л.
Для образования формиатного буферного раствора необходима определенная концентрация формиата натрия, которую найдем исходя из формулы (4.22):
![]() ,
,
откуда ![]() моль/л.
моль/л.
Количество вещества формиата натрия, необходимого для получения данного буферного раствора,
![]() моль,
моль,
его масса
![]() г.
г.
Задание XV. Решить задачи.
684. К 200 мл 0,5 н. раствора уксусной кислоты добавили 10 мл 0,8 н. раствора едкого натра. Определить рН полученного раствора.
685. Какой объем 20-процентного раствора уксусной кислоты плотностью 1,026 г/см3следует прилить к 1 л 0,075 н. раствора ацетата натрия, чтобы получить буферный раствор с рН = 2,75?
686. Рассчитать рН раствора, содержащего 1,5 моль/л ацетата натрия и 0,75 моль/л уксусной кислоты. Как изменится величина рН при добавлении к 50 мл этого раствора 1 мл 2 н. раствора едкого натра?
687. Сколько граммов безводного бензойнокислого натрия необходимо прибавить к 100 мл 0,02 моль/л раствора бензойной кислоты С6Н5СООН, чтобы получить буферный раствор с рН = 5?
688. К 25 мл 2-процентного раствора гидроксида аммония плотностью 0,99 г/см3добавили 1,5 г хлорида аммония. Определить рН полученного раствора, если его плотность равна 1,01 г/см3.
689. Как изменится рН в 0,1 н. растворе уксусной кислоты после добавления к нему кристаллического ацетата натрия до концентрации 0,1 моль/л?
690. Как изменится рН раствора, полученного смешиванием 100 мл 5-процентного раствора муравьиной кислоты плотностью 1,008 г/см3 и 100 мл 7-процентного раствора формиата калия плотностью 1,01 г/см3, если к нему прилить 50 мл 0,2 н. раствора едкого калия?
691. Какой объем 20-процентного раствора фосфорной кислоты (плотность 1,113 г/мл) надо добавить к 2 л раствора едкого кали с концентрацией 0,2 моль/л для получения буферного раствора с рН = 6?
692. Как изменится рН раствора, содержащего в 200 мл 2,14 г хлорида аммония и 2,1 г гидроксида аммония, в результате добавления к нему 10 мл 2 н. раствора соляной кислоты?
693. Какой объем раствора гидроксида бария концентрацией 0,5 моль/л следует добавить к 1,5 л 5-процентного раствора уксусной кислоты плотностью 1,006 г/см3, чтобы получить буферный раствор с рН = 4?
694. Рассчитать рН раствора, полученного смешиванием 10 м32-процентного раствора едкого натра (плотность 1,021 г/см3) и 15 м35-процентного раствора фосфорной кислоты (плотность 1,026 г/см3).
695. Какой объем 20-процентной серной кислоты (плотность 1,139 г/мл) необходимо добавить к 5 л раствора этиламина с концентрацией 0,02 моль/л для получения буферного раствора с рН = 9,8?
696. К 5 л 5-процентного раствора гидроксида аммония плотностью 0,986 г/мл добавили 10 л 3-процентного раствора серной кислоты плотностью 1,019 г/мл. Определить рН полученного раствора.
697. Определить рН борно-натриевого буферного раствора (концентрация Н3ВО3иNaH2BO315 и 10 % соответственно, средняя плотность раствора 1,12 г/см3).
698. Рассчитать рН раствора, полученного путем поглощения 20 л углекислого газа 6 л раствора едкого натра с концентрацией 0,1 моль/л. Процесс вели при температуре 25 °С и давлении 1 атм.
699. Определить рН фосфорно-натриевого буфера, если в 1 л раствора содержится 19,6 г фосфорной кислоты и 30 г дигидрофосфата натрия.
700. Объем хлористого водорода, равный 5 м3, был измерен при температуре 100 °С и давлении 1,5 атм. Определить рН раствора, полученного в результате поглощения этого газа 5 м3раствора гидроксида аммония с концентрацией 0,1 моль/л.
701. Рассчитать рН раствора, в 1 л которого содержится 12,5 г ацетата натрия и 17,5 г уксусной кислоты.
702. Какой объем аммиака должен быть поглощен при 25 °С и давлении 1 атм 2-процентным раствором серной кислоты плотностью 1,012 г/мл в количестве 300 мл, чтобы полученный раствор имел рН = 10?
703. Каков рН аммиачно-хлоридного буфера, содержащего в 1 л 70 г гидроксида аммония и 26,7 г хлорида аммония?
704. Какой объем раствора аммиака (концентрация 4,27 %, плотность 0,98 г/см3) надо добавить к 200 мл 0,1 н. раствора соляной кислоты, чтобы получить буферный раствор с рН = 8,24?
705. Рассчитать рН смеси карбоната и гидрокарбоната калия с концентрацией по 0,02 моль/л.
706. Какой объем раствора уксусной кислоты (концентрация 6 %, плотность 1,007 г/см3) следует долить к 100 мл раствора едкого натра (концентрация 0,6 %, плотность 1,005 г/см3), чтобы получить буферный раствор с рН = 4,18?
707. Рассчитать рН раствора дигидрофосфата натрия с концентрацией 1 моль/л.
708. Сколько граммов гипобромита натрия NaBrOследует добавить к 10 л 0,5 н. раствора бромноватистой кислоты, константа диссоциации которой равна 2,06×10-9, чтобы получить буферный раствор с рН = 6,74?
709. Рассчитать рН раствора гидросульфида калия с концентрацией 1 моль/л.
710. Какой объем аммиака должен быть поглощен при 25 °С и давлении 1 атм 2-процентным раствором соляной кислоты (плотность 1,008 г/см3) в количестве 300 мл, чтобы полученный раствор имел значение рН = 10?
711. Каково значение рН аммиачно-хлоридного буфера, содержащего в 1 л 70 г гидроксида аммония и 26,7 г хлорида аммония?
712. Как изменится рН СН3СООН в 0,2 М растворе, если к 100 мл этого раствора прибавили 30 мл 0,3 М раствора ацетата натрия?
713. Рассчитать рН полученного раствора, если к 100 мл 0,0375 М СН3СООН прибавили 0,102 гCH3COONa.
714. Вычислить рН раствора, полученного смешиванием 25 мл 0,2 М СН3СООН и 15 мл 0,1 МCH3COONa.
715. Вычислить рН полученного раствора, если в 1 л воды содержится 60,05 г СН3СООН и 82,03 гCH3COONa.
716. Вычислить рН раствора, если к 2 л воды прибавили 23 г НСООН и 21 г НСООК.
717. Вычислить рН раствора, полученного смешиванием 15 мл 0,1 М НСООН и 12 мл 0,2 М HCOONa.
718. Какой объем 0,2 М NaOHнадо прибавить к 40 мл 0,1 М раствора лимонной кислоты, чтобы получить раствор с рН = 3,0?
719. Какой объем раствора NaOH(концентрация 0,4 %) надо прибавить к 23 мл 0,2 М раствора ортофосфорной кислоты, чтобы получить раствор с рН = 2,3?
720. Какую массу гидроксида натрия надо растворить в 100 мл 0,1 М раствора гидрокарбоната натрия, чтобы получить раствор с рН = 10?
721. Какую массу гидрокарбоната натрия надо растворить в 30 мл раствора гидроксида натрия (концентрация 1 %), чтобы получить раствор с рН = 10,0?
722. Как изменится рН 1-процентного раствора НСООН, если к 230 мл этого раствора прибавить 540 мл раствора НСООKконцентрацией 0,5 %?
723. Сколько миллилитров 0,2 М HClнадо добавить к 50 мл 0,1 МNa2CO3, чтобы получить раствор с рН = 10,5?
