
- •Глава III. Основы молекулярно-кинетической теории
- •§12. Основные понятия и исходные положения
- •§13. Статистический метод исследования систем. Понятие о случайной величине и функции распределения
- •§14. Идеальный газ
- •§15. Основное уравнение молекулярно - кинетической теории
- •15.1. Вывод основного уравнения молекулярно-кинетической теории
- •15.2. Другие формы записи основного уравнения молекулярно-кинетической теории. Абсолютная температура - мера энергии теплового движения молекул
- •§16. Следствия из основного уравнения молекулярно-кинетической теории
- •§17. Распределение молекул по скоростям и кинетической энергии (распределение Максвелла)
- •§18. Барометрическая формула. Распределение молекул в потенциальном силовом поле (распределение Больцмана)
- •§19. Средняя длина свободного пробега молекул. Понятие о физическом вакууме
- •§20. Закон равномерного распределения энергии по степеням свободы
- •§21. Явления переноса в газах
- •21.1. Диффузия
- •21.2. Внутреннее трение (вязкость)
- •21.3. Теплопроводность
21.1. Диффузия
Рис.21.1.
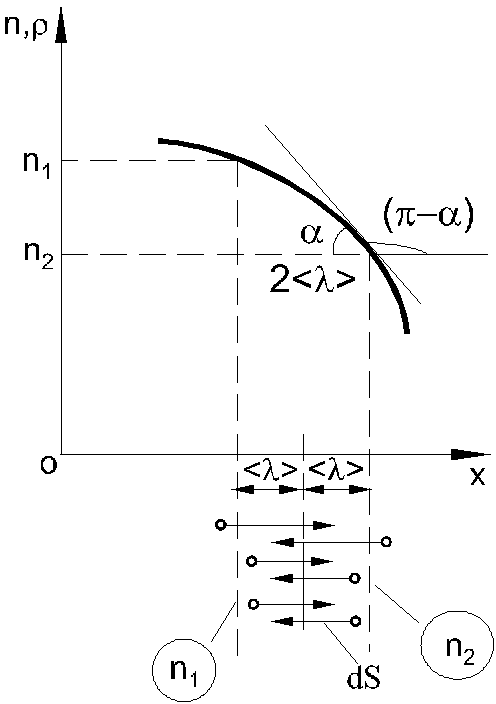
Ограничимся
рассмотрением диффузии газов. Если в
смеси газов концентрация какого-либо
газа распределена по объему сосуда
неравномерно, то возникает перенос
молекул этого газа в места с меньшей
концентрацией - диффузия. Если же в
сосуде находится только один газ,
концентрация которого распределена
неравномерно, то происходит диффузия
молекул газа в своей же среде (этот вид
диффузии иногда называется самодиффузией).
Рассмотрим диффузию химически однородного
газа. Предположим, что плотность газа
изменяется только в направлении оси X
и быстрота этого изменения характеризуется
производной
![]() (рис.21.1).
(рис.21.1).
Экспериментально установлено, что перенос массы газа подчиняется закону Фика:
![]() ,
(21.1)
,
(21.1)
где dM - масса газа, переносимого за время dt через элементарную площадку dS, расположенную перпендикулярно к оси X, вдоль, которой осуществляется перенос; D - коэффициент диффузии, зависящий от природы диффундирующего газа и условий, в которых он находится.
Знак
минус в выражении (21.1) указывает на то,
что перенос массы при диффузии
осуществляется в направлении
убывания
плотности, то есть вдоль положительного
направления оси X
при
![]() и в обратном направлении при
и в обратном направлении при![]() .
.
Используется и другая, более общая форма записи этого закона:
![]() (21.2)
(21.2)
где
![]() -
удельный поток массы, численно равный
массе вещества, которое диффундирует
за единицу времени через плоскую
поверхность единичной площади,
перпендикулярную к направлению переноса.
-
удельный поток массы, численно равный
массе вещества, которое диффундирует
за единицу времени через плоскую
поверхность единичной площади,
перпендикулярную к направлению переноса.
Из выражения (21.1) следует, что коэффициент диффузии численно равен удельному потоку массы при быстроте изменения плотности, равной единице.
Получим выражение для коэффициента диффузии газа с помощью молекулярно-кинетических представлений. Для этого рассчитаем результирующую массу dM молекул, переносимых посредством их хаотического движения через элементарную площадку dS (рис.21.1) по направлению и против направления оси X. Эта масса определяется как
![]() ,
(21.3)
,
(21.3)
где m - масса молекулы, dN1 и dN2 - число переносимых молекул соответственно слева направо и справа налево через площадку dS.
Будем считать, что ввиду хаотичности и равноправности всех направлений движения число молекул, движущихся вдоль одной из координатных осей (X,Y и Z), составляет одну треть имеющихся; следовательно, в положительном и отрицательном направлениях каждой из осей будет двигаться по одной шестой части всех молекул. Предположим, что все молекулы движутся со средней арифметической скоростью <V>. Тогда за время dt до площадки dS долетят все молекулы, движущиеся к ней в одном направлении и заключенные в области пространства объемом <V>dtdS, поэтому можно записать, что
![]() ,
(21.4)
,
(21.4)
![]() ,
(21.5)
,
(21.5)
где n1 и n2 соответственно концентрация молекул слева и справа от площадки dS. Концентрации n1 и n2 следует выбирать на расстоянии от площадки, равном средней длине свободного пробега <>, так как в этом случае все рассматриваемые молекулы долетят до площадки без столкновений.
Подставляя выражения (21.4) и (21.5) в (21.3), получим:
![]() . (21.6)
. (21.6)
В
курсе математики доказывается, что
тангенс угла наклона касательной к
кривой в каждой точке равен производной
от функции в этой точке. Как следует из
рис.
21.1
![]() .
Выразим из прямоугольного треугольника
.
Выразим из прямоугольного треугольника
![]() :
:
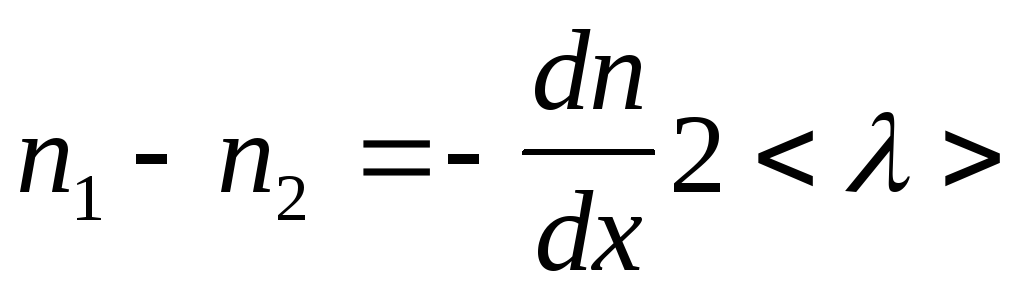 ,
,
где dn/dx градиент концентрации молекул. Учтем также, что
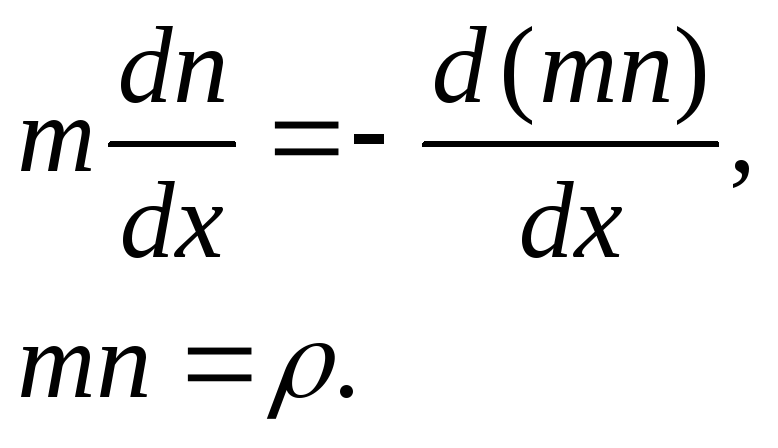
Подставляя полученные выражения в (21.6), получим
![]() .
(21.7)
.
(21.7)
Сравнивая полученное выражение с (21.1), находим для D выражение
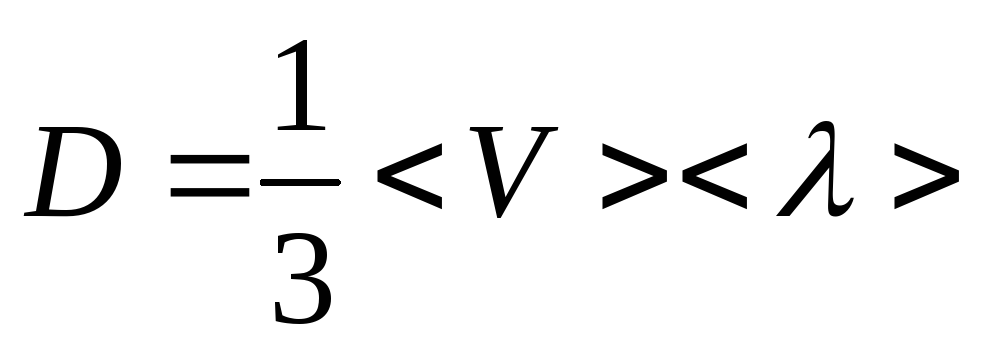 .
(21.8)
.
(21.8)
Подставив в (21.8) выражения (17.7) и (19.4) получим
![]() (21.9)
(21.9)
откуда
можно сделать вывод о том, что диффузия
происходит тем интенсивнее, чем больше
температура газа (так как![]() ),
меньше концентрация или давление газа
(так как
),
меньше концентрация или давление газа
(так как![]() или
или![]() )
и меньше эффективный диаметр молекул
(так как
)
и меньше эффективный диаметр молекул
(так как![]() ).
).
