
Вопросы.
Как влияет на термический КПД степень сжатия и степень расширения рабочего тела при сгорании?
Термический КПД цикла ДВС с изобарным подводом теплоты:
ηt
= [1 - ![]() ]
]
С увеличением степени сжатия и степени расширения термический КПД цикла ДВС с изобарным подводом теплоты уменьшается.
Какие пути повышения термического КПД используются в ДВС?
Верхний предел ε ограничивается в дизелях быстрым увеличением давления. Применяют значения ε = 14~25. В результате совершенствования процессов смесеобразования и горения ρ уменьшается.
Задача №5. Водяной пар с начальным давлением Р1 = 35 бар и начальной степенью сухости х1 = 0,96 расширяется до давления Р2 = 0,4 бар: а) по адиабате; б) по изотерме. Определить параметры: состояний 1 и 2, а также изменение внутренней энергии, работу и тепло процессов. Изобразить процессы в pv-, TS- и hs– диаграммах. Задачу решить, пользуясь hs-диаграммой. Результаты расчёта представить в таблице.
Решение:
Задачу решаем при помощи hs-диаграммы.
а) Расширение пара по адиабате.
Начальное состояние пара – точка 1 – на пресечении изобары Р1 = 3,5 МПа и линии постоянной степени сухости х1 = 0,96.
Параметры состояния в этой точке:
- энтальпия h1 = 2725 кДж/кг;
- удельный объём v1 = 0,052 м3/кг;
- энтропия s1 = 5,9 кДж/(кг·К);
- температура t1 = 242 0С;
- давление Р1 = 3,5 МПа;
-
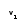




 степень сухости х1
= 0,96.
степень сухости х1
= 0,96.










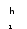










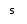


Конечное состояние – точка 2 – на пересечении линии постоянной энтропии s2 = s1 = 5,9 кДж/(кг·К) и изобары Р2 = 0,04 МПа.
Параметры состояния в этой точке:
- энтальпия h2 = 2050 кДж/кг;
- удельный объём v2 = 3,7 м3/кг;
- энтропия s2 = s2 = 5,9 кДж/(кг·К);
- температура t2 = 70 0С;
- давление Р2 = 0,04 МПа;
- степень сухости х2 = 0,744.
Тепло процесса:
Так как процесс адиабатный, q= 0.
Изменение внутренней энергии:
∆u = (h1 – P1·v1) – (h2 – P2·v2) = (2725 – 3,5·103·0,052)-(2050 – 0,04·103·3,7) = =641 кДж/кг.
Работа процесса:
l = ∆u = 641 кДж/кг.
б) Расширение пара по изотерме.


























Конечное состояние – точка 2 – на пересечении линии постоянной температуры t2 = t1 = 242 0С и изобары Р2 = 0,04 МПа.
Параметры состояния в этой точке:
- энтальпия h2 = 2950 кДж/кг;
- удельный объём v2 = 6 м3/кг;
- энтропия s2 = 8,4 кДж/(кг·К);
- температура t2 = t1 = 242 0С;
- давление Р2 = 0,04 МПа.
Тепло процесса:
q = T· (S2 – S1) = (242+273) · (8,4– 5,9) = 1288 кДж/кг.
Изменение внутренней энергии:
∆u = (h1 – P1·v1) – (h2 – P2·v2) = (2725 – 3,5·103·0,052)-(2950 – 0,04·103·6) = =167 кДж/кг.
Работа процесса:
l = q - ∆u = 1288 – 167 = 1121 кДж/кг.
Результаты расчётов сведём в таблицу.
|
процесс |
V1,м3/кг |
V2,м3/кг |
P1, МПа |
P2, МПа |
t1,0C |
t2,0C |
h1, кДж/кг |
h2, кДж/кг |
|
Адиабат- ный |
0,052 |
3,7 |
3,5 |
0,04 |
242 |
70 |
2725 |
2050 |
|
Изотер-мический |
0,052 |
6 |
3,5 |
0,04 |
242 |
242 |
2725 |
2950 |
|
процесс |
S1, кДж/(кг·К) |
S2, кДж/(кг·К) |
q, кДж/кг |
l, кДж/кг |
∆u, кДж/кг |
X1 |
X2 |
|
Адиабат- ный |
5,9 |
5,9 |
0 |
644 |
641 |
0,96 |
0,744 |
|
Изотер-мический |
5,9 |
8,4 |
1288 |
1121 |
167 |
0,96 |
- |
И


 зображение
процессов вpv-,
TS-диаграммах.
зображение
процессов вpv-,
TS-диаграммах.


























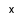





1-2* – адиабатное расширение
1-2 - изотермическое расширение
