
- •Часть 2
- •Общие методические указания
- •Указания к самостоятельной работе с учебными пособиями
- •Указания к решению задач
- •Указания к оформлению и выполнению контрольныхработ
- •Раздел 4. Электродинамика
- •Раздел 5. Оптика
- •Раздел 6. Элементы квантовой механики
- •Раздел 7. Элементы физики твердого тела
- •Раздел 8. Элементы ядерной физики и физики элементарных частиц
- •Краткие теоретические сведения и основные формулы электромагнетизм
- •Волновая оптика
- •Интерференция света
- •Дифракция света
- •Поляризация света
- •Квантовая физика
- •Виды оптических излучений.
- •Тепловое излучение и его характеристики.
- •Законы смещения Вина:
- •1. Длина волны, на которую приходится максимум в спектре излучения черного тела, обратно пропорциональна температуре:
- •Закон Рэлея–Джинса. Исходя из представлений статистической физики о равномерном распределении энергии по степеням свободы, Рэлей и Джинс получили формулу:
- •Фотоэффект.
- •Масса и импульс фотона. Единство корпускулярных и волновых свойств света.
- •Давление света.
- •Эффект Комптона.
- •Линейчатые спектры. Боровская теория атома водорода
- •Волновые свойства частиц. Гипотеза де Бройля
- •Принцип неопределенности
- •Волновая функция.
- •Квадрат волновой функции имеет смысл плотности вероятности, т.Е. Определяет вероятность нахождения частицы в единичном объёме в окрестностях точки с координатами X,y,z.
- •Уравнение Шредингера
- •Частица в одномерной прямоугольной потенциальной яме с бесконечно высокими стенками.
- •Атом водорода. Квантовые числа.
- •Принцип Паули
- •Поглощение света веществом. Закон Бугера.
- •Спонтанное и вынужденное излучение
- •Зонная теория твердого тела. Энергетические зоны в кристаллах. Уровень Ферми
- •Уровень Ферми
- •Состав и характеристика атомного ядра
- •Энергия связи
- •Радиоактивность
- •Деление ядер и цепная реакция
- •Ядерный синтез
- •Контрольная работа № 2
Масса и импульс фотона. Единство корпускулярных и волновых свойств света.
Используя
соотношения
![]() ,
получаем выражение дляэнергии,
массы и
импульса
фотона
,
получаем выражение дляэнергии,
массы и
импульса
фотона
![]()
![]()
![]() (81)
(81)
Эти соотношения связывают квантовые (корпускулярные) характеристики фотона – массу, импульс и энергию – с волновой характеристикой света – его частотой.
Свет обладает одновременно волновыми свойствами, которые проявляются в закономерностях его распространения, интерференции, дифракции, поляризации, и корпускулярными, которые проявляются в процессах взаимодействия света с веществом (испускания, поглощения, рассеяния).
Давление света.
Если фотоны обладают импульсом, то свет, падающий на тело, должен оказывать на него давление.
Пусть
поток монохроматического излучения
частоты v
падает перпендикулярно
поверхности. Если за 1с на 1м2
поверхности тела падает N
фотонов, то
при коэффициенте отражения p
света от
поверхности тела отразится pN
фотонов, а (1-p)N
фотонов — поглотится. Каждый
поглощенный фотон
передает
поверхности импульс
![]() ,а
каждый отраженный фотон -
,а
каждый отраженный фотон -
![]() .
Давление
света на поверхность равно импульсу,
который передают
поверхности
за 1с N фотонов:
.
Давление
света на поверхность равно импульсу,
который передают
поверхности
за 1с N фотонов:
![]() (82)
(82)
Энергетическая
освещенность поверхности:
![]() (энергия всех
фотонов, падающих на единицу поверхности
в единицу времени). Объемнаяплотность энергии
излучения:
(энергия всех
фотонов, падающих на единицу поверхности
в единицу времени). Объемнаяплотность энергии
излучения:
![]() .
Отсюда:
.
Отсюда:
![]() (83)
(83)
Эффект Комптона.
![]() -излучений)на свободных (или слабосвязанных)
электронах вещества, сопровождающееся
увеличением длины волны.
-излучений)на свободных (или слабосвязанных)
электронах вещества, сопровождающееся
увеличением длины волны.
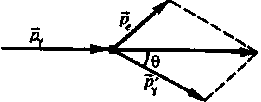
На рис. 22 изображёны
импульсы падающего γ-фотона
![]() ,
рассеянного после столкновения с
электроном
,
рассеянного после столкновения с
электроном![]() и
импульс электрона
и
импульс электрона![]() .Увеличение
.Увеличение
![]() не
зависит от длины волны
не
зависит от длины волны
![]() Рис. 22.падающегоизлучения
иприродырассеивающего
вещества, а определяется только
углом рассеяния
Рис. 22.падающегоизлучения
иприродырассеивающего
вещества, а определяется только
углом рассеяния
![]() :
:
![]() (84)
(84)
где
![]() — длина волны рассеянного излучения,
— длина волны рассеянного излучения,![]() —комптоновская длина волны. При
рассеянии на электроне:
—комптоновская длина волны. При
рассеянии на электроне:
![]() м. (85)
м. (85)
Эффект Комптона, излучение черного тела и фотоэффект служат доказательством квантовых (корпускулярных) представлений о свете.
Линейчатые спектры. Боровская теория атома водорода
Экспериментальные исследования спектров излучения отдельных атомов (разреженные газы) показали, что каждому газу присущ свой линейчатый спектр, состоящий из отдельных спектральных линий или групп близко расположенных линий (серий линий). Положение линий в спектре может быть описано простыми эмпирическим формулами. Так, положение серий линий атома водорода описывается обобщённой формулой Бальмера:
![]() ,
(86)
,
(86)
где ν - частота
спектральных линий в спектре, R-постоянная
Ридберга (![]() ),m = 1,2,3,4.. определяет серию, n= m+1, m+2,
m+3…определяет отдельные линии этой
серии.
),m = 1,2,3,4.. определяет серию, n= m+1, m+2,
m+3…определяет отдельные линии этой
серии.
Аналогичные серии были выделены в линейчатых спектрах других атомов.
Для объяснения закономерностей в линейчатых спектрах Бор объединил планетарную модель атома с гипотезой Планка о квантовом характере излучения.
Постулаты Бора.
Первый постулат Бора(постулат стационарных состояний):
существуют стационарные (не изменяющиеся со временем) состояния атома, находясь в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Каждое стационарное состояние характеризуется определенным (дискретным) значением энергии. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн.
 Бор предположил,
что момент импульса электрона в атоме
также должен принимать только определенные
дискретные значения:
Бор предположил,
что момент импульса электрона в атоме
также должен принимать только определенные
дискретные значения:
L=mvr=nћ,n=1, 2, … , (87)
Второй постулат Бора(правило частот): при переходе атома из одного состояния в другое испускается или поглощается один фотон с энергией
hν=En-Em (88)
равной разности энергий соответствующих стационарных состояний.
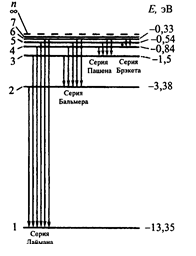
Излучение происходит при переходе атома из состояния с бoльшей энергией в состояние с меньшей энергией (при переходе электрона с орбиты более удаленной от ядра на ближнюю к ядру орбиту). Если же электрон поглощает энергию, он может перейти на более высокий уровень энергии. Можно рассчитать радиусы стационарных орбит электрона, значения энергии и спектральные серии, наблюдаемые в излучении ( Рис.27 )
Рис.27.
![]() –первый боровский
радиус (89)
–первый боровский
радиус (89)
![]() –постоянная
тонкой структуры. (90)
–постоянная
тонкой структуры. (90)
Энергия электрона в атоме водорода:
![]() ,
(91)
,
(91)
где
![]() –энергия
ионизации атома
–энергия
ионизации атома
![]() –постоянная
Ридберга (92)
–постоянная
Ридберга (92)
Энергия, излучаемая или поглощаемая атомом водорода:
![]() ,
,
где n и m – квантовые числа, соответствующие энергетическим уровням, между которыми совершается переход электрона в атоме.
Формула Бальмера для водородоподобных атомов:
![]() ,
(93)
,
(93)
или
![]() ,
(94)
,
(94)
или
![]() ,
(95)
,
(95)
где
![]() – квантовое число, характеризующие
уровни серии, лежащие выше уровня с
квантовым числомn;
– квантовое число, характеризующие
уровни серии, лежащие выше уровня с
квантовым числомn;
Z – заряд ядра.
В опытах Франка и Герцабыло экспериментально доказано
существование в атомах стационарных состояний.
