
- •И. С. Колпащикова, а. Ф. Бетнев, е. М. Алов сборник задач по органической химии
- •1. Указания к выполнению домашней работы
- •2. Алканы
- •2.1. Изомерия
- •2.2. Конформации - изобразить проекции Ньюмена
- •2.3. Строение и температура кипения
- •2.4. Синтез Вюрца
- •2.5. Механизм радикального замещения: Механизм, расчет теплот реакций (2) и (3), медленная стадия – на примере углеводородов, которые в медленной стадии образуют один углеводородный радикал
- •2.6. Галогенирование высших алканов: строение радикалов, образующихся в медленной стадии, сравнение их устойчивости и легкости образования
- •2.7. Расчет процентного состава моногалогензамещенных, образующихся в реакции галогенирования алканов, или сравнение активностей алканов в реакции моногалогенирования
- •2.8. Цепочка превращений (сульфохлорирование, сульфоокисление, нитрование, электролиз, реакция Вюрца, галогенирование алканов
- •3. Алкены
- •3.1. Вывод структурных изомеров
- •3.2. Строение и устойчивость
- •3.3. Механизм электрофильного присоединения
- •3.4. Реакция электрофильного присоединения, протекающая с перегруппировкой
- •3.5. Озонолиз
- •3.6. Полимеризация
- •3.7. Способы получения и химические превращения
- •3.8. Синтез алкенов и их химические превращения
- •3.9. Установление строения соединений по их свойствам
- •3.10. Задача на стехиометрический расчет
- •4. Диены. Алкины
- •4.1. Структурные изомеры диеновых углеводородов
- •4.2. Сравнение длины, энергий, дипольных моментов связей
- •4.3. Электрофильное присоединение к диенам
- •4.4. Полимеризация, озонолиз полимера
- •4.5. Реакция Дильса-Альдера
- •4.6. Свойства алкина как кислоты, реакция с солями более слабых кислот
- •4.7. Реакция гидратации алкинов
- •4.8. Цепочка химических превращений
- •4.9. Синтез алкинов
- •4.10. Установление строения соединений по их свойствам
- •5. Арены. Гетероциклы
- •5.1. Ароматичность, критерии ароматичности
- •5.2. Механизм электрофильного замещения в ядре
- •5.3. Соединения с различными ориентантами в порядке изменения реакционной способности (4 соединения)
- •5.4. Механизм ориентирующего влияния определенной группы в seAr
- •5.5. Совместное влияние двух групп (согласованная и несогласованная ориентация)
- •5.6. Синтез замещенных аренов на основе бензола
- •5.7. Цепочка химических превращений
- •5.8. Электрофильное замещение в конденсированных многоядерных углеводородах
- •5.9. Физико-химические свойства гетероциклов
- •5.10. Реакции гетероциклов
- •6. Галогеналканы. Галогенарены
- •6.1. Методы синтеза галогеналканов и галогенаренов
- •6.2. Механизм нуклеофильного замещения
- •6.3. Cила нуклеофила
- •6.4. Растворитель
- •6.5. Уходящая группа
- •6.6. Стереохимия
- •6.7. Перегруппировка
- •6.8. Конкурирующие реакции
- •6.9. Элиминирование
- •6.10. Реакционная способность галогенов в соединениях, содержащих группировки
- •6.11. Цепочка химических превращений
- •6.12. Синтез и химические превращения галогеналканов
- •6.13. Реакции нуклеофильного замещения в галогенаренах
- •6.14. Стехиометрический расчет
- •7. Спирты. Фенолы. Простые эфиры
- •7.1. Спирты: строение - температура кипения
- •7.2. Спирты, фенолы: строение – кислотность
- •7.3. Получение спиртов на основе магнийорганических соединений
- •7.4. Гидратация алкенов, гидролиз галогеналканов, гидроборирование
- •7.5. Подбор исходных соединений для получения спиртов магнийорганическим синтезом, окисление спиртов
- •7.6. Превращение в простые эфиры
- •7.7. Превращение в сложные эфиры
- •7.8. Взаимодействие спиртов с галогенводородами
- •7.9. Элиминирование
- •7.10. Установление строения спирта по его химическим свойствам
- •7.11. Реакция Вильямсона
- •7.12. Реакция расщепления простого эфира
- •7.13. Получение фенолов щелочным плавом, гидролизом галогенбензола, кумольный метод
- •7.14. Реакции фенолов в ароматическом ядре и в группе – он
- •7.15. Установление строения фенола по его химическим свойствам
- •8. Карбонильные соединения
- •8.1. Получение ароматических альдегидов и кетонов
- •8.2. Получение алифатических альдегидов и кетонов
- •8.3. Реакция Кучерова, пиролиз солей карбоновых кислот
- •8.4. Подвижность α-водородного атома, нуклеофильное присоединение hcn, спиртов, гидросульфита натрия
- •8.5. Нуклеофильное присоединение производных аммиака, роль катализатора
- •8.6. Альдольная конденсация, другие реакции с участием карбанионов
- •8.7. Альдольная конденсация с участием соединений других классов
- •8.8. Получение спиртов с помощью альдольной конденсации
- •8.9. Реакция Канниццаро
- •8.10. Реакция окисления
- •8.11. Химические свойства карбонильных соединений
- •9. Карбоновые и сульфоновые кислоты
- •9.1. Окисление спиртов, превращение насыщенной кислоты в -амино-, гидрокси-, ненасыщенную или двухосновную кислоту через -галогензамещенную
- •9.2. Синтез карбоновых кислот (магнийорганический и нитрильный синтез)
- •9.3. Алкилирование бензольного ядра и последующее окисление алкилароматического углеводорода
- •9.4. Строение и кислотность
- •9.5. Цепочка химических превращений, свойства кислот и их производных
- •9.6. Механизм реакций этерификации, гидролиза, реакционная способность
- •9.7. Сравнение поведения карбонильной группы карбоновой кислоты и кетона, сравнение реакционной способности ацильного и насыщенного углеродов
- •9.8. Получение и превращение сульфоновой кислоты
- •9.9. Установление строения карбоновой или сульфоновой кислоты
- •10. Амины
- •10.1. Получение алифатических аминов реакцией восстановления нитрилов, алкилированием аммиака и аминов и восстановительным аминированием
- •10.2. Строение и основность
- •10.3. Получение ароматических аминов и их превращение
- •10.4. Превращение аминов в соли диазония и реакции солей диазония с выделением азота
- •10.5. Получение замещенных ароматических соединений на основе солей диазония
- •10.6. Получение азокрасителя
- •10.7. Подбор исходных соединений для синтеза азокрасителя
- •Библиографический список
- •150023, Ярославль, Московский пр., 88
8.3. Реакция Кучерова, пиролиз солей карбоновых кислот
1036. Продукт взаимодействия ацетилена с амидом натрия в жидком аммиаке ввели в реакцию с бромэтаном, а затем провели гидратацию в присутствии солей двухвалентной ртути в растворе серной кислоты. Напишите уравнения реакций.
1037. Исходя из ацетилена и неорганических соединений, получите бутанон.
1038. Получите из 3,4-дибромгексана 3-гексанон.
1039. Из ацетилена и неорганических соединений получите 2-гексанон.
1040. Предложите способ получения бутанона из бромэтана и неорганических соединений.
1041. Используя в качестве исходных соединений ацетилен и пропилен, а также любые неорганические, получите 2-пентанон.
1042. Получите 3-пентанон, используя в качестве исходного соединения: а) пропионовую кислоту; б) 3-бромпентан.
1043. Используя ряд последовательных превращений, получите из 1-пропанола диизопропилкетон.
1044. Используя ряд последовательных превращений, получите из этилена бутанон.
1045. Используя ряд последовательных превращений, получите из хлорэтана 3-пентанон.
1046. Используя ряд последовательных превращений, получите из 1-хлорпропана 4-гептанон.
1047. Используя ряд последовательных превращений, получите из 2-метил-1-хлорпропана 2,6-диметил-4-гептанон.
1048. Используя ряд последовательных превращений, получите из хлористого бензила 1,3-дифенил-2-пропанон.
1049. Используя ряд последовательных превращений, получите из этилена 3-гексанон.
1050. Из н-бутилового спирта получите дибутилкетон.
8.4. Подвижность α-водородного атома, нуклеофильное присоединение hcn, спиртов, гидросульфита натрия
1051. Оптически активный фенил-втор-бутилкетон при стоянии в тяжелой воде D2O, содержащей основание OD, теряет оптическую активность и в -положении кетона появляется дейтерий. Скорость обмена протия на дейтерий равна скорости рацемизации. В растворе С2Н5OD в присутствии этоксида натрия в дифенилнитрометане легко происходит обмен водорода на дейтерий. Дайте объяснения наблюдаемым явлениям.
1052. Наиболее важным кеталем является 2,2-диметоксипропан, получаемый в промышленных условиях реакцией ацетона с метанолом. Напишите уравнение реакции, рассмотрите механизм.
1053. Реакцию образования ацеталей используют в лабораторных синтезах для защиты альдегидной группы. Глицериновый альдегид получают из ацеталя акролеина СН2=СН-СНО (почему не из самого акролеина?). Покажите, как это можно сделать.
1054. 1-Фенилэтанол можно получить реакцией между бензальдегидом и соответствующим магнийорганическим соединением. Чтобы удалить небольшое количество непрореагировавшего бензальдегида, продукт встряхивают с водным раствором гидросульфита натрия. Напишите уравнения реакций. Как можно выделить непрореагировавший альдегид?
1055. Предложите механизм следующего превращения:

1056. Спектроскопический анализ водного раствора 4-гидроксибутаналя позволяет обнаружить только 6 % ожидаемых альдегидных групп. Чем это объяснить? В какой форме находятся остальные альдегидные группы?
1057. Предложите механизм следующей реакции:
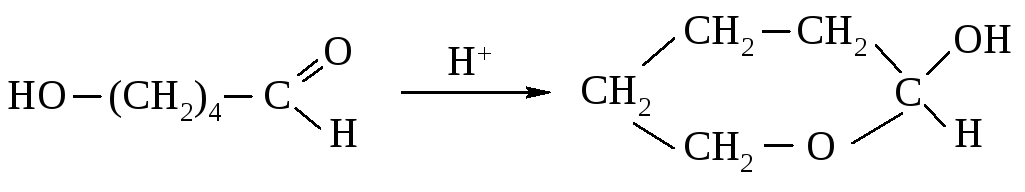
1058. Винилалкиловые эфиры R-CH=CH-OR1 очень быстро гидролизуются разбавленными водными кислотами с образованием спирта HOR1 и альдегида RCH2CHO. Гидролиз в H218O дает спирт H-OR1, не содержащий 18O. Укажите все стадии наиболее вероятного механизма гидролиза. Покажите, как этот механизм объясняет результаты опыта с изотопной меткой и необычайную легкость, с которой протекает этот гидролиз.
1059. При взаимодействии брома с ацетоном в присутствии основания образуется бромацетон, в котором последующее замещение водородов при данном атоме углерода происходит быстрее, чем первого (почему?). Образующийся тригалогенид легко атакуется основанием (галоформная реакция).
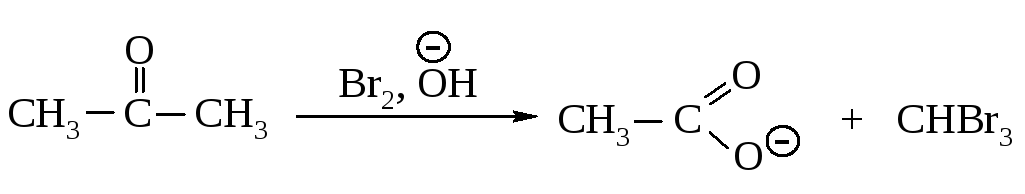
Рассмотрите механизм реакций.
1060. Основным компонентом водного раствора глутарового альдегида является циклический гидрат:
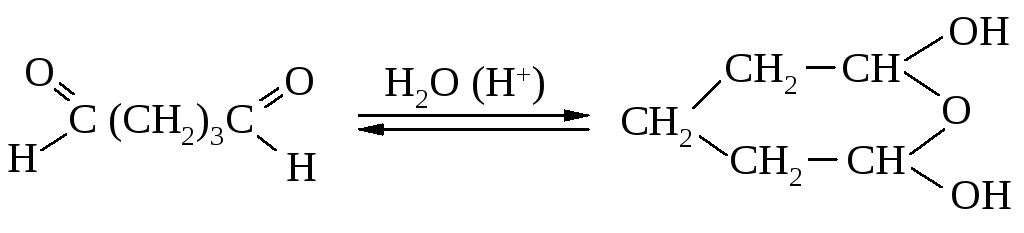
Рассмотрите механизм прямой и обратной реакций.
1061. 2,2-диметоксипропан, который можно рассматривать как простой эфир, быстро гидролизуется до метанола и ацетона в водном растворе кислоты, а диэтиловый эфир устойчив в этих условиях. Напишите механизм кислотного гидролиза 2,2-диметоксипропана и объясните это различие.
1062. Напишите уравнения реакций, назовите полученные соединения. Рассмотрите механизм реакции (б).
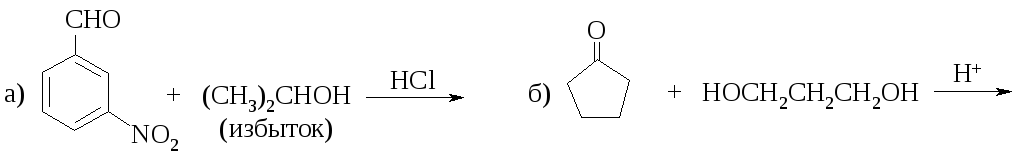
1063. Приведены относительные активности карбонильных соединений в реакции с цианидом калия в присутствии минеральной кислоты.
|
Карбонильное соединение |
Относительная активность |
|
Бензойный альдегид |
7 |
|
п-Толуиловый альдегид |
1 |
Рассмотрите механизм реакции. Объясните изменение реакционной способности этих соединений в реакции с КCN.
1064. Предложите возможный механизм для следующего превращения:
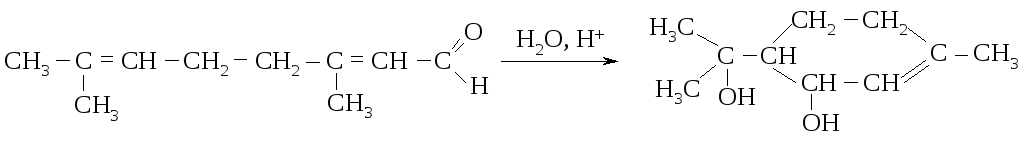
1065. Как реагируют масляный альдегид и бутанон с гидросульфитом натрия NaHSO3? Напишите схемы реакций. Назовите продукты реакции. Приведите механизм. Почему диизопропилкетон практически не взаимодействует с гидросульфитом натрия? Как эта реакция используется для очистки и выделения альдегидов и некоторых (каких?) кетонов из смесей?
