
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ

АРЕНЫ
Электрофильное замещение в ароматическом ядре
HNO 3+ H2SO4 ( NO 2 ) |
|
NO 2 |
Нитрование |
|
|
|
Нитробензол |
|
Cl2, FeCl 3 (Cl...Cl-FeCl 3) |
Cl |
|
Галогенирование |
|
|
|
Хлорбензол |
|
H2SO4 ( SO3) |
|
SO3H |
Сульфирование |
|
|
Бензолсульфоновая |
||
RCl, AlCl 3; ROH, H; |
кислота |
|
|
R |
|
RCH=CH 2, H; (R 1) |
|
|
Алкилирование |
|
|
RCOCl или (RCO) 2O |
Алкилбензол |
|
|
COR |
|
AlCl 3 (RC=O) |
|
|
|
|
|
Ацилирование |
|
|
|
Алкилфенилкетон |
|

АРЕНЫ
Электрофильное замещение в ароматическом ядре
Реакции электрофильного замещения в ароматическом ряду представляют собой двухстадийный процесс присоединения- отщепления
|
+ |
E + |
быстро |
E + |
|
|
быстро |
||||
|
|
|
-комплeкс |
||
|
|
|
|
|
|
|
|
|
|
|
H |
|
E + |
|
|
+ |
E |
|
|
мeдлeнно |
-комплeкс |
||
|
H |
|
|
|
E |
|
|
|
|
|
|
+ |
E + :B |
|
|
+ H-B |
|

АРЕНЫ
Электрофильное замещение в ароматическом ядре
Положительно заряженный электрофильный реагент или электрофил атакует доступное - электронное облако
бензола, вытягивая из него пару электронов.
+ E + |
áû ñòðî |
|
+ |
áû ñòðî |
E |
||
|
-êî ì ï ëeêñ |
|
|
|
|
|

АРЕНЫ
Электрофильное замещение в ароматическом ядре
За счет этой пары электронов и происходит присоединение электрофила к атому углерода с образованием - связи.
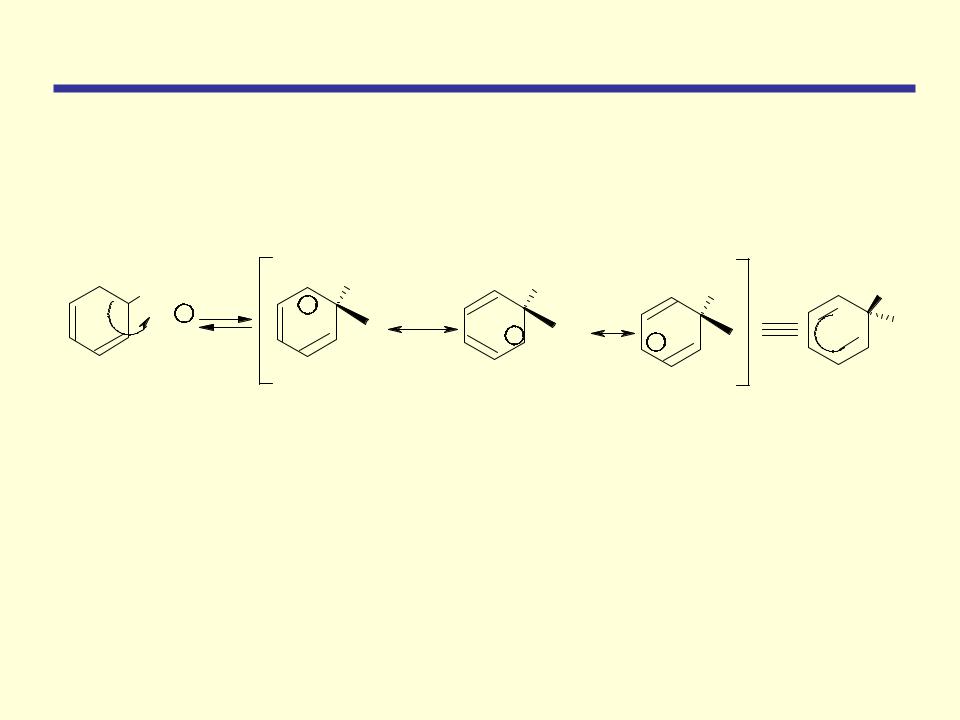
Атакуемый атом углерода переходит из sp2- гибридного состояния в sp3- гибридное состояние. При этом возникает карбокатион, называемый также -комплексом
|
|
H |
E + |
+ |
E |
ì eäëeí í î |
-êî ì ï ëeêñ |
|
АРЕНЫ
Электрофильное замещение в ароматическом ядре
Строение карбокатиона должно быть изображено гибридом трех граничных структур, которые отличаются только распределением электронов
.. H |
|
H |
|
H |
|
H |
|
H |
+ |
|
|
|
|
|
|||
E |
|
E |
|
|
|
E |
||
E + |
|
+ |
+ |
E |
|
|||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Четыре - электрона распределены между пятью атомами
углерода, находящимися в sp2- гибридном состоянии, положительный заряд не локализован на одном атоме углерода, а распределен между двумя орто-углеродными и одним пара-углеродным атомами относительно sp3- гибридизованного атома углерода. Распределение положительного заряда между несколькими атомами углерода делает карбокатион более устойчивым, именно благодаря такой стабилизации возможно образование карбокатиона из очень устойчивой молекулы бензола

АРЕНЫ
Электрофильное замещение в ароматическом ядре
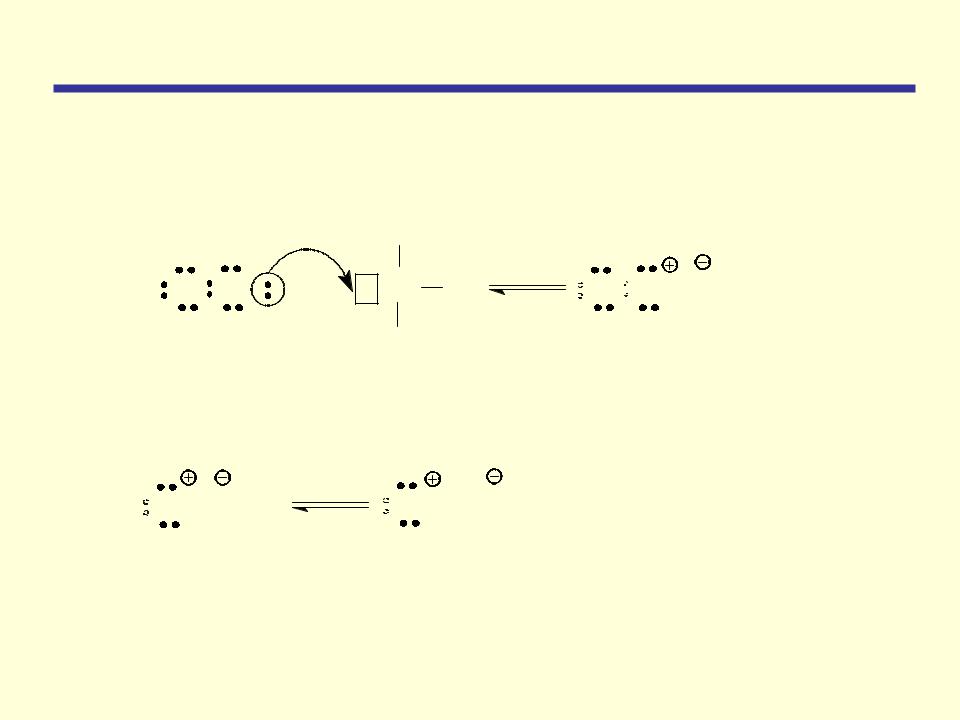
Первая стадия электрофильного замещения в ароматическом ядре подобна первой стадии электрофильного присоединения к алкенам. Но на второй быстрой стадии реакции происходит не присоединение нуклеофила, как в реакции электрофильного присоединения алкенов
|
|
|
H |
|
|
|
|
E + :B |
|
+ |
|
|||
|
|
|
||
|
|
|
|
|
|
||||
|
|
|
|
|
нуклeофильноe
присоeдинeниe
H

 E
E
H
B
а отщепление протона от sp3- гибридизованного атома углерода сопряженным анионом электрофила
|
H |
E |
|
|
|
+ |
E + :B |
+ H-B |

АРЕНЫ
Электрофильное замещение в ароматическом ядре
Это направление реакции имеет более низкую энергию активации (Е2< Е21), так как сопровождается образованием более устойчивого шести- -электронного секстета
E
|
|
|
|
H |
:B |
|
|
|
|
||||
|
|
|
|
|
E |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
E2 |
E2' |
|
E+ |
|
|
|
E |
||
|
|
|
|
|
H |
|
+ |
|
|
|
|
|
H |
:B |
Е1 |
|
|
|
|
B |
|
|
|
|
|
|
E |
|
|
|
|
|
|
HB |
|
медленная стадия |
|
|
|
|
|
|
|
|
|
|
|
быстраястадия |
|
|
|
|
|
|
координата реакции |
АРЕНЫ
Галогенирование
При галогенировании электрофил образуется в реакции галогена
с катализатором - кислотой Льюиса (AlCl3, FeCl3 и др)
Cl
Cl |
Cl |
Al |
Cl |
Cl донор 2е- акцептор 2е- основание кислота
Льюиса Льюиса

 Cl
Cl

 Cl - AlCl3
Cl - AlCl3 

ДАК
 Cl - AlCl4
Cl - AlCl4
ионная пара

 Cl + AlCl4
Cl + AlCl4
Комплексообразование с кислотой Льиса ведет к появлению частиного или целого положительного заряда на одном из атомов в молекуле хлора

АРЕНЫ
Галогенирование
Прямое фторирование является исключительно активным процессом и трудным для контроля. Иодирование проводят в присутствии окислителя. В этих условиях генерируется иодоний-ионы, которые и выступают в качестве электрофильных агентов
HNO3 
 I + I 2
I + I 2 

АРЕНЫ
Нитрование
Нитрование проводится нитрующей смесью - смесью азотной и серной кислот. Образование электрофильной реагента - нитроний-катиона NO2 + - происходит в реакции между азотной и
серной кислотами
O |
+ |
OH + |
H |
O |
SO |
OH |
O + |
+ |
_ |
OSO2OH |
_ O |
N |
N |
O H + |
|
||||||
|
|
|
|
2 |
|
_O |
H |
|
|
|
|
|
|
|
|
|
|
протонированная |
|
|
|
|
|
|
|
|
|
|
азотная кислота |
|
|
|
O + |
+ |
N |
O H |
_ O |
H |
протонированная |
|
азотная кислота |
|
+

 O N O + H2O электрофил катион нитрония
O N O + H2O электрофил катион нитрония
