
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
- •АРЕНЫ
АРЕНЫ
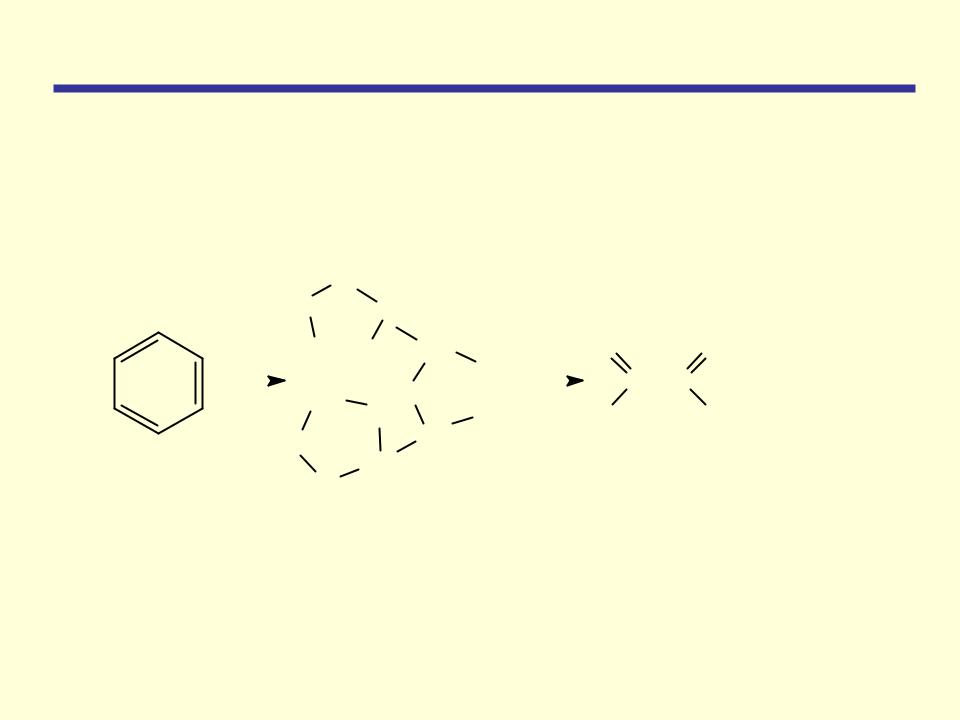
Реакции окисления
Озон действует на ароматическое ядро так же, как на углеводороды с двойными связями
|
O O |
CH |
|
|
|
|
|
|
|
|
||
3O3 |
|
CH |
|
O |
CH |
O |
3H O |
O |
|
O |
||
|
||||||||||||
|
|
|
|
|
||||||||
|
|
|
|
O O |
|
2 |
3 C |
|
C + 3Zn(OH) 2 |
|||
|
|
|
|
|
|
|
|
3Zn |
|
|||
|
CH |
|
|
|
|
|||||||
|
CH |
O |
|
H |
|
H |
||||||
|
O |
CH |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||||
|
|
O |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||

АРЕНЫ
Реакции окисления
Сильные неорганические окислители (KMnO4, K2Cr2O7 + H2SO4)
окисляют боковые цепи алкилароматических соединений до карбоксильных групп, связанных непосредственно с ароматическим кольцом
CH 2СH(CH 3)2 |
|
COOK |
COOH |
KMnO , 100 oC |
HCl |
|
|
4 |
|
|
|
CO2, H2O |
|
KCl |
|
1-Фенил- |
Бензоат калия |
Бензойная кислота |
|
-2-метилпропан

АРЕНЫ
Реакции окисления
Окисление бензола молекулярным кислородом
|
|
|
|
|
O |
|
O2, V2O5 HC |
C |
O Малеиновый |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
~400 OC HC |
C |
ангидрид |
||||
O

АРЕНЫ
Методы синтеза аренов
1. Ароматизация алканов
Процесс превращения алканов в арены называется дегидроциклизацией, т.к. одновременно включает в себя две реакции: замыкание в цикл линейного углеводорода и отщепление водорода
|
CH3 |
|
|
|
|
CH3 |
||||
|
|
|
|
|
|
|
||||
|
CH2 |
CH3 |
Cr2O3/Al2O3 |
|
|
|
|
|||
CH2 |
|
|
|
+ 4H2 |
||||||
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
500 oC |
|
|
|
||
CH2 |
CH2 |
|
|
|
||||||
|
|
|
|
|||||||
|
CH2 |
|
|
|
|
|
|
|
|
|
н-Гептан |
|
|
Толуол |
|||||||

АРЕНЫ
Методы синтеза аренов
2. Реакция Вюрца – Фиттига
При взаимодействии галогенаренов с галогеналканами (предпочтительно использовать бромпроизводные) образуются алкилбензолы
Br |
2Na |
CH 2CH 3 |
|
+ BrCH 2CH 3 |
+ 2NaBr |
||
|
|||
Бромбензол |
|
Этилбензол |

АРЕНЫ
Методы синтеза аренов
3. Алкилирование бензола
При действии на бензол алкилирующих агентов (галогеналканов, алкенов, спиртов) в присутствии кислот Льюиса, а также сильных кислот образуется алкилбензол
1) CH3Cl, AlCl 3 |
+ |
|
|
|
|
2) CH2=CH 2, Н |
|
|
|
CH 2CH 3 |
|
3) CH 3CH 2OH, H + |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

АРЕНЫ
Методы синтеза аренов
4. Гидрирование кислородсодержащих соединений ароматического ряда
|
|
|
|
CCH 3 |
H2, Ni, T |
|
|
|
CH 2CH 3 |
||
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||||
O |
|
||||||||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
