
2. Обсуждение результатов
Арилзамещенные тиофены являются антибиотиками, анисептиками, поверхностно-активными веществами и люминофорами.
Целью работы является исследование возможности синтеза нитрила арилзамещенного тиофена и изучение его свойств. Из рассмотренных в литературном обзоре методов синтезаарилзамещенных тиофенов и их производных был выбран наболее оптимальный и селективный метод, основанный на реакции Гриньяра, дегидратации, формилировании по Вильсмайеру-Хааку и конденсации с образованием карбнитрила.
Общая схема синтеза:

На первой стадии был найден лишь один метод синтеза 1-(тиофен-2-ил-)-циклогексанола (1), который реализован на практике. Реактив Гриньяра действует как нуклеофил, атакуя электрофильный атом углерода с образованием углерод — углеродной связи.


В кислой среде происходит дегидратация соединения (1) в результате чего получен 2-(циклогек-1-ен-1ил)-тиофен (2) с выходом 50 %.

Методы синтеза 2-фенилтиофена (3), найденные в литературе, были с низкими выходами и с использованием труднодоступных реактивов. Рассмотрев возможные варианты получения соединения и выбрав оптимальный, нами был использован метод, где в качестве дегидрирующего агента применяется хлоранил.

В результате получен продукт с выходом 51%.
Были найдены методики получения 5-фенилтиофен-2-карбольдегида (4). Среди предложенных в литературе методик синтеза имели место реакции с фосгеном, угарным газом, бороновой кислотой и металлоорганическими катализаторами, которые являются сложными в техническом исполнении и нами был использован классический метод формилирования по Вильсмайеру-Хааку. ДМФА образует комплекс с хлорокисью фосфора, который атакует арилзамещенный тиофен с образованием продукта, гидролизуемого водой в ароматический альдегид.
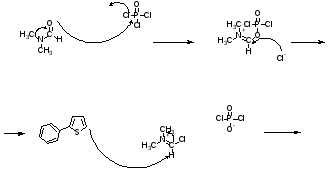

Соединение (4) очищают методом колоночной хроматографии на силикагеле марки «Merсk»-M-60, используя в качестве элюента четыреххлористый углерод. Выход карбальдегида (4) составил 87%. В ИК спектре полученного соединения (4) отмечены характерные полосы поглощения в области 1658ν (C=O) и 1454 ν (С=С).
На последней стадии получен карбонитрил из синтезированного карбальдегида. В литературе предлагаются многоступенчатые способы получения нитрилов, либо с использованием реакции Сузуки, а также реакции с достаточно вредными соединениями. Рассмотрев все варианты и выбрав самый подходящий метод, нами был синтезирован 5-фенилтиофен-2-карбонитрил (5), с использованием солянокислого гидроксиламина, пиридина и пропионового ангидрида. Реакция проходит по следующему механизму:

Соединение (5) очищают методом колоночной хроматографии 48.6 % на силикагеле, используя в качестве элюента четыреххлористый углерод. В ИК спектре полученного соединения (5) отмечены полосы поглощения в области 2218 ν (C≡N) и 1438 ν (С=С).
3. Эксперементальная часть
Реагенты и оборудование
Строение синтезированных соединений подтверждено данными ИК спектров.ИК спектры регистрировались на приборе Shimadzu IRAffinity-1 с использованием в виде таблетки KBr. Контроль за реакцией и индивидуальность соединений устанавливали с помощью ТСХ. Для ТСХ использовались пластинки Sorbfil, для колоночной хроматографии применялся силикагель «Merсk»-М-60. Температура плавления определялась капиллярным методом на приборе ПТП.
|
Название |
Формула |
Молекуляр ная масса |
Тпл. |
Ткип. |
Плотность |
|
2-Бромтиофен |
C4H3BrS |
163 |
- |
151 |
1.684 |
|
Магний |
Mg |
24 |
650 |
1105 |
1.737 |
|
Диэтиловый эфир |
(C2H5)2O |
74 |
-116.3 |
34.6 |
0.714 |
|
Йод |
J2 |
254 |
113.5 |
184.35 |
4.93 |
|
Циклогексанон |
C6H10O |
98 |
-16.4 |
155.7 |
0.9478 |
|
Хлоранил |
C6O2Cl4 |
245.89 |
290 |
- |
1.91 |
|
Бензол |
C6H6 |
78.1 |
5.5 |
80.1 |
0.8786 |
|
Едкий натрий |
NaOH |
40 |
318 |
1388 |
2.13 |
|
ДМФА |
C3H7NO |
73 |
-61 |
153 |
0.9445 |
|
Дихлорэтан |
C2H4Cl2 |
99 |
-35 |
84 |
1.253 |
|
Оксихлорид фосфора |
POCl3 |
151 |
1.18 |
107.2 |
1.65 |
|
Солянокислый гидроксиламин |
NH2OH∙HCl |
69.5 |
151 |
- |
1.67 |
|
пиридин |
C5H5N |
79.1 |
-41.6 |
115 |
0.9819 |
|
Пропионовый ангидрид |
(C2H5CO)2O |
130 |
- |
167 |
1. 0057 |






Синтез целевых продуктов.
