
Основы токсикологии
.pdf

 тиобарбитураты, уретан
тиобарбитураты, уретан
2.Снотворные (седативные) |
Барбитураты, |
хлоралгидрат, талидомид, |
этанол и |
другие |
|
спирты, бром |
|
|
|
|
|
|
|
|
|
|
|
3.Аналгетики |
Морфин и его аналоги |
|
|
|
|
4.Антипиретики |
Салицилаты, фенацетин, хинин |
|
|
||
5.Гормоны |
Эстроген, |
гестаген, |
андроген, |
кортикостероиды, |
|
анаболические стероиды, инсулин |
|
|
|||
|
|
|
|||
6.Химеотерапевтические |
Пенициллин, сульфониламиды, стрептомицин, эритромицин, |
||||
средства |
ПАСК |
|
|
|
|
7.Прочиче |
Иприты, триметиленмеламин, аминоптерин, |
свинец, |
|||
мышьяк, тиоурацил, иод и т.д. |
|
|
|||
|
|
|
|||
После прохождения барьера вещества оказываются в крови плода. Отсюда, в соответствии с общими закономерностями, они распределяются в его органах и тканях. Между взрослым организмом и плодом существует огромная разница в строении и свойствах тканей. Эти особенности лежат в основе иной реакции плода на многие токсиканты (см. ниже).
10. Депонирование
Под депонированием понимают особый вид распределения ксенобиотиков в организме, проявляющийся накоплением, а затем относительным постоянством их содержания в определенном органе или ткани, в течение нескольких суток - многих лет.
Депонирование имеет три основные причины: 1. Активный захват клетками ксенобиотика с последующим его удержанием; 2. Высокое химическое сродство вещества к определенным биомолекулам; 3. Значительная растворимость ксенобиотика в липидах.
Количественные характеристики процесса депонирования существенно зависят от условий, в которых они изучаются и потому носят достаточно относительный (больше/меньше) характер.
10.1. Депонирование вследствие химического сродства и растворимости в липидах
Различные токсиканты могут образовывать с биологическими молекулами ковалентные связи и таким образом накапливаться в тканях. Типичными примерами являются алкилирующие агенты тип ипритов, взаимодействующие с нуклеиновыми кислотами, многие металлы, образующие ковалентные связи с белками и другими лигандами и т.д. Мышьяк вследствие высокого сродства к кератину депонируется в ногтях и волосах. Свинец депонируется в костной ткани. Чрезмерное поступление железа в организм приводит к развитию гемосидероза, который может сохраняться на протяжение всей жизни.
Другой механизм депонирования - накопление липофильных веществ в жировой ткани. Таким образом, в организме в течение многих лет сохраняются полигалогенированные ароматические углеводороды (ПАУ), некоторые хлорорганические инсектициды (ДДТ и т.д.).
Существуют возможности влиять на процесс депонирования путем:
-прекращения поступления вещества в организм;
-усиления механизмов естественного выведения вещества. Так, кальций и свинец распределяются, депонируются и метаболизируют практически идентично. Поэтому фиксированный в костях свинец может быть мобилизован при понижении содержания кальция в крови. Усиление вентиляции легких при ингаляции карбогена усиливает выделение летучих веществ (эфиры и т.д.) и высвобождение их из жировой ткани;
-введения веществ, взаимодействующих с ксенобиотиком. Вещества, имеющие высокое сродство к депонированному агенту, могут вступить с ними во взаимодействие и вывести из места депонирования. Таким способом можно удалить из организма некоторые тяжелые металлы, например свинец, с помощью комплексообразователей (ЭДТА, унитиола и т.д.).
10.2. Депонирование вследствие активного захвата ксенобиотика
Если вещество поступает в клетки против градиента концентрации, то оно может накапливаться в них. Это имеет место в определенных органах и тканях в отношении лишь очень ограниченного количества веществ. Механизм депонирования выявлен для некоторых аналогов биогенных аминов (5-ОН-триптамина, хлорфенилаланина и др.), белковых токсинов (холерного, дифтирийного, столбнячного, ботулотоксина), йода и др.
ОГЛАВЛЕНИЕ/ T4 СТАТЬЯ
М а р т, 2 0 0 3 г.
С. А. КУЦЕНКО ОСНОВЫ ТОКСИКОЛОГИИ, Санкт-Петербург, 2002
ГЛАВА 4.4. МЕТАБОЛИЗМ КСЕНОБИОТИКОВ
Многие ксенобиотики, попав в организм, подвергаются биотрансформации и выделяются в виде метаболитов. В основе биотрансформации по большей части лежат энзиматические преобразования молекул. Биологический смысл явления - превращение химического вещества в форму, удобную для выведения из организма, и тем самым, сокращение времени его действия.
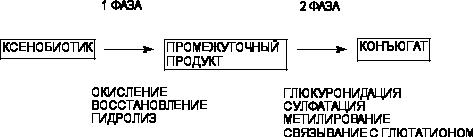
Метаболизм ксенобиотиков проходит в две фазы (рисунок 1).
Рисунок 1. Фазы метаболизма чужеродных соединений
В ходе первой фазы окислительно-восстановительного или гидролитического превращения молекула вещества обогащается полярными функциональными группами, что делает ее реакционно-способной и более растворимой в воде. Во второй фазе проходят синтетические процессы конъюгации промежуточных продуктов метаболизма с эндогенными молекулами, в результате чего образуются полярные соединения, которые выводятся из организма с помощью специальных механизмов экскреции.
Разнообразие каталитических свойств энзимов биотрансформации и их низкая субстратная специфичность позволяет организму метаболизировать вещества самого разного строения. Вместе с тем, у животных разных видов и человека метаболизм ксенобиотиков проходит далеко не одинаково, поскольку энзимы, участвующие в превращениях чужеродных веществ, часто видоспецифичны.
Следствием химической модификации молекулы ксенобиотика могут стать:
1.Ослабление токсичности;
2.Усиление токсичности;
3.Изменение характера токсического действия;

4. Инициация токсического процесса.
Метаболизм многих ксенобиотиков сопровождается образованием продуктов существенно уступающих по токсичности исходным веществам. Так, роданиды, образующиеся в процессе биопревращения цианидов, в несколько сот раз менее токсичны, чем исходные ксенобиотики. Гидролитическое отщепление от молекул зарина, зомана, диизопропилфторфосфата иона фтора, приводит к утрате этими веществами способности угнетать активность ацетилхолинэстеразы и существенному понижению их токсичности. Процесс утраты токсикантом токсичности в результате биотрансформации обозначается как "метаболическая детоксикация".
Впроцессе метаболизма других веществ образуются более токсичные соединения. Примером такого рода превращений является, в частности, образование в организме фторуксусной кислоты при интоксикации фторэтанолом.
Вряде случаев в ходе биотрансформации ксенобиотиков образуются вещества, способные совершенно иначе действовать на организм, чем исходные агенты. Так, некоторые спирты (этиленгликоль), действуя целой молекулой, вызывают седативно-гипнотический эффект (опьянение, наркоз). В ходе их биопревращения образуются соответствующие альдегиды и органические кислоты (щавелевая кислота), способные повреждать паренхиматозные органы и, в частности, почки. Многие низкомолекулярные вещества, являющиеся факультативными аллергенами, подвергаются в организме метаболическим превращениям с образованием реакционноспособных промежуточных продуктов. Так, соединения, содержащие в молекуле аминоили нитрогруппу в ходе метаболизма превращаются в гидроксиламины, активно взаимодействующие с протеинами крови и тканей, формируя полные антигены. При повторном поступлении таких веществ в организм помимо специфического действия развиваются аллергические реакции.
Порой сам процесс метаболизма ксенобиотика является пусковым звеном в развитии интоксикации. Например, в ходе биологического окисления ароматических углеводородов инициируются свободно-радикальные процессы в клетках, образуются ареноксиды, формирующие ковалентные связи с нуклеофильными структурами клеток (белками, сульфгидрильными группами, нуклеиновыми кислотами и т.д), активирующие перекисное окисление липидов биологических мембран (рисунок 2). В итоге инициируется мутагенное, канцерогенное, цитотоксическое действие токсикантов.
Рисунок 2. Образование ареноксидов в процессе метаболизма ароматических полициклических углеводородов при участии оксидаз смешанных функций (ОСФ)
Аналогично ареноксидам на клетки действуют N-оксиды, нитрозамины, гидроксиламины, также являющиеся канцерогенами и мутагенами. В опытах на собаках установлена прямая зависимость между канцерогенной активностью (рак мочевого пузыря) и концентрацией в моче продуктов N-окисления веществ в ряду: 1-нафтиламин, 2-нафтиламин, 4-аминодифенил.
По такому же механизму действуют на организм галогенированный бензол, нафтанол и многие другие ксенобиотики.
Процесс образования токсичных продуктов метаболизма называется "токсификация", а продукты биотрансформации, обладающие высокой токсичностью - токсичными метаболитами. Во многих случаях токсичный метаболит является не стабильным продуктом, подвергающимся дальнейшим превращениям. В этом случае он также называется промежуточным или реактивным метаболитом. Реактивные метаболиты это как раз те вещества, которые часто и вызывают повреждение биосистем на молекулярном уровне. Общим свойством практически всех реактивных метаболитов является их электродефицитное состояние, т.е. высокая

электрофильность. Эти вещества вступают во взаимодействие с богатыми электронами (нуклеофильными) молекулами, повреждая их. К числу последних относятся макромолекулы клеток, в структуру которых входят в большом количестве атомы кислорода, азота, серы. Это, прежде всего, белки и нуклеиновые кислоты. Реактивные метаболиты либо присоединяются к нуклеофильным молекулам, образуя с ними ковалентные связи, либо вызывают их окисление. В обоих случаях структура макромолекул нарушается, следовательно, нарушаются и их функции.
Биоактивация далеко не всегда сопровождается повреждением биосубстрата, поскольку одновременно в организме протекают процессы детоксикации и репарации. Интенсивность этих процессов может быть достаточной для компенсации ущерба, связанного с образованием реактивных метаболитов. Тем не менее при введении высоких доз токсиканта, повторном воздействии защитные механизмы могут оказаться несостоятельными, что и приведет к развитию токсического процесса.
1. Концепция l и ll фазы метаболизма ксенобиотиков
l фаза метаболизма в широком смысле может быть определена, как этап биотрансформации, в ходе которого к молекуле соединения либо присоединяются полярные функциональные группы, либо осуществляется экспрессия таких групп, находящихся в субстрате в скрытой форме. Это достигается либо путем окисления или (значительно реже) восстановления молекул с помощью оксидо-редуктаз, либо путем их гидролиза эстеразами и амидазами.
Фаза ll - этап биологической конъюгации промежуточных продуктов метаболизма с эндогенными молекулами, такими как глутатион, глюкуроновая кислота, сульфат и т.д. Специфические системы транспорта конъюгированных дериватов обеспечивают их выведение из организма.
В ходе биопревращений липофильный и, следовательно, трудновыводимый ксенобиотик становиться гидрофильным продуктом, что обусловливает возможность его быстрой экскреции.
Классическим примером биотрансформации ксенобиотиков является метаболизм бензола в организме (рисунок 3)
Рисунок 3. Метаболизм бензола
В ходе l фазы метаболизма обеспечивается превращение жирорастворимого субстрата в полярный продукт путем включения в молекулу гидроксильной группы. В ходе ll фазы образовавшийся фенол взаимодействует с эндогенным сульфатом, в результате полярность образующегося продукта еще более возрастает. Фенилсульфат прекрасно растворяется в воде и легко выделяется из организма.
Далеко не всегда преобразования молекулы представляет собой простое чередование 1 и 11 фаз метаболизма. Возможна и более сложная последовательность реакций биопревращений (рисунок 4).

Рисунок 4. Схема последовательности метаболических превращений дибромэтана (GST - глутатион-S-трансфераза; GSглутатион)
2. Локализация процессов биотрансформации
Основным органом метаболизма ксенобиотиков в организме человека и млекопитающих является печень, главным образом благодаря разнообразию и высокой активности здесь ферментов биотрансформации. Кроме того, портальная система обеспечивает прохождение всех веществ, поступивших в желудочно-кишечный тракт, именно через печень, до того, как они проникнут в общий кровоток. Это также определяет функциональное предназначение органа. Тончайшая сеть печеночных капилляров, огромная площадь контакта между кровью и поверхностью гепатоцитов, обеспечивающаяся микроворсинками базальной поверхности печеночных клеток, обусловливают высокую эффективность печеночной элиминации токсиканта на клеточном уровне (рисунок 5).
Рисунок 5. Локализация этапов метаболических превращений ксенобиотиков в организме
Продукты l фазы метаболизма поступают в общий кровоток и могут оказывать действие на органы и системы. Печень выбрасывает в кровь и продукты ll фазы метаболизма. Из крови продукты превращения могут захватываться почками, легкими, другими органами, повторно печенью для экскреции с желчью. С желчью метаболиты поступают в кишечник, где частично реабсорбируются и повторно поступать в печень (цикл печеночной рециркуляции).
Несмотря на доминирующую роль печени в метаболизме ксенобиотиков, другие органы также принимают участие в этом процессе. Почки и легкие содержат энзимы и l и ll фаз метаболизма. Особенно велика роль почек, поскольку в этом органе имеется специфическая система захвата и катаболизма продуктов конъюгации, образующихся в печени. Активность других органов, таких как кишечник, селезенка, мышечная ткань, плацента, мозг, кровь - значительно ниже, однако наличие энзимов, катализирующих процессы биотрансформации, при отравлении токсифицирующимися ксенобиотиками, имеет ключевое значение в развитии патологических процессов в этих органах. В процессе внепеченочного метаболизма могут образовываться продукты, как аналогичные продуктам печеночного происхождения, так и отличные от них.

Иногда в ходе внепеченочного метаболизма может осуществляться активация метаболитов, образующихся в печени.
Энзимы, участвующие в метаболизме ксенобиотиков, локализованы в основном внутриклеточно. Небольшое их количество определяется в растворимой фракции циотозоля, митохондриях, большинство же связаны с гладким эндоплазматическим ретикулумом (таблица 1). Методом ультрацентрфугирования гладкий эндоплазматический ретикулум выделяется из исследуемых клеток в виде фрагментов мембранных структур, называемых микросомами. Поэтому основная группа ферментов, участвующих в метаболизме ксенобиотиков, получила название "микросомальные энзимы".
Таблица 1. Энзиматические реакции метаболизма ксенобиотиков и локализация энзимов внутри гепатоцита.
1 ФАЗА
ТИП РЕАКЦИИ |
|
ЛОКАЛИЗАЦИЯ |
|
||
1. |
Окисление: |
микросомы |
Гидроксилирование |
||
Декарбоксилирование |
микросомы |
|
Образование |
оксидов |
микросомы |
Десульфурирование |
микросомы |
|
Дегалогенирование |
микросомы |
|
Окисление |
спиртов |
микросомы, цитозоль |
Окисление |
альдегидов |
цитозоль |
2. |
Восстановление: |
цитозоль |
Восстановление |
альдегидов |
|
Азо-восстановление |
микросомы |
|
Восстановление нитросоединений |
микросомы, цитозоль |
|
3. |
Гидролиз: |
микросомы, цитозоль |
Расщепление |
эфиров |
|
Расщепление амидных связей |
микросомы, цитозоль |
|
2 ФАЗА
ТИП РЕАКЦИИ |
|
|
ЛОКАЛИЗАЦИЯ |
Конъюгация с глюкуроновой кислотой |
микросомы |
||
Конъюгация |
с |
сульфатом |
цитозоль |
Ацилирование |
|
|
микросомы, цитозоль |
Конъюгация |
с |
глутатионом |
цитозоль |
Метилирование |
|
|
цитозоль |
Часть ферментных систем метаболизма ксенобиотиков локализуются в жидкостях организма. Прежде всего, это эстеразы плазмы крови, участвующие в гидролизе целого ряда чужеродных веществ, таких как ФОС, некоторые алкалоиды (атропин), лекарства (суксаметоний, прокаин) и др.
3. Первая фаза метаболизма
Разнообразие чужеродных химических веществ, способных подвергаться в организме метаболическим превращениям, является следствием многообразия энзимов, участвующих в l фазе биотрансформации и их низкой субстратной специфичности. Многие из энзимов существуют в нескольких формах (изоферменты), различающихся по своим физикохимическим свойствам (молекулярная масса, электрофоретическая подвижность, абсорбцией света с разними длинами волн), отношению к индукторам и ингибиторам (см. ниже) и активностью в отношении субстратов различного строения.
Энзимы l фазы, участвующие в процессе биотрансформации ксенобиотиков, можно классифицировать в соответствии с типом активируемой ими реакции:

1.Оксидазы смешанной функции: цитохромР-450 (Р-450) и флавинсодержащие монооксигеназы (ФМО);
2.Простогландинсинтетазы - гидропероксидазы (ПГС) и другие пероксидазы;
3.Алкогольдегидрогеназы и альдегиддегидрогеназы;
4.Флавопротеинредуктазы;
5.Эпоксидгидролазы;
6.Эстеразы и амидазы.
Примеры веществ, подвергающихся метаболизму при участии указанных энзимов, приведены в таблице 2.
Таблица 2. Примеры веществ, подвергающихся биотрансформации при участии энзимов l фазы
Энзимы и реакции |
Вещества |
|
|
|
|||
1. |
ЦитохромР-450 |
|
|
-эпоксид/гидроксилирование |
Алдрин, |
афлатоксины |
|
-N,O,S-деалкилирование |
Этилморфин, |
метилмеркаптан |
|
-N,S,P-окисление |
Тиобензамид, 2-ацетиламинофторид |
||
-десульфурация |
Паратион, |
сероуглерод |
|
-дегалогенирование |
СCl4, |
хлороформ |
|
-нитро-восстановление |
Нитробензол |
|
|
-азо-восстановление |
О-аминоазотолуол |
|
|
2. |
ФМО |
|
|
-N,S,P-окисление |
Никотин, |
тиомочевина |
|
-десульфурация |
|
|
|
3. |
Простогландинсинтетаза |
Ацетаминофен |
|
-дегидрирование |
|
||
-N-деалкилирование |
Диметиланилин |
|
|
-эпоксид/гидроксилирование |
Бенз(а)пирен |
|
|
-окисление |
Билирубин |
|
|
4.Алкогольдегидрогеназа
-окисление |
Метанол, |
этанол, |
гликоли |
-восстановление |
Альдегиды, |
|
кетоны |
5.Альдегиддегидрогеназа
-окисление Альдегиды
6.Эстеразы, амидазы
-гидролиз |
Параоксон, |
зарин |
7.Эпоксидгидролазы
-гидролиз Ареноксиды
Особое значение для биотрансформации ксенобиотиков имеют микросомальные энзимы. Как уже указывалось, морфологическим эквивалентом микросом в интактных клетках является гладкий эндоплазматический ретикулум. Ферменты микросом не принимают участие в окислении большинства эндогенных соединений, таких как аминокислоты, нуклеотиды, сахара и т.д., для которых существуют специфические пути превращения. Однако в метаболизме некоторых эндогенных соединений (например, стероидов) микросомальные оксидазы принимают участие наряду со специфическими ферментными комплексами. Под влиянием этих энзимов могут метаболизировать некоторые жирные кислоты, простогландины и т.д. Кофакторы микросомальных монооксигеназ, принимающих участие в метаболических превращения ксенобиотиков, представлены на рисунке 6.

Рисунок 6. Кофакторы энзимов l фазы метаболизма ксенобиотиков: (1) цитохромР-450 зависимые оксидазы (Р-450); (2) флавинсодержащие монооксигеназы (ФМО)
Входе микросомального окисления часто образуются реакционноспособные промежуточные продукты. Некоторые из них нестабильны и подвергаются дальнейшему превращению, другие достаточно устойчивы.
Втаблице 3 представлены некоторые примеры биопревращений, приводящих к образованию реактивных продуктов.
Таблица 3. Примеры биотрансформации ксенобиотиков с образованием активных промежуточных продуктов в ходе l фазы метаболизма
Исходное веществоПродукт реакции |
Класс соединения |
Энзимы |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ацилгалоген |
Р-450 |
|
хлороформ |
фосген |
||||||||||||||||
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
аллиловый спирт |
акролеин |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дихлорэтан хлорацетальдегид

 ненасыщенный альдегид
ненасыщенный альдегид
 алкогольдегидрогеназа
алкогольдегидрогеназа
альдегид Р-450
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
алкил |
Р-450 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
диметил |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
диазониум |
||||||||||||||||||||||||||||||
ион метилдиазониума |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
нитрозамин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Р-450 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
дикетон |
алкоголь |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
гексан |
гександион |
|
дегидрогеназа |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
эпоксид |
Р-450 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
винилхлорид |
хлорэтиленэпоксид |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Р-450 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
диол эпоксид |
эпоксидгидролаза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пероксидаза |
|
бенз(а)пирен |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
бензпирендиолэпоксид |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
хинол |
Р-450 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пероксидаза |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
бензол |
бензохинол |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
CCL4 |
CCL3* |
алкильный |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
тетрахлор |
Р-450 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
тетрахлорметил-радикалрадикал |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
метан |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||



























 хинонимин пероксидаза р-аминофенол р-бензохинонимин
хинонимин пероксидаза р-аминофенол р-бензохинонимин
3.1. Окислительно-восстановительные превращения
3.1.1. Оксидазы смешанной функции
3.1.1.1. ЦитохромР-450-зависимая монооксигеназная система
Энзимы рассматриваемой группы, цитохромР-450 зависимые оксидазы (Р-450), как правило, обладают низкой субстратной специфичностью, вызывая превращения веществ самого разного строения, и потому часто называются оксидазами смешенной функции (ОСФ). Р-450 относятся к группе гемопротеинов типа цитохромов b - пигментов, активно связывающих монооксид углерода. Название "цитохромР-450" энзимы получили в силу того, что максимум поглощения света пигментом, связанным с СО, осуществляется при длине волны 450 нм.
Р-450 представляют собой семейство энзимов, локализующихся в эндоплазматическом ретикулуме, которые могут быть разделены с помощью иммунологических и иных методов на несколько подсемейств. Отдельные ткани содержат несколько различных изоформ Р-450. Встречаются тканеспецифичные формы энзимов. Изоферменты Р-450 часто проявляют перекрестную субстратную специфичность, таким образом, как правило, более чем один изофермент принимает участие в метаболизме ксенобиотика. Наличие специфических форм энзимов обусловлено генетическими механизмами, а повышение содержания в тканях различных изоферментов индуцируется действием на организм различных ксенобиотиков: лекарств, ядов, экотоксикантов. Р-450 подвержены не только активации, но и инактивации, как исходными ксенобиотиками, так и их реактивными метаболитами.
Реакции микросомального окисления, протекающие при участии Р-450, как правило, зависят от содержания O2 и НАДФН в среде. Молекулярный кислород активируется цитохромомР-450 (или другими цитохормами, например, Р-448). Активация осуществляется с помощью НАДФН при участии флавин-содержащего энзима НАДФН-цитохромР-450 редуктазы. Поскольку донором электронов в превращениях субстратов, катализируемых этими энзимами, является НАДФН, суммарное уравнение реакции может быть записано следующим образом:
ЦитохромР-450, НАДФН-цитохромР-450 редуктаза и фосфолипиды биологических мембран, в которые встроены оба энзима, образуют микросомальный монооксигеназный комплекс. Несмотря на то, что энзимы комплекса связаны с биологическими мембранами, их свойства могут быть изучены in vitro.
Установлены основные закономерности протекания ферментативных процессов с участием микросомального монооксигеназного комплекса (рисунок 7).

Рисунок 7. Упрощенная схема превращения субстрата при участии Р-450
Как видно из рисунка на начальном этапе ксенобиотик (S) вступает во взаимодействие с окисленной формой цитохромаР-450. Затем к этому комплексу с помощью НАДФН-зависимой цитохромР-450 редуктазы присоединяется электрон, донором которого является восстановленный НАДФН. После этого комплекс взаимодействует с кислородом. После взаимодействия со вторым электроном (донор - НАДФН) происходит активация связанного с цитохромом кислорода, который приобретает способность связывать протоны и образовывать воду. Образовавшаяся при этом форма цитохромаР-450 гидроксилирует субстрат.
Метаболизируемое вещество не связывается непосредственно с геминовой группой цитохромаР-450. Оно присоединяется к белковой части цитохрома. Процесс превращения ксенобиотиков чувствителен к СО, поскольку это вещество вытесняет кислород из связи с железом геминовой группы цитохромаР-450. Некоторые оксидазы резистентны к СО (образование N-оксидов).
Поскольку Р-450 - гемопротеины, их активность отчасти регулируется процессами синтеза гема, т.е. связана с метаболизмом железа. Нарушение метаболизма, голодание, понижение соотношения НАДФН/НАДФ+ могут приводить к снижению активности Р-450.
3.1.1.1.1. Реакции, катализируемые цитохромомР-450
Окисление ксенобиотиков при участии Р-450 - основной механизм их биотрансформации в l фазе метаболизма. Р-450 катализирует окисление практически всех классов органических молекул. Субстратом для энзимов являются и простые молекулы типа хлороформа и стероиды и сложные гетероциклические соединения, например антибиотик циклоспорин. Р-450 могут катализировать не только окисление, но и восстановление некоторых биосубстратов, например четыреххлористого углерода, галотана, некоторых других галогенированных углеводородов с образованием свободных радикалов. Такое необычное превращение реализуется в условия пониженного парциального давления кислорода в тканях.
Эпоксидирование и гидроксилирование ароматических соединений.
Метаболизм полициклических и ароматических углеводородов сопровождается образованием реакционно-способных промежуточных продуктов метаболизма, в частности ареноксидов, способных вызывать некроз клеток и являющихся канцерогенами. Таким образом осуществляется, в частности, превращение бенз(а)пирена (см. выше) или нафталена:
