
- •Глава 1 Химическая термодинамика.
- •1.1 Основные понятия и определения в термодинамике.
- •Термодинамические процессы.
- •Внутренняя энергия
- •Формы обмена энергией
- •1.2. Первый закон термодинамики.
- •Теплоемкость
- •Влияние температуры на теплоемкость
- •Термохимия
- •Энтальпии образования и сгорания
- •Закон Гесса и следствия из него
- •Зависимость теплового эффекта от температуры. Уравнение Кирхгофа.
- •Второй закон термодинамики Самопроизвольные и несамопроизвольные процессы.
- •Содержание и формулировки второго закона термодинамики. Энтропия как функция состояния системы.
- •Статистический характер второго закона термодинамики.
- •Некоторые закономерности в изменении энтропии веществ.
- •Изменение энтропии в химических реакциях.
- •Температурная зависимость стандартной энтропии реакции.
- •Изменение энергии Гиббса
- •Термодинамическая зависимость стандартной энергии Гиббса химической реакции - ∆rG0т
- •Направление процессов в открытых многокомпонентных системах. Химический потенциал.
- •Термодинамика химических равновесий
- •Уравнение изотермы химической реакции.
- •Зависимость константы равновесия от температуры. Уравнение изобары реакции.
- •Глава 2 Химическая кинетика.
- •2.1 Общие представления о скорости химических реакций.
- •2.2 Зависимость скорости реакции от концентрации. Закон действующих масс.
- •Скорость гетерогенных химических реакций.
- •2.3 Влияние температуры на скорость химических реакций.
- •2.4 Кинетическая классификация реакций
- •Кинетические уравнения реакций различных порядков
- •Кинетические представления о химическом равновесии.
- •Смещение химического равновесия.
- •2.5 Теоретические подходы к трактовке элементарного акта химической реакции.
- •Теория активных соударений (тас)
Изменение энтропии в химических реакциях.
Перейдем от состояния вещества к процессам от абсолютных значений энтропий к их изменениям, обусловленным химическим взаимодействием. Зная значения стандартных энтропий можно рассчитать изменение энтропии при протекании химической реакции:
∆rS0298 = ΣviS0298i(продуктов реакции) - ΣvjS0298j(исходных веществ),
Так, для реакции v1А1 + v2А2= v3А3+v4А4;
∆rS0298 = [v3S0298(А3) + v4 S0298(А4) ] - [v1S0298(А1)+ v2S0298(А2)]
Например, для процесса протекающего при стандартных условиях
Н2(г) + ½ О2(г) = Н2О(ж);∆rS0298
∆rS0298
= S0298![]() - (S0298
- (S0298
![]() +½
S0298
+½
S0298
![]() )
= 69,95 – 130,52 – ½ 205,04 = - 163,14 Дж/моль*К
)
= 69,95 – 130,52 – ½ 205,04 = - 163,14 Дж/моль*К
Стандартная энтропия любого вещества является положительной величиной (S0298 >0), изменения энтропии в процессах (∆rS) могут быть положительными, отрицательными или равными нулю.
Температурная зависимость стандартной энтропии реакции.
Стандартная энтропия реакции при Т ≠ 298 К вычисляется с учетом теплоемкостей исходных веществ и продуктов реакции.
∆rS0(т)
= ∆rS0298
+![]() dT (1.55)
dT (1.55)
Если считать, что теплоемкость не является функцией температуры ∆Ср(Т) ≠ f(T), но после интегрирования получим:
∆rS0(т)
=∆rS0298+∆Ср * ln![]() (1.56)
(1.56)
При температурной зависимости теплоемкости, которая выражается степенным рядом:
∆Ср0=∆а +∆в * Т
формула (1.55) принимает вид:
∆rS0(т)
=∆rS0298+![]() dT =∆rS0298+∆а * ln
dT =∆rS0298+∆а * ln![]() +∆в (Т - 298) (1.57)
+∆в (Т - 298) (1.57)
Изменение энергии Гиббса
Изменение энергии Гиббса - критерий направленности самопроизвольного процесса в закрытой системе. Реальные процессы происходят, как правило, в закрытых системах в изобарно-изотермических (р,Т = const) условиях, это наиболее типичный режим для самых различных процессов. Из уравнения (1.50) при р = const и Т = const находим
δА' ≤ - d (U + pv - TS) р,Т (1.58)
введем обозначение
δА' ≤ - d (Н - TS) (1.59)
G = H – TS (1.60)
Функция G является функцией состояния системы и называется энергией Гиббса или изобарно-изотермическим потенциалом. Энергия Гиббса при р,Т = const является экстенсивным свойством системы ее абсолютные значения не поддаются вычислению.
Для обратимого процесса
δА' = dА' max = - (dG) р,Т (1.61)
А' max = - (G2– G1) = - (ΔG) р,Т (1.62)
Отсюда для обратимого (квазистатического) процесса при рассматриваемых условиях максимальная (полезная) работа (А' max) приобретает свойства функции состояния и равна убыли энергии Гиббса.
Уравнение (1.60) можно переписать в виде Н = G + T * S, где энергия Гиббса характеризует ту часть полной энергии системы, которая может быть превращена в работу в изобарно-изотермический процесс. В этом состоит физический смысл величины G. Величина Т * S характеризует связанную энергию, т.е. ту часть полной энергии системы, которая рассматривается в окружающей среде в виде теплоты. Для установления критерия направленности самопроизвольного процесса в закрытой системе продифференцируем уравнение (1.60).
dG = dU + pdv + vdP – TdS – SdT (1.63)
Согласно выражению (1.52), ТdS ≥ dU + рdV
dU ≤ ТdS – рdV (1.64)
Подставим в уравнение (1.63) вместо dU большую либо равную ей величину ТdS – рdV получим следующие неравенство:
dG≤ - S * dТ + Vdр (1.65)
Для изобарно-изотермического процесса (р,Т = const, dp = dT = 0) выражение (1.65) примет вид (dG)р,Т ≤ 0, или для конечных изменений энергии Гиббса
(ΔG)р,Т ≤ 0 G → Gmin (1.66)
Следовательно, в закрытой системе знак изменения энергии Гиббса является критерием направленности самопроизвольного процесса при проведении его в изобарно-изотермических условиях:
если ΔG= 0 (G → Gmin, энергия Гиббса достигла минимального значения), то система находится в состоянии термодинамического равновесия;
если ΔG< 0 (G → Gmin, энергия Гиббса убывает), то процесс в данном направлении термодинамически возможен;
если ΔG> 0, процесс в данном направлении термодинамически невозможен.
Применяя выражение (1.65) к обратимому равновесному процессу, получим
dG = – SdT + VdP (1.67)
из условия (1.67) вытекает
![]() (1.68)
(1.68)
![]() (1.69)
(1.69)
Из соотношений (1.68) следует, что объем системы, служит мерой возрастания энергии Гиббса при увеличении давления при постоянной температуре, а энтропия – мерой убыли энергии Гиббса с возрастанием температуры при постоянном объеме. Такие функции состояния, частные производные которых по соответствующим отработанным параметрам состояния в явной форме выражают другие параметры, называются характеристическими. Подставляя (1.69) в (1.60), получим
G = H + T![]() ,
или для процесса (в том числе и для
химической реакции) изменение энергии
Гиббса при переходе системы из состояния
1 в состояние 2
,
или для процесса (в том числе и для
химической реакции) изменение энергии
Гиббса при переходе системы из состояния
1 в состояние 2
∆rG0(т)
=∆rН0(т)
+ Т , (1.70)
, (1.70)
Где
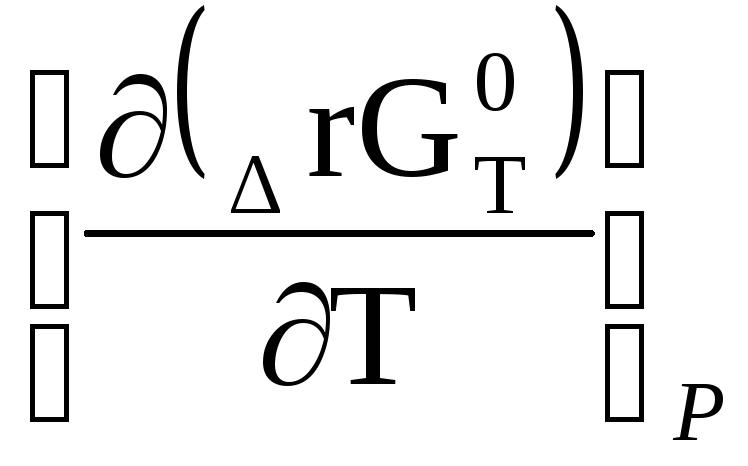 =
–∆rS0(т)
=
–∆rS0(т)
Выражение (1.70) называется уравнением Гиббса-Гельмгольца, оно связывает изменение энергии Гиббса химической реакции с ее тепловым эффектом и температурой. Иначе его можно записать в виде
∆rG0т =∆rН0т - Т∆rS0т (1.71)
Анализ уравнения (1.71) показывает, что знак и величина ∆rG0т зависят от двух факторов: энтальпийного -∆rН0т и энтропийного Т∆rS0т . Соотношение этих факторов определяет термодинамическую возможность самопроизвольного протекания реакции в закрытой системе прир,Т = const.
С одной стороны, в ходе химической реакции система стремиться перейти к минимальному уровню энтальпии, выделив часть ее в форме теплоты (∆rН0т< 0), с другой стороны, система стремиться занять наиболее вероятное состояние, характеризующееся максимумом беспорядка, т.е. максимумом энтропии (∆rS0т > 0).
Если процесс протекает так, что ∆rН0т= 0, то рост энтропии становится единственной движущей силой. И, наоборот, при условии∆rS0т = 0, движущей силой процесса является убыль энтропии.
Компенсация энтропийного и энтальпийного факторов соответствует установлению равновесия в системе.
∆rН0т = Т∆rS0т (1.72)
Изменение энергии Гиббса химической реакции при стандартных термодинамических условиях (р = 101,3 кПа, Т = 298 К) можно вычислить по уравнению ∆rG0298 =∆rН0298 -∆rS0298 * 298;
Возможен и другой путь расчета ∆rG0298 - по стандартным энергиям Гиббса образования исходных веществ и продуктов реакции∆fG0298;
∆rG0298
=![]() (1.73)
(1.73)
Стандартной энергией Гиббса образования вещества ∆fG0298называется изменение энергии Гиббса в реакции образования одного моля данного соединения из простых веществ, находящихся в термодинамически устойчивых модификациях, проведенной в стандартных термодинамических условиях.
Если в таблице нет значения ∆fG0298для какого-либо сложного вещества, его можно вычислить по уравнению
∆fG0298 =∆fН0298– 298∆fS0298; (1.74)
где ∆fН0298и∆fS0298– стандартные изменения энтальпии и энтропии соответственно в реакции образования одного моля этого соединения из простых веществ, находящихся в термодинамически устойчивых состояниях, проведенной в стандартных термодинамических условиях.
