
- •Министерство здравоохранения Республики Беларусь
- •Isbn 978-985-496-906-0 Содержание
- •Занятие № 1
- •Информационная часть занятия
- •1. Правила по технике безопасности при работе в химической лаборатории
- •2.1 Классификация органических соединений по природе функциональной группы и по строению углеродного скелета
- •2.2 Принципы химической номенклатуры – систематическая номенклатура июпак. Заместительная и радикально-функциональная номенклатура
- •2.4 Конформации циклических соединений
- •Занятие № 3
- •Практическая часть
- •Практическая часть
- •Практическая часть
- •Практическая часть
- •Содержание занятия
- •Практическая часть
- •Содержание занятия
- •Практическая часть
- •Содержание занятия
- •Содержание занятия
- •Литература
- •Практическая часть
- •Содержание занятия
- •Практическая часть
- •Содержание занятия
- •Литература
- •Практическая часть
- •Содержание занятия
- •Практическая часть
- •Содержание занятия
- •Литература
- •Практическая часть
- •Содержание занятия
- •Практическая часть
- •Занятие № 18 Тема: Физиологически активные гетерофункциональные производные бензольного ряда.
- •Содержание занятия
- •Практическая часть
- •Интегральная
- •10-Бальная шкала оценки знаний и умений студентов по
- •Оценка знаний студентов на основании письменного тестирования.
- •Вопросы для подготовки к экзамену по биоорганической химии
2.4 Конформации циклических соединений
В циклических молекулах наряду с торсионными напряжениями и напряжениями Ван-дер-Ваальса могут возникать напряжения Байера (угловые напряжения), обусловленные отклонением валентных углов от тетраэдрического – 109,5. Возникновение этих напряжений обусловлено отталкиванием электронных пар, образующих -связи, которые оказываются сближенными в пространстве, что приводит к увеличению энергии системы.
Циклопропан. В молекуле циклопропана атомы углерода лежат в вершинах правильного треугольника, угол между связями ССС равен 60. Такое значение валентного угла свидетельствует о возникновении сильных угловых напряжений в этой молекуле. Кроме угловых напряжений, в циклопропане возникают и торсионные напряжения, так, связи С-Н заслоняют друг друга, что также увеличивает энергию этой молекулы за счет отталивания противостоящих связей (электронных пар, образующих эти связи). Наличие сильных угловых и торсионных напряжений делает трехчленный цикл неустойчивым, поэтому в реакциях с участием циклопропана часто наблюдается разрыв цикла, в результате чего исчезают угловые напряжения.

Неустойчивость циклопропана может быть объяснена и тем, что в молекуле между атомами углерода возникают не -связи, а -связи, которые образуются при угловом перекрывании орбиталей. Угловое перекрывание орбиталей не требует снижения валентного угла от 109,5 до 60, при котором может идти их максимальное перекрывание вдоль линии, соединяющей атомы углерода. Возникновение -связей, являющихся промежуточными между - и -связями как по способу перекрывания орбиталей, так и по прочности, логично объясняет нестойкость циклопропана и его поведение в химических реакциях.
Циклобутан. Плоский четырехчленный цикл характеризуется наличием сильных угловых напряжений (угол 90 вместо 109,5) и торсионных напряжений. Однако циклобутан несколько стабильнее циклопропана за счет снижения напряжений в результате вращения вокруг связи углерод-углерод и вывода из плоскости одной метелиновой группы СН2.

Циклопентан. Плоский пятичленный цикл, имеющий форму правильного пятиугольника, характеризуется наличием торсионных и практическим отсутствием угловых напряжений, так, углы между связями равны 108, что незначительно отличается от обычного значения 109,5. Снижение торсионных напряжений достигается за счет образования неплоской структуры, напоминающей форму незакрытого конверта.

Практическое отсутствие угловых и торсионных напряжений в конформации «конверта» делают пятичленный цикл устойчивым.
Циклогексан. Молекула циклогексана в плоской конформации имеет форму правильного шестиугольника. Такая конформация характеризуется сильными угловыми (угол между связями 120 вместо 109,5) и торсионными напряжениями (связи заслоняют друг друга), что делает ее энергетически невыгодной, а такой плоский цикл непрочным. Снижение напряжений и увеличение стабильности циклогексана достигается за счет существования молекул в виде неплоских структур – конформаций ванны и кресла. В конформации ванны в молекуле нет угловых, но имееют место торсионные напряжения. В конформации кресла нет ни угловых, ни торсионных напряжений.

При комнатной температуре 99,9% молекул циклогексана находятся в конформации кресла.
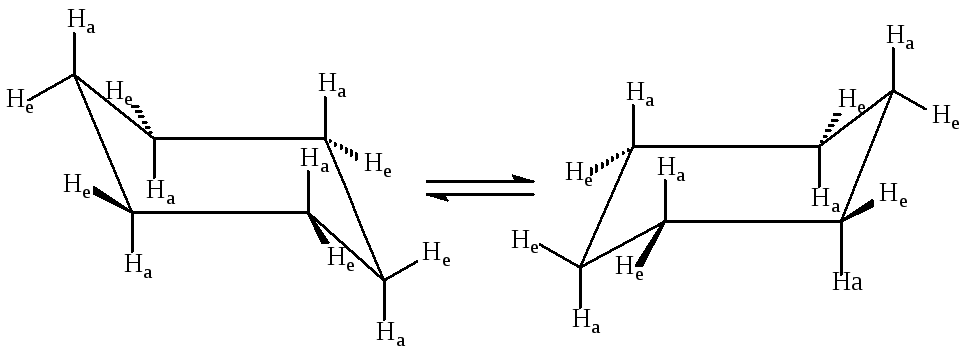
Обе конформации кресла энергетически равноценны, если в молекуле циклогексана нет заместителей. Связи атомов углерода с атомами водорода, расположенные параллельно оси симметрии молекулы циклогексана, называются аксиальными, связи, которые лежат под углом 109,5 к оси симметрии – экваториальными. Если в молекуле есть объемный заместитель, то энергетически более выгодной является та конформация кресла, в которой заместитель находится в экваториальном положении. Конформация кресла, в которой заместитель находится в аксиальном положении, менее выгодна энергетически, так как в этом случае в молекуле возникают 1,3–диаксиальные взаимодействия, которые обусловлены отталкиванием заместителя и атомов водорода в аксиальных положениях.

Однако известны производные циклогексана, в которых 1,3- диаксиальное расположение заместителей является предпочтительным. В этих соединениях между заместителями, находящимися в аксиальных положениях, возникает внутримолекулярная водородная связь, которая стабилизирует конформацию кресла и снижает ее энергию.

Практическая часть
Назовите по систематической номенклатуре IUPAC соединения, формулы которых приведены ниже:

Напишите структурные формулы соединений, исходя из их названий:
Пентен-3-он-2
Цикклопентадиен-1,3
2-Гидроксибензойная кислота
Цис-бутен-2-диовая кислота
3. Нарисуйте препочтительные конформации кресла для цис-3-хлорциклогексанола и цис-1,3-диметилциклогексана.
занятие № 2
Тема: Стереоизомерия, ее значение для проявления биологической активности.
Цель: Систематизировать знания о стереоизомерии органических соединений, сформировать представления о взаимосвязи физических, химических свойств и биологической активности молекулы с ее пространственным строением. Сформировать знания об абсолютной и относительной конфигурациях, D- и L-рядах стереохимической номенклатуры, энантиомерах и диастереомерах.
Исходный уровень:
Стереоизомеры: конфигурационные и конформационные.
Цис-, транс-изомеры.
Содержание занятия
1. Рассмотрение теоретического материала.
1.1 Структурная изомерия, виды структурной изомерии.
1.2 Стереоизомеры, конфигурация, конформация, конформационные и конфигурационные изомеры, диастереомеры, энантиомеры.
1.3 Элементы симметрии молекул: ось, плоскость и центр. Ахиральные и хиральные молекулы.
1.4 Асимметрический атом углерода (хиральный центр). Энантиомерия молекул с одним хиральным центром. Оптическая активность. Проекционные формулы Фишера. Относительная и абсолютная конфигурация. D - и L- система стереохимической номенклатуры.
1.5 Рацематы и рацемические смеси. Методы разделения рацемических смесей.
1.6 Стереоизомерия молекул с двумя и более центрами хиральности: энантиомерия и диастериоизомерия на примере винной кислоты. Мезоформы.
1.7 Значение стереоизомерии для проявления биологической активности.
2. Практическая часть.
2.1. Тестовый контроль усвоения материала.
ЛИТЕРАТУРА:
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. Москва, Медицина, 2008г., с. 64 – 85; 1991г., с.52 – 54, 68 – 75, 77 – 82, 86 – 87.
2. Павловский Н.Д. Лекции по биоорганической химии. Гродно, ГрГМУ, 2011, С. 138-151.
3. Руководство к лабораторным занятиям по биоорганической химии под редакцией Тюкавкиной Н.А. ,«Медицина», Москва, 1985,С. 138-152.
4. Конспект лекций.
Тестовые задания к теме: «Стереоизомерия»
1. Укажите соединение, существующее в виде пары -диастереомеров:
1) бутен-2
2) пропанол-2
3) пентадиен-1,4
4) глицериновый альдегид
5) акролеин
2. Укажите соединение, существующее в виде пары энантиомеров:
1) глицерин
2) этиленгликоль
3) гексен-1
4) 3-метилгексан
5) 2,2-диметилбутан
3. Укажите соединение, содержащее один хиральный центр:
1) метилциклопентан
2) циклопентанон
3) 2-метилциклогексанон-1
4) 4-метилциклогексанон-1
5) пропандиол-1,3
4. Укажите соединения, содержащие два хиральных центра:
1) бутанол-2
2) 2-метилциклопентанол-1
3) 2-метилбутандиол-2,3
4) 2-метилциколгексанон-1
5) 2-аминоэтанол-1
5. Укажите проекционную формулу Фишера, соответствующую D-молочной кислоте:

6. Укажите проекционную формулу Фишера, соответствующую D-аланину:
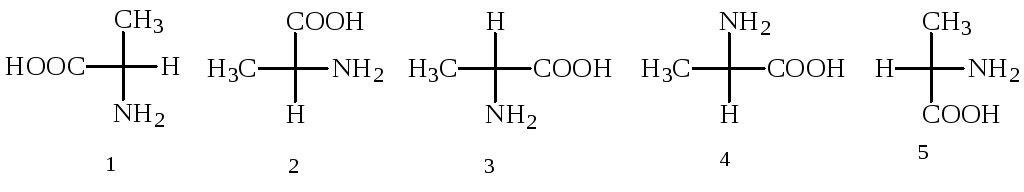
7. Укажите соединение, которое существует в виде 3 стереоизомеров:
1) 2-амино-3-гидроксибутановая кислота
2) 2,3-дихлорбутановая кислота
3) 2-амино-3-гидроксипропановая кислота
4) 2,3-дихлорбутандиовая кислота
5) этилгексан
8. Укажите соединение, которое может существовать в виде 4 стереоизомеров:
1) 2-амино-3-гидроксибутановая кислота
2) 2,2-дихлорбутановая кислота
3) 2-амино-3-гидроксипропановая кислота
4) 2,3-дигидроксибутандиовая кислота
5) метилгексан
9. Выберите верное утверждение. 3 -Метилбицикло4,3,0нонан (формула приведена ниже):

1) содержит один хиральный центр
2) содержит два хиральных центра
3) содержит три хиральных центра
4) имеет плоскость симметрии
5) имеет центр симметрии
10. Выберите верное утверждение.1,2-диметилбицикло4,3,0нонан

1) содержит один хиральный центр
2) содержит два хиральных центра
3) содержит три хиральных центра
4) имеет плоскость симметрии
5) имеет центр симметрии
11. Для молекулы 2-метилциклогексанола справедливо утверждение:

1) не имеет хиральных центров
2) имеет один хиральный центр
3) имеет два хиральных центра
4) имеет плоскость симметрии
5) не обладает оптической активностью
12. Выберите справедливые утверждения. Молекула тестостерона:
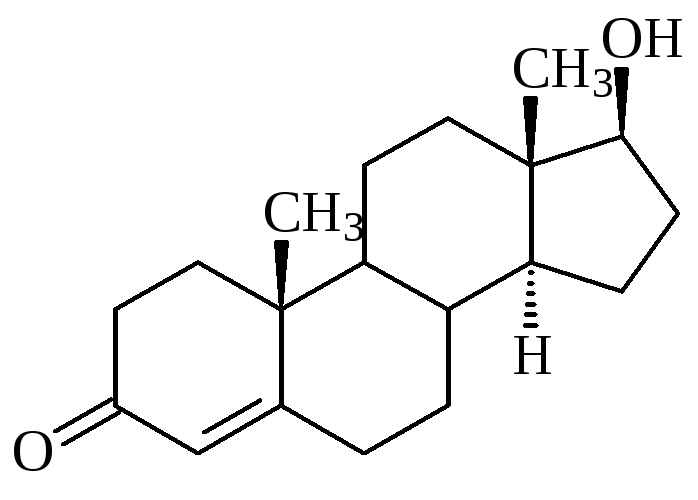
1) содержит один хиральный центр
2) содержит три хиральных центра
3) содержит пять хиральных центров
4) содержит шесть хиральных центров
5) содержит семь хиральных центров
13. В молекуле кортикостерона (формула приведена ниже) имеется семь хиральных центров. Хиральными центрами являются атомы углерода под номерами:

1) 5,8,9,10,11,13,14
2) 8,9,10,11,13,14,17
3) 9,10,11,13,14,17,18
4) 10,11,13,14,17,18,19
5) 11,13,14,17,18,19,21
14. В молекуле холестерина (формула приведена ниже) имеется восемь хиральных центров. Хиральными центрами являются атомы углерода под номерами:

1) 3,8,9,10,13,14,17,20
2) 3,5,8,9,10,13,14,17
3) 8,9,10,13,14,17,18,20
4) 10,13,14,17,18,19,20,21
5) 10,11,13,14,17,18,19,20,21
15. Смесь энантиомеров может образоваться в результате реакции между:
1) этеном и хлороводородом
2) пропаном и хлором
3) бутаном и бромом
4) бутеном-1 и бромоводородом
5) пропеном и хлороводородом
|
№ п/п |
Ответы |
№ п/п |
Ответы |
№ п/п |
Ответы |
№ п/п |
Ответы |
№ п/п |
Ответы |
|
1 |
1 |
4 |
2 |
7 |
4 |
10 |
3 |
13 |
2 |
|
2 |
4 |
5 |
1 |
8 |
1 |
11 |
3 |
14 |
1 |
|
3 |
3 |
6 |
4 |
9 |
3 |
12 |
4 |
15 |
3,4 |
