
- •Методические указания Красноярск 2004
- •Печатается по решению Редакционно-издательского совета университета
- •660074, Красноярск, ул. Киренского, 28
- •Пример 2.
- •Пример 3.
- •Пример 4.
- •Задания
- •Пример 2.
- •Пример 3.
- •Пример 4.
- •Задания
- •Пример 2.
- •Пример 3.
- •Задания
- •Пример 2.
- •Пример 3.
- •Пример 4.
- •Задания
- •Пример 2.
- •Пример 3.
- •Задания
- •Пример 2.
- •Пример 4.
- •Пример 5.
- •Задания
- •Пример 2.
- •Пример 3.
- •Задания
- •Пример 2.
- •Задания
- •Пример 2.
- •Задания
- •Пример 4.
- •Задания
- •Пример 2.
- •Пример 3.
- •Пример 4.
- •Задания
- •Пример 2.
- •Пример 3.
- •Задания
- •Пример 2.
- •Пример 3.
- •Пример 4.
- •Задания
- •Пример 4.
- •Задания
- •Пример 2.
- •Пример 3.
- •Пример 4.
- •Пример 5.
- •Пример 6.
- •Пример 9.
- •Пример 10.
- •Пример 11.
- •Задания
- •Пример 2.
- •Пример 3.
- •Пример 4.
- •Пример 5.
- •Пример 6.
- •Пример 9.
- •Пример 10.
- •Пример 11.
- •Задания
- •Пример 2.
- •Пример 3.
- •Задания
- •Пример 2.
- •Пример 3.
- •Пример 4.
- •Пример 5.
- •Пример 6.
- •Пример 7.
- •Пример 10.
- •Задания
- •Органические соединения. Полимеры
- •Стандартная энергия Гиббса образования
- •Константы диссоциации слабых электролитов
- •Растворимость солей и оснований в воде
- •Ряд стандартных электродных потенциалов металлов
- •Оглавление
Ряд стандартных электродных потенциалов металлов
-
Электрод
Электродная реакция
Е0, В
Li+/Li
Li+ +
 = Li
= Li–3,045
K+/K
K+ +
 = K
= K–2,925
Rb+/Rb
Rb+ +
 = Rb
= Rb–2,925
Cs+/Cs
Cs+ +
 = Cs
= Cs–2,923
Ba2+/Ba
Ba2+ + 2
 = Ba
= Ba–2,906
Ca2+/Ca
Ca2+ + 2
 = Ca
= Ca–2,866
Na+/Na
Na+ +
 = Na
= Na–2,714
Mg2+/Mg
Mg2+ + 2
 = Mg
= Mg–2,363
Be2+/Be
Be2++ 2
 = Be
= Be–1,847
Al3+/Al
Al3+ + 3
 = Al
= Al–1,662
Mn2+/Mn
Mn2+ + 2
 = Mn
= Mn–1,179
Zn2+/Zn
Zn2+ + 2
 = Zn
= Zn–0,763
Cr3+/Cr
Cr3+ + 3
 = Cr
= Cr–0,744
Fe2+/Fe
Fe2+ + 2
 = Fe
= Fe–0,440
Cd2+/Cd
Cd2+ + 2
 = Cd
= Cd–0,403
Co2+/Co
Co2+ + 2
 = Co
= Co–0,277
Ni2+/Ni
Ni2+ + 2
 = Ni
= Ni–0,250
Sn2+/Sn
Sn2+ + 2
 = Sn
= Sn–0,136
Pb2+/Pb
Pb2+ + 2
 = Pb
= Pb–0,126
2H+/H2
2H+ + 2
 = H2
= H20,000
Cu2+/Cu
Cu2+ + 2
 = Cu
= Cu+0,337
Ag+/Ag
Ag+ +
 = Ag
= Ag+0,799
Hg2+/Hg
Hg2+ + 2
 = Hg
= Hg+0,854
Pd2+/Pd
Pd2+ + 2
 = Pd
= Pd+0,987
Pt2+/Pt
Pt2+ + 2
 = Pt
= Pt+1,190
Au3+/Au
Au3+ + 3
 = Au
= Au+1,498
Оглавление
ВВЕДЕНИЕ 5
КОНТРОЛЬНЫЕ ЗАДАНИЯ 8
КОНТРОЛЬНОЕ ЗАДАНИЕ 1 8
Моль. Эквиваленты и молярные массы эквивалентов простых и сложных веществ. Закон эквивалентов 8
Строение атома 12
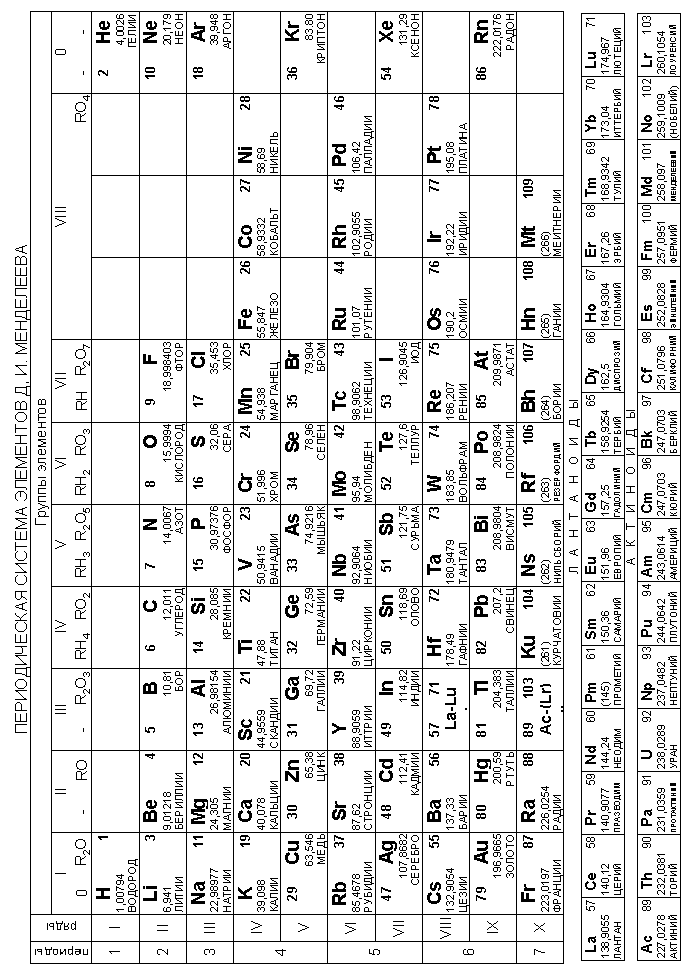
Периодическая система элементов Д. И. Менделеева 16
Химическая связь и строение молекул. Конденсированное состояние вещества 20
Энергетика химических процессов (термохимические расчеты) 24
Химическое сродство 28
Химическая кинетика и равновесие 33
Способы выражения концентрации растворов 39
Свойства растворов 43
Ионно-молекулярные (ионные) реакции обмена 47
Гидролиз солей 50
КОНТРОЛЬНОЕ ЗАДАНИЕ 2 53
Окислительно-восстановительные реакции 53
Электродные потенциалы и электродвижущие силы 60
Электролиз 65
Коррозия металлов 68
Комплексные соединения 74
s-элементы 78
Жесткость воды и методы ее устранения 87
р-элементы (...ns2np1–6) 96
d-элементы (...(n – l)d1-10ns0-2) 103
Органические соединения. Полимеры 111
ПРИЛОЖЕНИЕ 119
Растворимость солей и оснований в воде 121
Оглавление 124
