
- •Реакции полимеризации и сополимеризации олефинов. Натуральный и синтетический каучуки понятие о высокомолекулярных соединениях.
- •Классификация карбоновых кислот. Предельные одноосновные кислоты. Гомологический ряд. Изомерия. Номенклатура. Ацильные радикалы. Физические и химические свойства. Высшие жирные кислоты. Мыла.
- •Непредельные одноосновные кислоты. Понятие о двухосновных кислотах и кислотах с несколькими двойными связями.
- •Важнейшие представители: муравьиная, уксусная, капроновая, энантовая, акриловая, щавелевая, олеиновая, стеариновая, сорбиновая кислоты. Реакция поликонденсации.
- •Жиры и масла. Получение, гидролиз и гидрогенизация жиров. Саломас, маргарин.
- •Карбоновые кислоты ароматического ряда. Бензойная кислота. Фталевые кислоты. Понятие об окси-кислотах (молочная, лимонная, винная кислоты).
- •Амины. Классификация, изомерия, номенклатура, получение. Физические и химические свойства (основность, алкилирование, ацилирование, действие азотистой кислоты). Понятие о диаминах.
- •3. Цветные (качественные) реакции на белки:
Классификация карбоновых кислот. Предельные одноосновные кислоты. Гомологический ряд. Изомерия. Номенклатура. Ацильные радикалы. Физические и химические свойства. Высшие жирные кислоты. Мыла.
КАРБОНОВЫЕ КИСЛОТЫ — это производные УВ, содержащие функциональную карбоксильную группу —СООН.
![]()
где т — число карбоксильных групп, определяющее основность кислоты.
По основности кислоты делятся на:
—одноосновные (монокарбоновые), m=1;
—двухосновные (дикарбоновые), m=2;
—трехосновные (трикарбоновые), m=3 и т. д.
В зависимости от строения углеводородного радикала R карбоновые кислоты делятся на:
—предельные (насыщенные), R = алкил;
—непредельные (ненасыщенные) — производные непредельных УВ;
—ароматические — производные ароматических УВ.
 Гомологический
ряд
Гомологический
ряд
Номенклатура и изомерия
По международной заместительной номенклатуре название кислоты производят от названия соответствующего (с тем же числом атомов углерода) углеводорода с добавлением окончания -овая и слова кислота. Нумерацию цепи всегда начинают с атома углерода карбоксильной группы, поэтому в названиях положение группы —СООН не указывают.
При составлении названий кислот, имеющих сложное строение, иногда также используют тривиальные названия кислот, соответствующие наиболее длинной прямой цепи. В этом случае атомы углерода в прямой цепи обозначают греческими буквами, начиная с атома углерода, соседнего с карбоксильной группой: α (альфа), β (бета), γ (гамма) и т. д.
Например,

Внутри класса предельных монокарбоновых кислот возможна только изомерия углеродной цепи. Первые три члена гомологического ряда (НСООН, СН3СООН, С2Н5СООН) изомеров не имеют. Монокарбоновые кислоты изомерны сложным эфирам карбоновых кислот.
Ацильные радикалы, генерируемые из альдегидов, легко фрагментируют при температуре выше 100°С на алкильные радикалы и СО.
Физические свойства
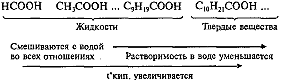
Химические свойства
Для насыщенных монокарбоновых кислот характерна высокая реакционная способность. Это определяется главным образом реакциями карбоксильной группы (разрыв связей О—Н и С—О), а также реакциями замещения атомов «Н» у α-утлеродного атома.
1.Реакции с разрывом связи О—Н (кислотные свойства, обусловленные подвижностью атома водорода карбоксильной группы). Предельные монокарбоновые кислоты обладают всеми свойствами обычных кислот.
—Диссоциация. В водных растворах монокарбоновые кислоты ведут себя как одноосновные кислоты: происходит их ионизация с образованием иона водорода и карбоксилат-иона.
Карбоновые кислоты являются слабыми кислотами. Наиболее сильной в гомологическом ряду насыщенных кислот является муравьиная кислота, в которой группа —СООН связана с атомом водорода.
2.Образование солей:
а) взаимодействие с активными металлами:
б) взаимодействие с основными оксидами:
в) взаимодействие со щелочами (реакция нейтрализации):
г) взаимодействие с аммиаком или гидроксидом аммония:
д) взаимодействие с солями более слабых кислот (карбонатами и гидрокарбонатами):
2. Реакции с разрывом связи С—О (замещение ОН-группы)
—Взаимодействие
со спиртами
с
образованием сложных эфиров (реакция
этерификации):
![]()
—Взаимодействие
с аммиаком
с
образованием амидов кислот ![]()
—Взаимодействие
с галогенидами фосфора
(PCls,
PCIJ
или тионилхлоридом SOCl2
с
образованием галогенангидридов
карбоновых кислот ![]()
![]()
—Межмолекулярная дегидратация карбоновых кислот с образованием ангидридов
Ангидриды представляют собой производные кислот, состоящие из двух соединенных через кислород кислотных радикалов (ацилов).
3.Реакции с разрывом связей С—Н у α-углеродного атома (реакции с участием радикала)
Атомы водорода у α-углеродного атома более подвижны, чем другие атомы водорода в радикале кислоты, и могут замещаться на атомы галогена с образованием α-галоген-карбоновых кислот.
Жирные кислоты — алифатические одноосновные карбоновые кислоты с открытой цепью, содержащиеся в этерифицированной форме в жирах, маслах и восках растительного и животного происхождения. Жирные кислоты, как правило, содержат неразветвленную цепь из четного числа атомов углерода и могут быть как насыщенными, так и ненасыщенными. ВЖК содержат более двенадцати атомов углерода.
Мыла — это соли высших жирных кислот (С10—С18). Мыла делятся на растворимые в воде (натриевые, калиевые, аммониевые) и нерастворимые (металлические мыла — соли Са, Mg, Ва, Pb, Ni, Мn, А1 и др.). Растворимость мыл в воде зависит от характера катиона: nh4+ > К+ > Na+ > Li+.
Жидкие калиевые мыла и твердые натриевые мыла получают растворением высших алифатических кислот в водных растворах едких щелочей:
С17Н35СООН + NaOH → C17H35CООNa + Н20 Стеариновая кислота Стеарат натрия (твердое мыло)
С17Н35СООН + КОН → С17Н35СООК + Н20
Стеарат калия (жидкое мыло)
