
4.2. Гидролиз 2-(динитрометилен)-5,5-динитропиримидин-4,6(1н,3н,5н)-диона.
Следующей стадией при получении ДАДНЭ является гидролиз 2-(динитрометилен)-5,5-динитропиримидин-4,6(1Н,3Н,5Н)-диона. Он был исследован в широком интервале кислотности среды, начиная от pH=7 до значения Н0=3,09 соответствующего 50% серной кислоте. Оказалось, что до рН=2 гидролиз практически не идет. В более кислой среде реакция описывается уравнением первого порядка с коэффициентами корреляции более 0,99. На рисунке 4.11 представлены пример кинетической кривой и зависимость концентраций компонентов во времени при гидролизе в среде 1Н соляной кислоты при 20°С. Суммарная концентрация ДАДНЕ и тетронитропроизводного остается постоянной, что говорит о высокой селективности процесса.
На рисунке 4.12 представлена зависимость константы скорости реакции гидролиза от кислотности среды. В интервале от рН 2 – до рН 0 происходит быстрый её рост. Однако к 31% серной кислоте (Но=-1,73) рост замедляется и далее константа слабо убывает. Одновременно происходи резкое падение выхода целевого продукта - с 95% до 53%. Следовательно, в средах в высокой кислотностью наряду с основной реакцией гидролиза тетранитропродукта, приводящей к ДАДНЭ, протекает процесс его полного разрушения. Поэтому для получения ДАДНЭ с высоким выходом необходимо проводить гидролиз в серной кислоте с концентрацией не выше …
Для подтверждения этих данных был проведен опыт по препаративному гидролизу тетранитропроизводного в 25% серной кислоте при комнатной температуре и соотношении компонентов 20 мл кислоты на 1 г. (время?) Выход составил 89,3% что находится в хорошем согласовании с кинетическими данными.
|
|
|
|
Рисунок 4.11 (а) Зависимость концентраций компонентов от времени при гидролизе тетранитропроизводного в среде 1 Н соляной кислоты при 20 °С |
Рисунок 4.11 (б) Расчет константы скорости реакции при гидролизе тетранитропроизводного в среде 1 Н соляной кислоты при 20 °С |
Для оценки возможных потерь ДАДНЭ в отработанной кислоте спектрофотометрическим методом была измерена его растворимость в воде, 1.8% и 25% растворах серной кислоты при комнатной температуре. Для этих растворов она соответственно составила 0,3, 0,16 и 0,15 г/л. Таким образом, потери за счет растворимости при выделении целевого продукта составляют 1-2%. Из вышеперечисленных фактов следует, что для получения ДАДНЕ с высоким выходом реакционную массу после нитрования следует разбавлять до концентрации кислот 25 – 30% масс.
|
|
|
|
Рисунок 4.12 (а) Зависимость константы скорости гидролиза тетранитропроизводного от кислотности среды |
Рисунок 4.12 (б) Зависимость выхода на стадии гидролиза от кислотности среды (как определяли?) |
Желательно привести наряду с графиком 4.12 таблицу зависимости выхода ДАДНЭ от концентрации серной кислоты.
4.3. Препаративные опыты по получению даднэ
На заключительном этапе работы для подтверждения кинетических опытов была проведена серия экспериментов по получению ДАДНЭ, в которых нитрование 6-гидрокси-2-метилпиримидин-4(3Н)-она серно-азотными нитрующими смесями проводили в различных условиях.
Результаты представлены в таблице 4.1. Модуль по серной кислоте оставался постоянным и составлял 4 мл на 1 г исходного вещества. Видно, что для полного протекания процесса требуется 3-х часовая выдержка. Избыток азотной кислоты так же немного повышает выход, что согласуется с данными кинетических экспериментов.
Таблица 4.1
Условия проведения препаративных экспериментов по синтезу ДАДНЭ
|
Время реакции, минуты |
45 |
90 |
180 |
90 |
90 |
90 |
|
HNO3/моль нитруемого соединения |
6,5 |
6,5 |
6,5 |
4,4 |
5,1 |
8
8
|
|
Выход ,% |
63 ,5 |
80,7 |
86,9 |
79,0 |
81,9 |
83,8 |
|
Параметр |
|
|
|
|
|
|
|
HNO3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Следует дать более полные данные об этих экспериментах, температура, навеска исходного вещества, концентрация аз.кислоты в нитрующей смеси (связать с кинетикой)
Таким образом, достигнут выход 80-87%, что хорошо согласуется с результатами кинетических экспериментов. При учете 2% потерь на растворимость этот результат предполагает 94 – 96% выход на каждой стадии.
Полученные продукты были проанализированы методом ВЭЖХ и показали чистоту не менее 99%. Дополнительно проведен анализ методом ДСК. Результаты представлены на рисунке 4.13.
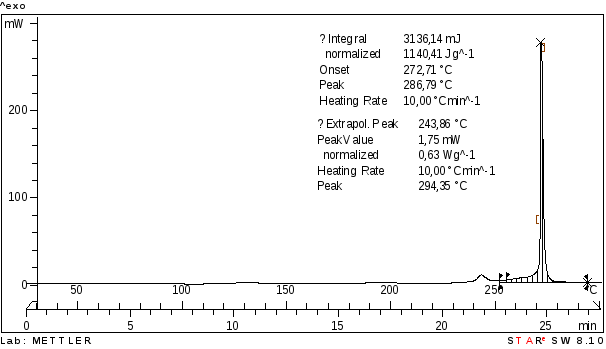

Рисунок 4.13 ДСК анализ одного из образцов полученного ДАДНЭ
Как видно из диаграммы интенсивное разложение полученного 1,1-диамино-2,2-динитроэтилена начинается в районе 270 °С. Также наблюдается незначительное разложение в областях от 180 до 210°С и от 240 до 250°С. Присутствует эндотермический пик в районе 105°С (переход α-формы в β [7]). Полученные результаты хорошо согласуются с результатами получены для термостатированного ДАДНЭ [17].




