
- •Липиды.
- •1.Важнейшие липиды тканей человека.Резеврные и протоплазматические липиды.
- •2.Классификация липидов.
- •3.Жирные кислоты, хар-ные для липидов тканей человека.
- •4.Эссенциальные жк-незаменимые факторы питания липидной природы.
- •5.Триацилглицерины.Строение, био функции.
- •6. Холестерин, биологическая роль, строение.
- •7. Основные фосфолипиды тканей человека, строение глицеролфосфолипидов, ф-ции.
- •8. Сфинголипиды, строение, биологическая роль.
- •9. Гликолипиды тканей чел. Гликоглицеролипиды и гликосфинголипиды. Ф-ции гликолипидов
- •10.Пищевые жиры и их переваривание.Гидролиз нейтрального жира в жкт,роль липаз.
- •11. Гидролиз фосфолипидов в жкт, фосфолипазы ( первая часть не оч… простите)
- •12. Желчные кислоты, строение, роль в обмене липидов
- •13. Всасывание продуктов переваривания липидов
- •14. Нарушение переваривания и всасывания липидов
- •15. Ресинтез триацилглицеринов в стенке кишечника
- •16) Образование хиломикронов и транспорт пищевых жиров. Липопротеин-липаза.
- •17)Транспорт жирных кислот альбуминами крови.
- •18)Биосинтез жиров в печени
- •20)Взаимопревращения разных классов липопротеинов , физиологический смысл процессов
- •Вопрос 26. Обмен жирных кислот, -окисление как специфический путь катаболизма жирных кислот, химизм, ферменты, энергетика.
- •Вопрос 27. Судьба ацетил-КоА
- •Вопрос 28. Локализация ферментов -окисления жирных кислот. Транспорт жирных кислот в митохондрии. Карнитин-ацилтрансфераза.
- •Вопрос 29. Физиологическое значение процессов катаболизма жирных кислот.
- •Вопрос 30. Биосинтез пальмитиновой жирной кислоты, химизм, жирнокислотная синтетаза.
- •Вопрос 32. Биосинтез ненасыщенных кислот. Полиненасыщенные жирные кислоты.
- •Вопрос 33. Биосинтез и использование ацетоуксусной кислоты, физиологическое значение процессов. К кетоновым телам относят три вещества: β-гидроксибутират, ацетоацетат и ацетон.
- •Синтез кетоновых тел:
- •Окисление кетоновых тел:
- •Вопрос 34. Обмен стероидов.Холестерин как предшественник других стероидов.Биосинтез холестерина. Обмен стероидов
- •Вопрос 35.Регуляция биосинтеза холестерина, транспорт холестерина кровью.
- •36. Роль лпнп и лпвп в транспорте холестерина.
- •37. Превращение холестерина в желчные кислоты, выведение из организма х и жк.
- •38. Конъюгация желчных кислот, первичные и вторичные жк
- •39. Гиперхолестеринэмия и ее причины.
- •40. Биохимические основы развития атеросклерохза. Факторы риска.
- •41. Биохимические основы лечения гиперхолестеролемии и атеросклероза
- •42. Роль омега-3 жирных кислот в профилактике атеросклероза (тупой! Тупой вопрос! Будь он проклят. Ничего нормального не нашел…что-то нарыл в интернете)
- •43. Механизм возникновения желчнокаменной болезни
- •44. Биосинтез глицеролфосфолипидов в стенке кишечника и тканях (тоже как-то не очень…что нашел, пардон)
- •46. Катаболизм сфинголипидов. Сфинголипидозы. Биосинтез сфинголипидов.
- •47. Обмен безазотистого остатка аминокислот, гликогенные и кетогенные аминокислоты
- •48. Синтез глюкозы из глицерина и аминокислот.
- •49. Глюкокортикостероиды, строение, функции, влияние на обмен ве¬ществ. Кортикотропин. Нарушение обмена при гипо- и гиперкортицизме (стероидном диабете).
- •50. Биосинтез жиров из углеводов
- •51. Регуляция содержания глюкозы в крови
- •52. Инсулин, строение и образование из проинсулина. Изменение концентрации в зависимости от режима питания
- •53. Роль инсулина в регуляции обмена углеводов, липидов и аминокислот.
- •54. Сахарный диабет. Важнейшие изменения гормонального статуса и обмена веществ.
- •55. Патогенез основных симптомов сахарного диабета.
- •56. Биохимические механизмы развития диабетической комы.(я не уверена что правильно)
- •57. Патогенез поздних осложнений сахарного диабета (микро- и макроангиопатии, ретинопатии,нефропатия,катаракта)
Вопрос 26. Обмен жирных кислот, -окисление как специфический путь катаболизма жирных кислот, химизм, ферменты, энергетика.
Жирные кислоты поступают с пищей или синтезируются в организме (кроме полиеновых кислот). Субстраты, необходимые для синтеза жирных кислот, образуются при катаболизме глюкозы и таким образом, часть глюкозы превращается сначала в жирные кислоты, а затем в жиры. Хотя специфический путь катаболизма жирных кислот заканчивается образованием ацетил-КоА, служащим исходным субстратом для синтеза жирных кислот, процессы синтеза и окисления жирных кислот необратимы. Они происходят в разных компартментах клеток (биосинтез протекает в цитозоле, а окисление - в митохондриях) и катализируются разными ферментами. Окисление жирных кислот как источников энергии увеличивается в постабсорбтивный период, при голодании и физической работе. В этих состояниях их концентрация в крови увеличивается в результате мобилизации из жировых депо, и они активно окисляются печенью, мышцами и другими тканями. При голодании часть жирных кислот в печени превращается в другие "топливные" молекулы - кетоновые тела. Они, в отличие от жирных кислот, могут использоваться нервной тканью как источник энергии. При голодании и длительной физической работе кетоновые тела служат источником энергии для мышц и некоторых других тканей.
Активация жирных кислот
Важно отметить, что перед тем, как вступить в различные реакции, жирные кислоты должны быть активированы, т.е. связаны макроэргической связью с коферментом А:
RCOOH + HSKoA + АТФ → RCO ~ КоА + АМФ + PPi.
Реакцию катализирует фермент ацил-КоА син-тетаза. Выделившийся в ходе реакции пирофосфат гидролизуется ферментом пирофосфатазой: Н4Р2О7 + Н2О → 2 Н3РО4.
Выделение энергии при гидролизе макроэргической связи пирофосфата смещает равновесие реакции вправо и обеспечивает полноту протекания реакции активации
Жирные кислоты должны еще попасть в матрикс митохондрий. Этот процесс будет в 28 вопросе.- «Транспорт жирных кислот с длинной углеводородной цепью в митохондриях»
β-Окисление - специфический путь катаболизма жирных кислот, при котором от карбоксильного конца жирной кислоты последовательно отделяется по 2 атома углерода в виде ацетил-КоА.
β-Окисление жирных кислот, происходит в матриксе митохондрий в аэробных условиях и заканчивающийся образованием ацетил-КоА. Водород из реакций β-окисления поступает в ЦПЭ, а ацетил-КоА окисляется в цитратном цикле, также поставляющем водород для ЦПЭ. Поэтому β-окисление жирных кислот - важнейший метаболический путь, обеспечивающий синтез АТФ в дыхательной цепи.
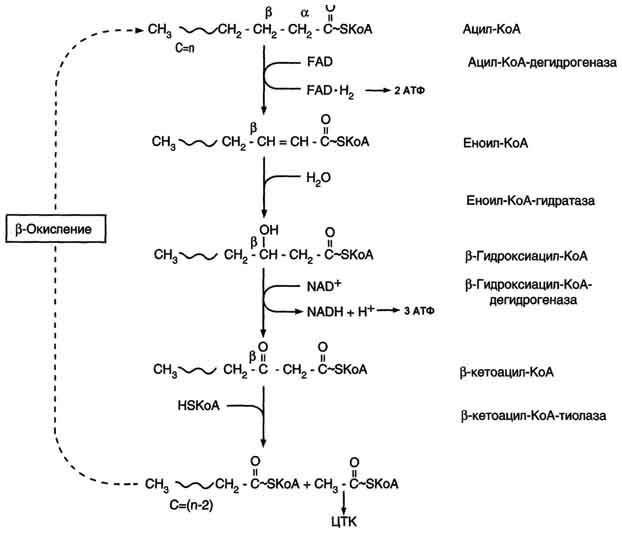
(То что идет в ЦТК – это ацЕтил-Коа, ацил-Коа подвергается дальнейшему окислению) Эту последовательность реакций обычно называют "циклом β-окисления", имея в виду, что одни и те же реакции повторяются с радикалом жирной кислоты до тех пор, пока вся кислота не превратится в ацетильные остатки.
Энергетика:
Продуктами каждого цикла β-окисления являются FADH2, NADH и ацетил-КоА. Хотя реакции в каждом "цикле" одни и те же, остаток кислоты, который входит в каждый последующий цикл, короче на 2 углеродных атома. В последнем цикле окисляется жирная кислота из 4 атомов углерода, поэтому образуются 2 молекулы ацетил-КоА, а не 1, как в предыдущих. Суммарное уравнение β-окисления, например пальмитоил-КоА может быть представлено таким образом:
С15Н31СО-КоА + 7 FAD + 7 NAD+ + 7 HSKoA → 8 СН3-СО-КоА + 7 FADH2 + 7 (NADH + H+).
Если рассчитывать выход АТФ при окислении пальмитиновой кислоты (табл. 8-7), то из общей суммы молекул АТФ необходимо вычесть 2 молекулы, так как на активацию жирной кислоты тратится энергия 2 макроэргических связей (см. реакцию активации жирной кислоты).
Синтез АТФ при полном окислении пальмитиновой кислоты
|
β-Окисление |
Количество молекул АТФ |
|
7 NADH (от пальмитоил-КоА до ацетил-КоА), окисление каждой молекулы кофермента в ЦПЭ обеспечивает синтез 3 молекул АТФ |
21 |
|
7 FADHa, окисление каждой молекулы кофермента в ЦПЭ обеспечивает синтез 2 молекул АТФ |
14 |
|
Окисление каждой из 8 молекул ацетил-КоА в ЦТК обеспечивает синтез 12 молекул АТФ |
96 |
|
Суммарное количество молекул АТФ, синтезированных при окислении одной молекулы пальмитоил-КоА |
131 |
Во многих тканях окисление жирных кислот - важный источник энергии. Это ткани с высокой активностью ферментов ЦТК и дыхательной цепи - клетки красных скелетных мышц, сердечная мышца, почки. Эритроциты, в которых отсутствуют митохондрии, не могут окислять жирные кислоты. Жирные кислоты не служат источником энергии для мозга и других нервных тканей, так как жирные кислоты не проходят через гематоэнцефалический барьер, как и другие гидрофобные вещества. В экспериментах показано, что скорость обмена жирных кислот в нервной ткани существенно меньше, чем в других тканях.
Еще проще можно посчитать по формуле:
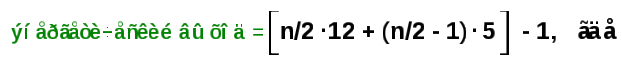
n – количество С-атомов в жирной кислоте;
n/2 – количество молекул ацетил-КоА, образованных в процессе β-окисления;
12 – количество АТФ, синтезирующихся при окислении ацетил-КоА в ЦТК;
(n/2 – 1) – количество циклов β-окисления;
5 – количество молекул АТФ, образованных в каждом цикле за счёт двух реакций дегидрирования;
1 – затрата 1 молекулы АТФ на активацию жирной кислоты
