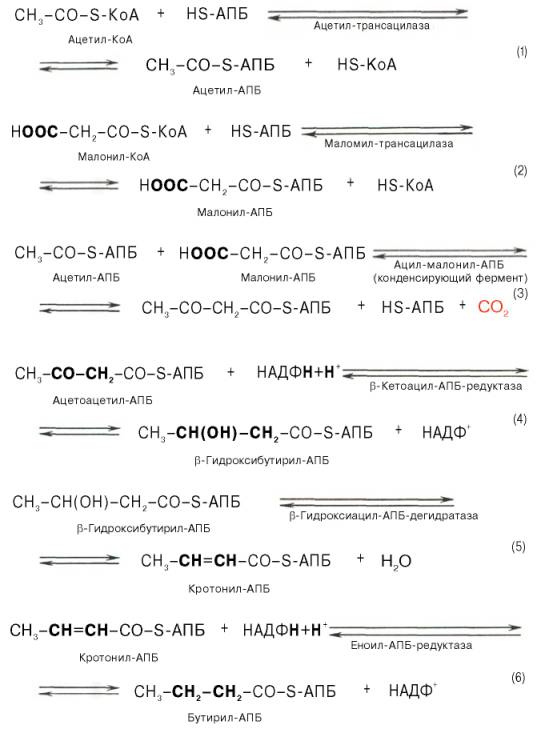
- •Липиды.
- •1.Важнейшие липиды тканей человека.Резеврные и протоплазматические липиды.
- •2.Классификация липидов.
- •3.Жирные кислоты, хар-ные для липидов тканей человека.
- •4.Эссенциальные жк-незаменимые факторы питания липидной природы.
- •5.Триацилглицерины.Строение, био функции.
- •6. Холестерин, биологическая роль, строение.
- •7. Основные фосфолипиды тканей человека, строение глицеролфосфолипидов, ф-ции.
- •8. Сфинголипиды, строение, биологическая роль.
- •9. Гликолипиды тканей чел. Гликоглицеролипиды и гликосфинголипиды. Ф-ции гликолипидов
- •10.Пищевые жиры и их переваривание.Гидролиз нейтрального жира в жкт,роль липаз.
- •11. Гидролиз фосфолипидов в жкт, фосфолипазы ( первая часть не оч… простите)
- •12. Желчные кислоты, строение, роль в обмене липидов
- •13. Всасывание продуктов переваривания липидов
- •14. Нарушение переваривания и всасывания липидов
- •15. Ресинтез триацилглицеринов в стенке кишечника
- •16) Образование хиломикронов и транспорт пищевых жиров. Липопротеин-липаза.
- •17)Транспорт жирных кислот альбуминами крови.
- •18)Биосинтез жиров в печени
- •20)Взаимопревращения разных классов липопротеинов , физиологический смысл процессов
- •Вопрос 26. Обмен жирных кислот, -окисление как специфический путь катаболизма жирных кислот, химизм, ферменты, энергетика.
- •Вопрос 27. Судьба ацетил-КоА
- •Вопрос 28. Локализация ферментов -окисления жирных кислот. Транспорт жирных кислот в митохондрии. Карнитин-ацилтрансфераза.
- •Вопрос 29. Физиологическое значение процессов катаболизма жирных кислот.
- •Вопрос 30. Биосинтез пальмитиновой жирной кислоты, химизм, жирнокислотная синтетаза.
- •Вопрос 32. Биосинтез ненасыщенных кислот. Полиненасыщенные жирные кислоты.
- •Вопрос 33. Биосинтез и использование ацетоуксусной кислоты, физиологическое значение процессов. К кетоновым телам относят три вещества: β-гидроксибутират, ацетоацетат и ацетон.
- •Синтез кетоновых тел:
- •Окисление кетоновых тел:
- •Вопрос 34. Обмен стероидов.Холестерин как предшественник других стероидов.Биосинтез холестерина. Обмен стероидов
- •Вопрос 35.Регуляция биосинтеза холестерина, транспорт холестерина кровью.
- •36. Роль лпнп и лпвп в транспорте холестерина.
- •37. Превращение холестерина в желчные кислоты, выведение из организма х и жк.
- •38. Конъюгация желчных кислот, первичные и вторичные жк
- •39. Гиперхолестеринэмия и ее причины.
- •40. Биохимические основы развития атеросклерохза. Факторы риска.
- •41. Биохимические основы лечения гиперхолестеролемии и атеросклероза
- •42. Роль омега-3 жирных кислот в профилактике атеросклероза (тупой! Тупой вопрос! Будь он проклят. Ничего нормального не нашел…что-то нарыл в интернете)
- •43. Механизм возникновения желчнокаменной болезни
- •44. Биосинтез глицеролфосфолипидов в стенке кишечника и тканях (тоже как-то не очень…что нашел, пардон)
- •46. Катаболизм сфинголипидов. Сфинголипидозы. Биосинтез сфинголипидов.
- •47. Обмен безазотистого остатка аминокислот, гликогенные и кетогенные аминокислоты
- •48. Синтез глюкозы из глицерина и аминокислот.
- •49. Глюкокортикостероиды, строение, функции, влияние на обмен ве¬ществ. Кортикотропин. Нарушение обмена при гипо- и гиперкортицизме (стероидном диабете).
- •50. Биосинтез жиров из углеводов
- •51. Регуляция содержания глюкозы в крови
- •52. Инсулин, строение и образование из проинсулина. Изменение концентрации в зависимости от режима питания
- •53. Роль инсулина в регуляции обмена углеводов, липидов и аминокислот.
- •54. Сахарный диабет. Важнейшие изменения гормонального статуса и обмена веществ.
- •55. Патогенез основных симптомов сахарного диабета.
- •56. Биохимические механизмы развития диабетической комы.(я не уверена что правильно)
- •57. Патогенез поздних осложнений сахарного диабета (микро- и макроангиопатии, ретинопатии,нефропатия,катаракта)
Вопрос 29. Физиологическое значение процессов катаболизма жирных кислот.
Реакции β-окисления и последующего окисления ацетил-КоА в ЦТК служат одним из основных источников энергии для синтеза АТФ по механизму окислительного фосфорилирования. Образуется ацетил-КоА, а он нужен для синтеза важных вещ-в (кетоновые тела, холестрин, жирные кислоты). Идет в ЦТК –при этом образуется 12 АТФ.
Нарушения окисления жирных кислот.
У людей с наследственными дефектами карнитинацилтрансферазы I или ферментов синтеза карнитина в скелетных мышцах снижается скорость поступления жирных кислот в матрикс митохондрий и, соответственно, скорость β-окисления. В этих случаях жирные кислоты с длинной цепью не используются как источники энергии. У таких людей снижена способность к физической активности; в шишечных клетках могут накапливаться жиры, образуя вакуоли.
Генетический дефект дегидрогеназы жирных кислот со средней длиной углеводородной цепи
В митохондриях имеется 3 вида ацил-КоА-дегидрогеназ, окисляющих жирные кислоты с длинной, средней или короткой цепью радикала. Жирные кислоты по мере укорочения радикала в процессе β-окисления могут последовательно окисляться этими ферментами. Генетический дефект дегидрогеназы жирных кислот со средней длиной радикала наиболее распространён по сравнению с другими наследственными заболеваниями. Активность этой дегидрогеназы особенно важна для грудных детей, у которых жиры молока служат основным источником энергии, а в триацилглицеролах молока преобладают жирные кислоты со средней длиной цепи. Невозможность использовать жирные кислоты как источники энергии приводит к увеличению скорости окисления глюкозы. В результате у детей развивается гипогликемия - причина внезапной детской смертности (10% от общего числа умерших новорождённых). Если такие дети выживают, то после голодания в течение 6-8 ч у них развиваются гипогликемические приступы (слабость, головокружение, рвота, потеря сознания). Введение глюкозы приводит к исчезновению симптомов.
Во всех случаях, когда нарушается β-окисление, жирные кислоты накапливаются в клетках и распадаются по пути ω-окисления, которое в норме идёт с очень низкой скоростью. Окисление происходит по метильному ω-атому углерода и в результате образуются дикарбоновые кислоты, выделяющиеся с мочой. Определение этих кислот в моче может служить диагностическим признаком нарушения β-окисления.
Нарушение окисления фитановой кислоты. При редком наследственном заболевании - болезни Рефсума, развивающейся вследствие генетического дефекта одного из ферментов, участвующих в α-окислении, фитановая кислота, поступающая с пищей, не окисляется и накапливается в организме, в основном в нервной ткани. Это приводит к нарушению структуры нервной ткани и развитию многих неврологических симптомов.
Вопрос 30. Биосинтез пальмитиновой жирной кислоты, химизм, жирнокислотная синтетаза.
1)Образование ацетил-КоА и его транспорт в цитозоль
Синтез жирных кислот происходит в абсорбтивный период. Активный гликолиз и последующее окислительное декарбоксилирование пирувата способствуют увеличению концентрации ацетил-КоА в матриксе митохондрий. Так как синтез жирных кислот происходит в цитозоле клеток, то ацетил-КоА должен быть транспортирован через внутреннюю мембрану митохондрий в цитозоль. Однако внутренняя мембрана митохондрий непроницаема для ацетил-КоА, поэтому в матриксе митохондрий ацетил-КоА конденсируется с оксалоацетатом с образованием цитрата при участии цитратсинтазы:
Ацетил-КоА + Оксалоацетат -> Цитрат + HS-КоА.
Затем транслоказа переносит цитрат в цитоплазму .
Перенос цитрата в цитоплазму происходит только при увеличении количества цитрата в митохондриях, когда изоцитратдегидрогеназа и α-кетоглутаратдегидрогеназа ингибированы высокими концентрациями NADH и АТФ. Эта ситуация создаётся в абсорбтивном периоде, когда клетка печени получает достаточное количество источников энергии. В цитоплазме цитрат расщепляется под действием фермента цитратлиазы:
Цитрат + HSKoA + АТФ → Ацетил-КоА + АДФ + Pi + Оксалоацетат.
Ацетил-КоА в цитоплазме служит исходным субстратом для синтеза жирных кислот, а окса-лоацетат в цитозоле подвергается следующим превращениям (см. схему ниже).
Пируват транспортируется обратно в матрикс митохондрий. Восстановленный в результате действия малик-фермента NADPH используется как донор водорода для последующих реакций синтеза жирных кислот. Другой источник NADPH - окислительные стадии пентозофосфатного пути катаболизма глюкозы..
Образование малонил-КоА из ацетил-КоА - регуляторная реакция в биосинтезе жирных кислот.
2)Первая реакция синтеза жирных кислот - превращение ацетил-КоА в малонил-КоА. Фермент, катализирующий эту реакцию (ацетил-КоА-карбоксилаза), относят к классу лигаз. Он содержит ковалентно связанный биотин (рис. 8-36). В первой стадии реакции СО2 ковалентно связывается с биотином за счёт энергии АТФ, во второй стадии СОО- переносится на ацетил-КоА с образованием малонил-КоА. Активность фермента ацетил-КоА-карбоксилазы определяет скорость всех последующих реакций синтеза жирных кислот.
Реакция протекает в два этапа: I – карбоксилирование биотина с участием АТФ и II – перенос карбоксильной группы на ацетил-КоА, в результате чего образуется малонил-КоА:

Реакции, катализируемые синтазой жирных кислот, - ферментным комплексом, катализирующим реакции синтеза пальмитиновой кислоты, описывается ниже.
После
образования малонил-КоА синтез жирных
кислот продолжается на мультиферментном
комплексе - синтазе жирных кислот
(пальмитоилсинтетазе). Этот фермент
состоит из 2 идентичных протомеров,
каждый из которых имеет доменное строение
и, соответственно, 7 центров, обладающих
разными каталитическими активностями
(рис. 8-37). Этот комплекс последовательно
удлиняет радикал жирной кислоты на 2
углеродных атома, донором которых служит
ма-лонил-КоА. Конечный продукт работы
этого комплекса - пальмитиновая кислота,
поэтому прежнее название этого фермента
- пальмитоилсинтетаза.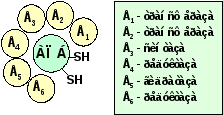
Биосинтез по порядку:

Далее цикл реакций повторяется. Допустим, что идет синтез пальмитиновой кислоты (С16). В этом случае образованием бутирил-АПБ завершается лишь первый из 7 циклов, в каждом из которых началом является присоединение молекулы малонил-АПБ к карбоксильному концу растущей цепи жирной кислоты. При этом отщепляется дистальная карбоксильная группа малонил-АПБ в виде СО2.
Например, образовавшийся в первом цикле бутирил-АПБ взаимодействует с малонил-АПБ:
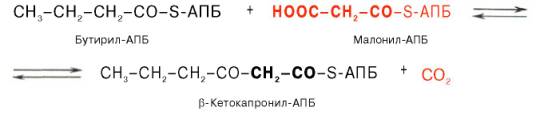
Вопрос 31.Биосентез жирных кислот с длинной цепью углеводных атомов(С18 и больше С-атомов) Синтез жирных кислот протекает в цитоплазме клетки. В митохондриях в основном происходит удлинение существующих цепей жирных кислот. Установлено, что в цитоплазме пече-ночных клеток синтезируется пальмитиновая кислота (16 углеродных атомов), а в митохондриях этих клеток из уже синтезированной в цитоплазме клетки пальмитиновой кислоты или из жирных кислот экзогенного происхождения, т.е. поступающих из кишечника, образуются жирные кислоты, содержащие 18, 20 и 22 углеродных атома. Первой реакцией биосинтеза жирных кислот является карбоксилирование ацетил-КоА, для чего требуются бикарбонат, АТФ, ионы марганца. Катализирует эту реакцию фермент ацетил-КоА-кар-боксилаза. Фермент содержит в качестве простетической группы биотин. Реакция протекает в два этапа: I – карбоксилирование биотина с участием АТФ и II – перенос карбоксильной группы на ацетил-КоА, в результате чего образуется малонил-КоА. Малонил-КоА представляет собой первый специфический продукт биосинтеза жирных кислот. В присутствии соответствующей ферментной системы малонил-КоА быстро превращается в жирные кислоты. Последовательность реакций, происходящих при синтезе жирных кислот: