
Лекция 2
Равновесия в системах «насыщенный раствор - осадок» Механизм образования осадков
На первый взгляд образование осадков идет по одинаковому механизму:
Ag++Cl-→AgCl↓
Ba2++SO42-→BaSO4↓
На самом деле осадки AgCl↓ и BaSO4↓ состоят из отдельных кристаллов, включающих в себя огромное число ионов, расположенных строго определенным образом.
Рассмотрим механизм образования осадков. Образование осадков происходит в пересыщенных растворах в несколько стадий:
Индукционный период – время до появления первых признаков осадка. Величина этого периода зависит от химической природы образующегося осадка (при осаждении BaSO4 индукционный период сравнительно велик, при осаждении AgCl – очень непродолжительный), концентрации реагентов, чистоты реагентов и т.д. Процесс образования осадка начинается с возникновения первичных центров кристаллизации (первичных зародышей), которое может быть спонтанным (гомогенным) или индуцированным (гетерогенным) В первом случае в растворе образуется группа ионов, размер которой превышает некоторую критическую величину. Во втором случае образование первичного зародыша происходит в результате адсорбции ионов на поверхности посторонней частицы (пылинки). Гетерогенный механизм образования центров кристаллизации встречается чаще, чем гомогенный.
Процесс образования первичного зародыша можно представить следующим образом:
Ag++Cl-→AgCl
AgCl +Ag+→(Ag2Cl)+
(Ag2Cl)++Cl-→(AgCl)2
До тех пор, пока не образуется (AgCl)n. Размер критического зародыша, т.е. величина n, зависит от природы ионов и составляет от 2 до 9. Частицы, содержащие меньше ионов, чем критический зародыш, склонны к разрушению и растворению.
Рост кристаллов. Укрупнение частиц осадка включает в себя такие процессы, как диффузия ионов к поверхности осадка, адсорбция их на поверхности и включение в кристаллическую решетку. Образующиеся осадки могут быть кристаллическими или аморфными. Большинство аморфных осадков также имеют кристаллическую структуру, но состоят из множества слабо связанных между собой очень маленьких кристаллов.
Характер образующегося осадка определяется соотношением скоростей двух процессов: образования зародышей и роста первичных центров кристаллизации, а это соотношение зависит от относительного пересыщения (ОП) раствора, возникающего при добавлении раствора осадителя:
ОП = (Q - S) /S,
где Q - концентрация осаждаемого вещества в какой-либо момент времени; S – концентрация осаждаемого вещества в насыщенном растворе (растворимость).
Скорости процессов образования первичных зародышей и роста кристаллов связаны с ОП уравнением:
=k(ОП)n
Для образования зародышей n=4, для роста кристаллов n=1. Однако k для процесса кристаллизации больше.
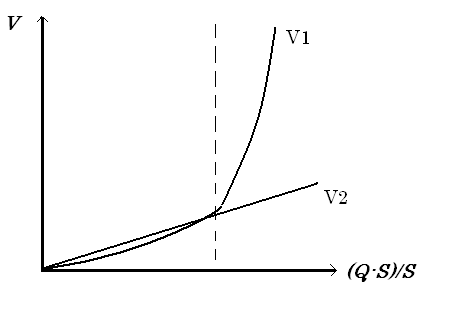
При малых значениях ОП преобладает рост кристаллов, вследствие чего образуется малое количество крупных кристаллов, при больших – образование новых первичных центров кристаллизации, поэтому образуется множество мелких кристаллов.
Послеосаждение. Это образование второго малорастворимого соединения на поверхности уже образовавшегося первого осадка. При осаждении ионов кальция из раствора, содержащего ионы кальция и магния действием раствора оксалата, первым выпадает осадок CaC2O4, а Mg2+ остается в растворе в пересыщенном состоянии. Через некоторое время на поверхности CaC2O4 осаждается MgC2O4.
Старение осадка. Совершенствование его структуры:
Рекристаллизация первичных частиц – перенос вещества от мелких частиц к более крупным после растворения мелких;
Термическое старение – совершенствование структуры за счет теплового движения;
Соединение мелких частиц в более крупные (агломераты);
Переход от аморфного осадка к кристаллическому при повышении температуры смеси.
