

Раздел 11
ХИМИЧЕСКАЯ КИНЕТИКА
ГЛАВА 1 . ОСНОВНЫЕ ПОНЯТИЯ
§ l . ВВЕДЕНИЕ
Для исследования химических процессов применяют обыч но дВ<l метод<1: термодинамический и кинетический.
Пример 1.1. Для ;щлотропного превр<1щения Сrр = Салм найдено, что ! J . Gт = О при 1 500оС и Р = 36000 атм, т.е. при этих условиях возможен переход графит<1 в <1лмаз. Однако скорость превращения настолько м;щ<l, что процесс практически не идет. Таким образом, относительно хорошие термодинамические вы ходы часто кинетически не ре;щизуются.
Поэтому при изучении разли<шых химических процессов в природе и технике наряду с примененисм основных соотноше ний термодин<1мию1 нужно хорошо понИМ<lТЬ и умело применять основные законы и уравнения химической кинетики.
|
§ |
|
СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ |
С к оростью х и м и ч е с ко й р е <1 к ц и и в газах и раство |
|||
р<1Х принято |
назыв<1ть изменение количества любого из реагирую |
||
|
2. |
|
|
щих веществ в единицу времени в единице объема. В качестве из
менения количества вещества в химической кинетике обычно ис пользуют изменение числа молей n. Скорость реакции при посто янных внешних условиях (р, Т и др.) не остается постоянной, а
изменяется со временем. По мере изр<1сходования исходных ве |
|
ществ чаще всего скорость реакции уменьшается (рис. 63). |
|
Средней скоростью w за определенный промежуток вре |
|
мени t t0 для реакции |
|
А _, В |
(1 . 1) |
Н<lЗЬШ<lЮТ отношение конечного изменения количества вещества одного из реагирующих веществ в единице объема к промежутку
времени:
v = |
1 |
(п - n0) |
. |
( 1 .2) |
|
± - |
t - t0 |
|
|
|
V |
|
|
|
Это выражение l\1ожно записать иначе:
1 70

t
Рис.бЗ. Изменение скорости реакции
со временем
Рис.64. Изменение конuентраuии ел и
сн со временем в реакции А В
|
w |
|
v |
- |
• |
= |
|
1 |
6n |
||
= |
± - |
= - !0 |
|||
|
|
|
|
м |
|
где дп |
n - n0; |
дt |
t |
|
|
Если отнести изменение числа молей к бесконечно малому промежутку времени, то в пределе, когда дt будет стремиться к нулю, получим уравнение
1 dn |
( 1 .4) |
- v dt ' |
|
W = + - - |
|
которое является математическим выражением для истинной ско
рости реакции в данный момент времени. |
|
|
||
Скорость любой реакции, записанной в общем виде: |
|
|||
v1B1 |
v2B2 + . v' 1B' 1 + v'2B 2 . . |
, |
( 1 .5) |
|
можно измерять+как по изменению. . |
количества' + . |
любого из исход |
||
ных веществ, так и по изменению количества любого из продук
тов реакции в единицу времени в единице объема. Поскольку ско
рость реакции принято считать всегда положительной величиной,
то для однозначного определения ее пользуются следующим вы
ражением:
|
|
|
- - - |
|
- - |
|
. |
|
. jV |
- - - . . |
|
. . • |
|
||||||||
v |
w |
= |
|
1 |
dn1 |
|
1 |
dllj |
= |
|
|
1 |
dnj |
|
1 |
dn]. |
= |
|
|
||
|
|
|
= - |
|
|
|
. |
= - |
|
= |
|
|
B l ' |
|
( 1 .6) |
||||||
|
|
|
|
v1V |
dt |
|
v2V |
dt |
|
|
|
v |
dt |
|
v2V dt |
|
|
|
|
||
где 1 |
и nl' v2 и n2 относятся к исходным веществам |
|
В2, |
|
, а v'1 |
||||||||||||||||
и n, 1 , |
v,2 |
и n |
,2 • . • |
- к продуктам реакции В' 1, |
В'2, |
. • . |
|
|
|
|
|
||||||||||
В замкнутой системе, в которой объем не меняется, n/V = ci'
так что выражения средней и истинной скоростей для реакции ( 1 . 1) приобретают вид
1 7 1

w
w
= + -
= ±
6с 6t
dc
- .
dt
,
Скорость любой реакции общего типа (уравнение 1 .5) при посто янном объеме выразится следующим соотношением:
|
1 |
dc1 |
1 |
dc2 |
w |
= - - - = - - - |
|||
v1 |
dt |
v2 |
dt |
|
1 |
dc] |
1 |
dc]. |
= - . . . = -v; |
-dt |
= -v2 |
--dt = . . . (l .ба) |
На рис. 64 изображена зависимость концентраций исходного вещества А и конечного продукта реакции В от времени для односторонней реакции (1 . 1). О д н о с т о р о н н и м и реакциями называют реакции, идущие до конца в одном направлении.
Если же объем в системе меняется, например при реакциях в потоке, то
1 |
dn |
dc |
' |
( 1 .7) |
V |
dt |
dt |
||
W = ± - - 7 ' ±- |
|
|||
поскольку |
|
|
|
|
|
|
|
|
( 1 .8) |
С учетом этого уравнения получим в общем случае опреде ление истинной скорости реакции, пригодное для систем с по
стоянным и переменным объемами:
1 |
dn |
dc |
n |
dV |
( 1 .9) |
v |
dt |
dt |
v2 |
dt |
|
W = - - |
= - + - - . |
||||
Естественно, что при V = const (dV = О) находим: w |
dc |
||||
dt . |
|||||
|
|
|
|
|
= - |
При изложении основных положений химической кинетики мы будем в дальнейшем исследовать преимущественно реакции,
происходящие без изменения объема в системе, т.е. реакции в
замкнутом объеме или в потоке без изменения числа молей в реакции (когда объем также не меняется). Поэтому без системати ческих оговорок будем использовать для обозначения скоростей
реакций выражения типа ( 1 .6а).
|
§ 3. ОСНОВНОЙ ПОСТУЛАТ ХИМИЧЕСКОЙ КИ НЕТИКИ |
||
|
Х и м и ч е с к о й |
к и н е т и к о й называют учение о скоростях |
|
|
механизмах. М е х аих |
зависимости от различных факторов и об |
|
химических реакций , |
|||
их |
|
н и з м о м х и м и ч е с к о й р е а к ц и и назы- |
|
1 72
вают обычно совокупность элементарных процсссов, через кото рые проходит эта реакция.
Согласно о с н о в н о м у п о с т ул а ту х и м и ч е с к о й к и н с т и к и : "скорость химической реакции (при постоянном объе
ме) пропорциональна произведению текущих концентраций ис ходных веществ, возведенных в некоторые степени".
Для реакции вида ( 1 .5) аналитическим выражением этого
постулата будет уравнение: |
|
|
||
и; = - _!_ dc; = |
_!_ dcj |
= kcPcq с . . . |
( 1 . 1О) |
|
1 dt |
1 dt |
|
· |
|
Этот постулат был |
использован К.Гульдбергом и |
П .Вааге |
||
1 2 |
|
|
||
при выводе vзакона |
действующих масс, почему его иногда непра |
|||
v |
|
|
|
|
вильно называют законом действующих масс. Ясно, что в форме
уравнения |
постулат имеет силу только для реакций, проте |
|
кающих при( 1 .постоянном1О) |
объеме в системе. |
|
Коэффициент пропорциональности k, называемый к о н |
||
с т а н т о й |
с к о р о с т и р е а к ц и и , есть скорость реакции при |
|
концентрациях всех исходных веществ, равных единице1 • Для ка ждой реакции при постоянной температуре существует одно оп ределенное значение константы скорости.
§ 4. ПОНЯТИЕ О ПОРЯДКЕ И МОЛЕКУЛЯРИОСТИ РЕАКЦИ Й
Величины р, q, r в уравнении (1 . 10) называются порядками реакций по веществам, а сумма этих показателей:
p + q + r + ... = n
называется п о р яд к о м р е а к ц и и .
Порядки реакции по веществам могут принимать любые - целые и дробные, положительные и отрицательные - значения. Если сумма р + q + r + .. . = 1, то говорятО) о реакциях первого порядка. В этом случае уравнение ( 1 . 1 принимает вид:
( 1 . 1 0б)
При условии: р + q + r + ... = 2 имеют дело с реакцией второго порядка; если же р + q + ,. + ... = 3 - налицо реакция третьего порядка. Реакции более высоких порядков обычно не встречаются. В то же время в гетерогенных и фотохимических реакциях имеют место реакции нулевого порядка, когда скорость реакции не зависит от концентрации исходных веществ:
|
р е а к ц и и .с дан ны й |
|
нт ин |
|
ывается |
|
д ел ь |
н о й1 Вс к о р о с т ь ю |
коэффицие |
|
|
||||
связи с этим в литераrур |
|
огда наз |
|
у |
|
||
1 73

W = f<!o) ' |
( l . I Oв) |
идаже дробного порядка.
Вкаждом отдельном случае порядок реакции находится из
опытных данных и не всегда совпадает с м о л е к ул я р н о с т ь ю |
|||
в реакцию. |
v, |
определяемой просто числом молекул, вступающих |
|
р е а к ц и и |
|
||
|
Для реакции типа ( 1.5) молекуляриость реакции равна: |
||
|
V = L:v' = V1 + V,. + . . . . |
( 1 . 1 1) |
|
В зависимости от числа v реакции называются мономолекуляр ными, бимолекулярными или тримолекулярными. Например, ре акция
6FeCl2 + КСЮ3 + бНСl = 6FeCl3 + KCl + ЗНр
отвечает третьему порядку, хотя в ней реагируют 13 молекул. Лишь в случае элементарных (одностадийных) реакций порядок реакции совпадает с ее молекулярностью. Например, реакции омыления сложных эфиров щелочами типа
снзсоос2н5 + NaOH = СНЗСООNа + с2нрн
являются бимолекулярными, подчиняюшимися уравнениям ре акций второго порядка.
§5. ВЛИЯН И Е ТЕМПЕРАТУРЫ НА СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ
Вбольшинстве случаев скорость химической реакции увели чивается при повышении температуры. Я.Вант-Гофф показал, что
при повышении температуры на 10° скорость гомогенных реак ций увеличивается в 2-4 раза. Изменение концентраций и пока зателей степеней в уравнении ( 1 . 10) столь незначительно, что ими можно пренебречь по сравнению с изменением константы
скорости реакции. В связи с этим температурным коэффициентом
скорости реакции называют отношение констант скорости данной реакции при температурах ( Т + 10) К и ТК, т.е.
у = |
kT+IO |
. |
( 1 . 12) |
|
kт |
|
|||
Вант-Гофф нашел, |
что для большинства реакций у 3. Это озна |
|||
чает, что при31изменении0 температуры на l00° скорость реакции
изменится в = 59049 раз.
Для разных реакций величина у меняется в небольших пре делах, однако для большинства реакций было обнаружено, что
температурный коэффициент скорости реакции уменьшается обычно с ростом температуры.
1 74

§ 6. УРАВН ЕНИЕ АРРЕ НИУСА. Э Н ЕРГИЯ АКТИВАЦИИ
Более общую зависимость константы скорости от темпера
р а в н е н и е Ар р |
с |
н и у с а : |
туры дает у d ln k |
( 1 . 1 3) |
|
dT |
|
|
где ЕА - так называемая энергия активации. После интегрирова
ния этого уравнения получают зависимость k от Т в явном виде:
lв k |
Е |
|
const, |
|
|
( 1 . 1 4) |
|
R T |
|
|
|
|
|
удобную для определения из опытных данных (рис.65). |
||||||
|
= - А |
+ |
|
|
|
|
Э н е р г и е й а кт и в аЕАц и и на |
ln 1<. |
|
|
|||
зывают обычно избыток энергии по |
|
|
||||
|
|
|||||
сравнению со средней энергией реа- |
|
|
||||
гирующих веществ , |
необходимый |
|
|
|||
для того, чтобы между этими веще |
А |
|
|
|||
ствами с заметной скоростью про |
|
|
||||
щла химическая реакция. Энергия ак |
|
|
|
|||
тивации (как любая энергетическая |
|
|
|
|||
величина) измеряется в Дж/моль од |
|
|
|
|||
ного из прореагировавщих веществ |
|
|
1/Т |
|||
или продуктов реакции. |
|
|
|
|||
|
|
|
||||
Ее величина зависит от вида |
|
|
||||
реагирующих |
веществ (молекулы , |
Рис . б S .Зависимость логарифма |
||||
радикалы, атомы, ионы и т.п.). Так, |
константы скорости реаiО.(ИИ от |
|||||
о |
обратной температуры |
|||||
для реак ц и й |
между вал е н т н о - |
|
|
|||
|
|
|
||||
насыщенными молекулами энергии активации близки по величине к их энергиям диссоциации и
составляют величины порядка 1 00 - 200 кДж/моль. Реакции между валентно-ненасыщенными атомами или рад икалам и происходят с энергиями активации, близкими к нулю, реакции атомов (или радикалов) с молекулами идут с промежуточными
значениями э нергии активации (порядка 40 - 100 кДж/моль).
Пример 1.2. Для реакции диссоциации
2HI Н2 + 12
найден ы следующие значения констант скорости при разных тем
пературах: |
|
|
|
|
Т, К |
647 |
683 |
7 1 6 |
7 8 1 |
k (л/моль·мин) |
5, 16· Iо-з |
3,07· 1 0·2 |
0, 1 5 |
2,38 |
Определить энергию активации этой реакции.
175

lnk
-ц -6
r,z |
r,ц |
t,б |
(t,1т)
·taJ
Рис.бб. Зависимость ln k от !/ТдЛЯ реакции 2HI Н2 + 12
Решение. Как следует из уравнения ( 1 . 14), энергию актива ции можно определить: а) графически , построив зависимость ln k = 1{1/1); б) с помощью практически любого компьютера (или калькулятора), использующего метод наименьших квадратов.
Для наглядности nроведем расчет графическим способом. С этой целью nредварительно вычислим значения 1/Т и ln k:
( 1/1)· 103 |
|
1 , 575 |
|
|
|
1,464 |
|
|
1 ,398 |
1,280 |
|||
ln k |
-5,267 |
|
|
|
-3,484 |
|
|
- 1 ,898 |
0, 868 |
||||
и построим зависимость ln k = / ( 1/ 1 ) (рис .66). |
|
|
|||||||||||
Из рисунка 66 |
находим: |
|
|
|
|
|
|
||||||
|
|
|
- |
R tg a . |
= |
|
0,868 |
|
5,267)1 0 |
3 |
|
||
|
|
|
|
|
|
-----'-- |
|
||||||
|
ЕА = |
|
|
|
|
-8,3 14 ( |
+ |
|
|
|
|
||
|
|
|
|
|
6 135 |
1,280 - 1,575 |
|
|
|||||
|
|
|
|
|
= 8,3 14 О,295 = 1 72,9 кДж/моль. |
|
|||||||
Если уравнение ( 1 . 13) nроинтегрировать в небольтих пре |
|||||||||||||
делах от т! |
ДО |
т , когда можно принять, |
что |
ЕА = const, |
получим |
||||||||
выражение: |
2 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
( 1 . 1 5) |
удобное для вычисления значений констант скорости при неко
торых температурах |
т;, |
если известны значения |
kт, |
и |
ЕА |
для этой |
|
|
|
|
|||||
реакции. |
|
|
|
|
|
|
|
Если же из уравнения ( 1 . 1 5) получить выражение |
|
||||||
ЕА |
RTIT2 |
ln kт2 |
|
|
|
|
|
= Т2 - Т1 |
kт1 , |
|
|
|
( 1 . 16) |
||
его можно использовать для аналитического определения энергии
активации, особенно при небольтом числе экспериментальных
данных.
176

Энергия активации имеет большое значение при анализе геохимических процессов. Так, чем ниже значение энергии акти вации реающи разложения в ряду подобных минералов, например карбонатов, тем больше возможность перехода катионов Zп2' , Fe2+ , Mll2• под влиянием гидротермальных растворов в подвиж ное равнов{;сис и тем больше возможность отложения их в виде изоморфных сфалеритов (ZnS, FeS, MnS). Ниже приводятся зна чения энергии активации процессов разложения некоторых кар бонатов:
МеС03 |
MnC03 |
ZлС03 |
|
ЕА, кДж/моль |
94 |
67 |
|
§ 7. ПОНЯТИЕ ОБ АКТИВНЫХ СТОЛКНОВЕ Н ИЯХ |
|
||
Каждая химическая реак:ция между одинаковыми |
раз |
||
ИJIИ
личными веществами начинается, естественно, со столкновения двух частиц. Однако, как показывают опыты, число прореагиро вавших частиц (молекул, ионов и т.п.) при не очень высоких тем пературах на много порядков ниже числа сталкивающихся частиц. Так, например, в реак:ции
NOC1 + NOC1 = 2NO + С12
при 529 К и 1 атм образуется примерно 2· 10·" юля NO в 1 см3 в 1 с. Расчет полного числа столкновений при этих условиях приводит к значениям порядка 105 молей NOC1jcм3·c.
Таким образом, если обозначить буквой z число обших столкновений, а символом z. -- число активных столкновений, приводящих к реакции, получим для указанной реак:ции, что
z, /z = 1Q-11,
т.е. активным столкновением будет только одно из 1011 общих столкновений.
Расхождения между значениями z. и z и привели Аррениуса к выводу о том, что в реакцию могут вступать только молекулы, обладающие определенным избытком энергии (энергии актива ции).
Теория столкновений приводит к следующему соотноше нию между z. и z :
(1 . 17)
в котором учтена зависимость z от T(z = A Гi2n2). Здесь n - число
молскул в 1 см3; Е. - так называемая "классическая" энергия
аJ'...Тивации, равная разности между потенци:L'lьными энергиями активных и исходных молекул:
1 77
1 2 Зак. 3 1 47
Eа = Uз - Uисх . |
( 1 . 1 8) |
Сопоставляя уравнения ( 1 . 14) и ( 1 . 17) (с учетом того , что za=kn2), находим:
( 1 . 1 9)
После логарифмирования и дифференцирования по температуре этого уравнения найдем :
d ln k |
1 |
--Еа. 2 |
,i RT |
--- |
= - + |
Е. + - |
|
|
= |
2 |
|
dT |
2Т |
RT |
RT2 |
( 1 . 1 9а)
откуда получим связь "классической" с опытной (аррениусов екай) энергией активации:
( 1 .20)
ГЛАВА 2. КИНЕТИКА ГОМОГЕННЫХ ХИМИЧЕСКИХ
РЕАКЦИЙ
§1. ОДНОСТОРОННИЕ РЕАКЦИ И ПЕРВОГО ПОРЯДКА
Исследуем сначала закономерности, относящиеся к ско ростям односторонних реакций разных порядков, причем для простоты будем рассматривать реакции , происходящие независи мо одна от друтой. Кроме того, примем температуру и объем сис
темы в течение всей реакции неизменными.
Начнем исследование с простейших односторонних реак ций первого порядка типа ( 1 . 1 ):
Сэтой целью перепишем уравнение ( 1 . 10) в виде
|
|
_ dc = klc' |
(2. 1 ) |
||
|
с |
- |
dt |
|
|
в котором |
текущая (в дан ный момент времени) |
концент- |
|||
|
|||||
рация вещества А в системе.
Разделив персменные в этом уравнении:
_dc = edr' dc
иинтегрируя полученное соотношение, найдем :
1 78

l п с |
-k1t + const. |
t = |
|
|
(2.2) |
||
тогда |
|
находим из условия : |
|
с |
= |
с0, |
|
Постоянную интегрирования= |
|
О, |
|
||||
ln с0 = const, |
|
|
|
|
(2.3) |
||
откуда |
|
|
|
|
|
|
|
ln с = - k1t + ln с0• |
|
|
|
|
|
||
Окончательно получаем выражение |
|
|
|
|
|
||
k l = ! ln Со |
|
|
|
|
(2.4) |
||
t |
с • |
|
|
|
|
|
|
необходимое для вычисления константы скорости односторонней реакции первого порядка.
Из уравнения (2.4) видно, что размерность константы ско рости реакции первого порядка выражается через обратное вре-
мя : |
|
dim{ k'} = (с- 1 , мин - 1, • • • , год· 1). |
(2.5) |
С другой стороны, поскольку в уравнение (2.4) |
входит от |
ношение концентраций, значение k не изменится, если это отно шение заменить отношением других величин, пропорциональных концентрациям , например, отношением числа молей, молекул , миллилитров, миллиметров ртутного столба и т.п. Тогда получим в обшем случае:
е = ! ln c0 |
= ! ln n° |
= ! ln N° |
' |
(2.6) |
|||
t |
с |
t |
n |
t |
N |
|
|
где n - число молей; N - число молекул вешества А, вступающих |
|||||||
в реакцию ( 1 . 1) . |
|
|
|
|
|
|
|
Из уравнения (2.6) |
можно вычислить концентрации (коли |
||||||
чества) веществ А и В, остающихся (А) и образующихся (В) к определенному моменту времени. Действительно, после потенци рования этого уравнения находим:
(2.7)
(2.8)
Здесь с - текущая концентрация вещества А, а (с0 - с) - кон
центрация вещества В, р:шная концентрации прореагировавшего |
|||||||||
вещества А. |
|
|
|
|
|
|
|||
|
- |
На |
рис.67 изображены экспоненциа.пьные зависимости с и |
||||||
|
|
||||||||
с0 |
от времени. |
|
|
|
|
|
|
||
|
сВ точке пересечения кривых (с0 - с) |
|
следовательно, в |
||||||
этой точке с = с0/2 . Вре |
мя , |
в |
|
которого прореагирует поло- |
|||||
1 2* |
|
|
|
|
течение |
|
= с, |
1 79 |
|

с
Рис.б7. Зависимость с и С0 - с от времени в односторонней реакции первого порядка
вина исходного вещества А, называют временем полупревраще
ния, а в случае реакций первого порядка - п е р и о д о м п о л у
Р а с п а д а (по аналогии с распадом радиоактивных веществ, под
чиняющихся реакциям первого порядка).
Полагая в уравнении
1112 = |
ln 2/k |
' |
|
(2.4) t = 0,693
= /k
-rl/2 и
',
с = crJ2, находим:
(2.9)
откуда
k' = 0,693jr112 , |
(2.9а) |
т.е. константа скорости реакции первого порядка обратно пропор цианальна периоду полураспада.
Из уравнения (2.9) видно, что в реакциях первого порядка (и только в н их) период полураспада (время полупревращения)
не зависит от концентрации исходного вещества. |
||||
Пример 2.1. За 14 дней а |
ность 210Ро уменьшилась на 6,85%. |
|||
Определить з начения |
k1, 1 1/2 и t (время) , в течен ие которого |
|||
полоний распадается на 90%ктив. |
|
|||
Решение. |
И з условий задачи N1 = 0,93 15N0, поэтому из урав |
|||
нения (2.6) |
|
|
|
|
k1 = _ ! lп NQ . =_!_ In |
No |
= 5 07 - 10-3 дней·1 , |
||
t1 |
N1 |
14 |
0,93 1 5N0 |
' |
а из уравнения (2.9) следует, |
что |
|
||
' |
J |
2 |
0,693 |
|
0,693 |
- I Оз |
= 13 |
7 дней . |
|
|
|
|
|
|
|||||
|
f |
|
k' |
|
5,07 |
|
|
||
Если теперь записать уравнение |
(2.6) относительно t, получим |
||||||||
выражение |
|
|
|
|
|
|
|||
|
|
|
t |
= |
1 |
l п |
No . |
|
|
|
|
|
|
k' |
|
N |
|
|
|
Из условия задачи при t2 = ? |
N2 |
= |
О, 1 О N0, |
поэтому |
|||||
1 80

k ' |
N |
|
= |
_!_Q3 |
__ |
|
o |
= |
454 |
|
|
t2 = 1 |
o |
|
|
In |
N |
дня. |
|||||
- In |
|
|
5,07 |
|
|
|
|
||||
|
N |
|
|
0,10N0 |
|
|
|
||||
К числу односторонних реакций первого порядка относятся уже упоминавшисся реакции радиоактивного распада, реакции
разложения сложных веществ (карбонатов, кристаллоi11дратов и
т.п.) при их нагревании, реакции изомеризации и т.п.
§2. ОДНОСТОРОННИЕ РЕАКЦИ И ВТОРОГО ПОРЯДКА
Оскорости реакции второго порядка можн о судить по уменьшению концентрации одного из исходных веществ. В про стейшем случае, когда концентрации обоих исходных веществ А и
Вв реакции
A + B C + D |
(2 . 1 0) |
равны , согласно основному постулату химической кинетики за пишем:
w = - dc |
= k п с 2 . |
(2. 1 1) |
dt |
|
|
После разделения персменных
-dc = k 11dt (2. 1 1 а)
с2
иинтегрирования полученного дифференциального уравнения (2. 1 1 а) получим:
- = k /1t |
+ |
coпst. |
с |
|
|
1 |
|
|
Постоянная интегрирования определяется из условия: t = О, с = с0,
тогда
или
(2. 1 2)
Если вместо текущей концентрации исходного вещества с использовать в уравнении (2 . 12) ее убыль с = с0 - сх, можно прийти к уравнению вида:
k |
" |
= |
xc"- - |
,- |
|
|
|
lt с0 (с0 - с----х ) · |
(2. 13) |
1 8 1
Решая уравнение (2 . 1 2) относительно |
и |
- |
получим: |
|
соk t |
|
с с0 |
с, |
|
с = -----'---"11 ' |
|
(2 . 14) |
||
1 + c0 |
с2о k11t11t |
|
|
|
1 |
|
|
(2. 15) |
|
сх = Со - с = |
+ c0k |
|
|
|
Из уравнений (2. 1 2), (2 . 1 3) вытекает, что размерность кон -
станты скорости реакции второго порядка равна:
(2. 16)
Естественно, что в зависимости от используемых единиц измере ния времени (секунда, минута, ... , год) и концентрации (моль/л, моль/смЗ, молекулjсм3 и т.д.) численные значения констант ско рости реакции будут различаться на много порядков. Так, напри мер, константы скорости газовых реакций, представленные в таб лицах обычно в еди ницах "см3jмолекула·с " , отличаются на 22 порядка от тех же констант скорости , выраженных в единицах "лjмоль·мин " . Действительно:
k( |
л |
- 6,02 . 1023 |
. 60 k |
' |
|
см3 |
|
моль · мин ) |
|
1000 |
смз |
|
( молекула · с ) - |
||
|
= 3,6 - 1 022 k'( |
молекула · с |
). |
||||
(2. 17)
Время полупревращения любого исходного вещества (при равн ых начальных концентрациях) в реакциях второго порядка равно :
|
|
1 |
|
71/2 |
|
-- ' |
(2. 1 8 ) |
|
k с0 |
||
|
оно обратно пропорционально начальной кон |
||
откуда видно, что = |
|
|
|
центрации реагирующих веществ. |
|||
Пример |
Формальдегид окисляется перекисью водорода в |
||
муравьиную кислоту2.2. |
: |
- неоон + нр |
|
неон + нр2 |
|||
по уравнению реакций второго порядка. Если смешать равные
объемы молярных растворов Н202 и неон, то через 2 ч при 60°е
концентрация НеООН станет равной 0,2 1 5 моль/л. Вычислить
значения kп и 1 112 .
1 : : 1 2

Решение. Из условия задачи сх = 0 , 2 1 5 и с0 - сх =0,285 моль/л.
Из уравнения (2 . 1 3) находим:
k 11 |
= |
1 |
с |
х- сх) |
1 |
0,2 1 5 |
= |
|
-t |
с0(с0 |
2 0,500 · 0,285 |
||||
или , поскольку для реакций в растворах
0,75 л/моль·ч
kп чаше измеряется в
"л/моль· мин " , найдем:
k |
11 |
= |
0'75 = |
1 |
||
|
|
60 |
|
|||
Из уравнения (2 . 1 8) |
|
|||||
|
|
= -- = |
||||
Tl/2 |
|
|
l |
|
|
|
|
|
|
k |
|
c0 |
|
' |
25 · |
1 0- |
2 |
лjмоль·мин . |
||
|
|
|
||||
получим: |
|
|
|
|||
|
l 02 |
|
|
= \ 60 |
МИН . |
|
|
1 ,25 |
- 0,500 |
||||
Если начальные концентрации исходных веществ А и В раз личны и равны , соответственно, сд и с8, то для расчета констант скорости реакций второго порядка в этом случае применяют урав
нение
k u =
1 |
ln св(сл |
- сх) _ |
(2. 19) |
t(сл - с8) |
сд (св - сх) |
|
|
Реакций второго порядка из вестно очен ь много . Это - реакции образован ия и диссо циации йодисто го водорода, реакции о м ыления сложных эфиров шелочам и , реакции этерификации и т . п .
Реакции третьего порядка встречаются чрезвычайно редко. Наиболее типичными из них являются реакции взаимодействия оксида азота (II) с кислородом или галогенами, например:
2NO + 02 2N02•
Поэтому часто ограничиваются рассмотрением реакций первого
ивторого порядков.
§3. ПОНЯТИЕ О СЛОЖНЫХ РЕАКЦИЯХ. ПРИНЦИП НЕЗАВИСИМОСТИ
РЕАКЦИ Й
В природе и технике простые (односторонние) реакции на
блюдаются редко. Большинство р е а к ц и й являются с л о ж н ы м и , т.е. протекают в несколько элементарных стадий , которые идут одновременно (параллельно) или последовательно. При этом
некоторые стадии проходят с участием промежуточных веществ, не являющихся ни исходными веществами, ни продуктами реакции.
К сложным реакциям относятся:
k,
обратимые |
А |
k, |
В, |
(2.20) |
|
|
|
\ 8 3 |
параллельные
последовательные сопряженные
|
|
/"k в |
|
(2.2 1 ) |
|
|
А ' |
|
|
||
|
|
ko . .. с |
|
|
|
А |
|
в |
|
с , |
(2.22) |
|
|
|
|||
А + В D + Е, |
|
(2.23) |
|||
|
kl |
|
k2 |
|
|
А+ С F + G.
Ксложным часто относят и цепные реакции , представляющие
собой периодически повторяющуюся последовательность реакuий
(стадий), в которых образуются свободн ые атомы или (и) радика
лы. Сложные реакuии и их отдельные стадии могут быть разных
порядков. В основе кинетики сложных реакций лежит п р и н ц и п н с з а в и с и м о с т и р с а к ц и й , согласно которому "если в системе
протекает несколько реакuий, то каждая из них происходит неза висимо от других, так что общее изменение в с истеме равно сум ме этих нсзависимых изменений " . К каждой отдельной реакuии
применимы в таком случае основной постулат химической кинети ки и, соответствен но, уравнения простых (односторонних) реак ций.
Скорость последовательной реакuии определяется скоро стью наиболее медленной стадии , скорость же параллельных ре акuий определяется скоростью наиболее быстрой стадии.
Принцип независимости реакuий не является таким общим, как основной постулат химической кинетики. Он непримсним , например, к сопряженным реакuиям, в которых одни простые рсаю1ии существен но влияют (часто ускоряют) на протеканис друшх реакuий .
§ 4. ОБРАТИМЫЕ РЕАКЦИИ ПЕРВОГО ПОРЯДКА
Если в реакuии (2.20)
А -k:--В4
т2
в начальный момент времени концентрация молскул А равнялась
ел, а концентрация молекул В - с8, то, согласно основному по стулату химической кинетики, можно записать:
w = ·- |
d |
(сл |
сх ) k2 (св - сх )· |
c = k 1 |
|||
|
dt |
|
|
Прсобразуем правую часть этого уравнения , учитывая , что
(2 .24)
1 84

Тогда
(2.25)
Обратимые реакции Идут с отличной от нуля скоростью до тех
пор, пока скорости прямой и обратной |
реакций не сравняются , |
|||||||||
т.е. до достижения равновесия, когда |
|
) |
|
|||||||
d |
= (k |
+ k )( |
1 |
|
|
k |
2cB |
с |
равн=(). |
|
|
|
k |
сд - |
- |
|
|||||
cx |
1 |
|
|
|
|
|
||||
dt |
2 |
|
k1 |
+ k2 |
х |
(2.25а) |
||||
В этом случае (при t -+ оо) величина сх стремится к равновесному значению сх,оо' которое будет равно :
|
|
|
k1сд |
- k2c8 |
||||||||
сх,оо |
|
|
|
k |
1 |
+ |
|
|
||||
|
|
|
|
|
|
|
|
|
||||
|
значение |
|
х,оо |
|||||||||
Подставляя это |
|
= |
( |
|
1 |
|
|
с |
|
|
в уравнение (2.25), найдем : |
|
d;; |
|
+ k |
2 |
) |
(cx,uo - сх )· |
|||||||
|
|
= |
|
k |
|
|
|
|
||||
Проинтегрировав это уравнение, получим выражение |
||||||||||||
ln Сх'оо - Сх |
= -(k1 + k2)t, |
|||||||||||
|
|
сх,оо |
|
|
|
|
|
|
|
|
||
которое затем преобразуем в уравнение:
(2.25б)
(2.26)
(
k1
+
k2
)
=
1 - t
ln
Сх |
оо |
' |
|
сх,оо - сх
,
(2.27)
напоминающее по ВИдУ уравнение
первого порядка.
Потенцируя уравнение (2.27),
С учетом того, что cA,r = сА - сх и
текущие концентрации веществ А и
времени в вИде соотношений:
СА ,t |
- СА - Сх |
- СА |
- |
Сх |
|
|
|
|
(2.4) односторонних реакций
найдем:
(2.28)
св,r = св + сх, где cA,r и св,r -
В, получим их зависимость от
,оо |
[ |
1 |
- е |
-(kJ+k2)1 |
] |
' |
|
|
|
(2.29)
1 85

с |
с |
Рис.68. Зависимость сд - |
сх. сн + сх и сх от времени в обратимых рса](l(иях первого |
||||||||||||
|
|
а. |
|
|
|
сх.ао. |
б - при |
мn.;1ых cx.w |
|
|
|
||
|
|
порядка: а - при больших |
|
|
(ел - cJ , (св |
|
|
||||||
|
На рис.68, |
|
б |
изображены зависимости |
+ cJ |
и |
|||||||
|
|
|
|
|
|
|
|
|
|
||||
|
от времени для разных (больших и малых) значений |
|
зави |
||||||||||
сящих от |
соотношения констант скорости |
k1 |
и |
k2 в соответствии |
|||||||||
|
а, |
|
|
|
|
||||||||
с уравнением (2.25б). |
|
|
|
|
|
сх.оо' |
|
|
|||||
сх |
Из уравнения (2.24) при равновесии имеем: |
|
|
||||||||||
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
(2.30) |
|
откуда с учетом уравнения (2.27) |
получаем выражен ия для |
||||||||||||
расчета отдельных констант: |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
(2.3 1 ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
(2. 3 1 а) |
|
|
|
§ 5. МЕТОДЫ ИЗМЕРЕНИЯ СКОРОСГЕЙ РЕАКЦИ Й |
|
|
|
||||||||
|
Реакции в растворах легко наблюдать по изменению окрас |
||||||||||||
ки (колориметрия), по вращению плоскости поляризации (поля
риметрия ), по изменению электропроводности (кондуктомет
рия), коэффициентов поглощения света (спектрофотометрия) и |
|
друтих физических свойств растворов. |
· |
|
|
Скорость реакций , сопровождающихся изменением кон центраций кислот, щелочей, ионов галогенов и т.п., определяет
ся измерением рН среды или титрованием растворов.
Кинетика реакций в растворах, приводящих к образованию слабо растворимых газов (Н2, N2, 02 и др . ), а также газовых реак
ц ий с изменением числа молей. , изучается по изменению даi3Jiе
ния газов в замкнутой с исте м е
186
Радиоактивный распад элементов в минералах и солях опре деляется радиохимическими методами. Разновидностью этих методов является так называемый метод радиоактивных индика торов (или меченых атомов), когда предварительное введение в
исходную систему небольших количеств радиоактивного (или ред кого стабильного) изотопа реагирующего элемента позволяет на блюдать за изменением его концентрации без какого-либо вмеша
тельства извне. Этот метод является бесконтактным, как и боль шинство физических методов измерения скоростей реакций, так
как при этом не нарушается ход реакции при измерении ее скорости .
§ 6. МЕТОДЫ ОПРЕДЕЛЕНИЯ ПОРЯДКА РЕАКЦИЙ
Для определения порядка реакции применяются различные способы. Простейшим из них является метод подбора констант скорости, заключающийся в подстановке опытных данных в урав нения реакций первого или второго (реже третьего) порядка и установлении того порядка, уравнение которого соответствует постоянству значений констант скорости.
Метод подбора констант чаще используется в графическом варианте. С этой целью соответствующие кинетические уравнения (2.4) и (2 . 1 2) сначала линеаризуют, т.е. приводят к линейной зависимости концентрации (или искоторой функции от концен трации) о т времени. Так, например, для реакции первого порядка уравнение (2.4) преобразуют в форму:
(2.32)
а уравнение (2 . 1 2), используемое в кинетике реакций второго по рядка, записывают в виде :
.с!. = _с!0_ + k:J |
(2.33) |
Изображая графически эти зависимости от времени (рис .69, а, б), устанавливают, какому порядку лучше отвечают опытные данные.
Можно определять порядок реакций и по зависимости вре мени полупревращен ия одного из исходных веществ от его на чальной концентрации. Так, для реакций первого порядка из урав нения (2.9)
1 87

ln c
Рис.69.
ё,
t |
|
|
|
а |
t |
||
Зависимость от времени(lп с), I-п с и 1/с дпя( односторонних реакuий : а - первого
б второго 1/с) порядков
следует, что период полураспада не должен зависеть от начальных концентраций исходных веществ. Вместе с тем для реакций вто рого порядка из уравнения (2. 1 8) время полупревращения
1 'J/2 = -k l/Со
обратно пропорционально начальной концентрации исходных веществ.
Для реакций третьего порядка можно показать, что время полупревращения обратно пропорционально квадрату начальной
концентрации исходных веществ: |
|
||
r1/2 = |
2k ш3 |
с2о . |
(2.34) |
§ 7. БЫСГРЫЕ РЕАКЦИ И В РАСГВОРАХ, ЛИМИТИРУЕМЫЕ ДИФФУЗИЕЙ
Скорость быстрых реакций (с энергией активации, близкой нулю) определяется обычно скоростью диффузии. Согласно зако ну Фика число частиц, перссекающих поверхность S в 1 с, про
порционально площади поверхности и градиенту концентрации частиц в направлении потока:
dn |
DS |
d |
|
|
|
cr |
(2.35) |
||
где с - объемнаяdt -кон- |
|
dr |
||
|
|
|||
центрация' |
частиц. |
|||
При центрально-симметричной диффузии в стационарном
режиме концентрация частиц растворенного вещества с, на рас
стоянии r от поверхности равна:
(2.36)
188
Поскольку |
|
dc,= |
cr0 |
|
r ----.:;оо = |
О при |
r = |
r0• |
||
Очевидно, что |
с, |
с при |
|
и |
с, |
|
||||
|
|
dr |
r 2 |
' |
|
|
|
|
|
(2.37) |
|
|
|
|
|
|
|
|
|||
число частиц, |
перссекающих сферическую поверхность (S = 4 тег2) |
|||||||||
в 1 с в направлении увеличения |
r, |
определится уравнением: |
||||||||
|
|
dn |
-4nDcr0 . |
|
|
|
(2.38) |
|||
|
|
- = |
|
|
|
|||||
|
|
dt |
|
|
|
|
|
|
|
|
Число частиц, достигающих поверхности S за 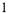 с, составляет:
с, составляет:
dn
- = 4nDcr0. (2.38а) dt
Число частиц типа А, которые в процессе диффузии дости гают за 1 с сферической поверхности с радиусом (гл + r8), равно:
(2.39)
Эту величину можно рассматривать как число столкновений всех молекул типа А с одной молекулой типа В. Полное число столк
новений за 1 с между всеми движущимися молекулами типа А и |
||
неподвижн |
вZл = 4тсDл(rл +rв)сл с8. |
(2.40) |
|
ыми молекулами типа В определится соотношением: |
|
Для обратного случая имеем: |
|
|
|
|
(2 .40а) |
Поскольку оба процесса не зависят друт от друга, полное |
||
число столкновений будет равно : |
|
|
|
|
(2.4 1 ) |
Это уравнение является одной из ф о р м |
у р а в н с н и я |
|
С м о л у х о в с к о г о и представляет собой выражение для скоро
сти реакций нейтральных частиц , лимитируемой диффузией . Множитель, стоящий перед произведением концентраций частиц
А и В, является константой скорости :
(2.42)
Для перевода размерности константы в обычные (для химиков)
единицы измерения умножим правую часть уравнения (2.42) на
NA и разделим на 1 000:
1 89

где NА - |
kп |
|
41nN |
|
(Dл + Dв)(rл + rв ) |
|
л/моль·с , |
(2. |
4 |
3) |
||||
|
|
|
000 |
|
|
|||||||||
постоянная |
Авоr.щро, равная 6,02 |
· |
10 |
2 |
3 |
молекул/моль. |
|
|
||||||
|
= |
|
|
А |
|
|
|
|
|
|
|
|
|
|
Если реагирующие частиuы - ионы, надо учитывать влия-
ние электростатических сил на скорость реакции. В этом случае по
Дебаю имеем: |
= --А |
|
+ |
|
+ |
r8) |
-6-6 . |
|
|
|
|
|
|
||||||
kп |
N |
(Dл |
|
Dв)(rл |
|
|
|
(2.44) |
|
4тr. |
|
|
е |
1 |
|||||
|
1 000 |
|
|
|
|
|
|
||
|
t5 = |
ZлZвС2 |
Здесь |
ekTа |
(2.44а)
Zл и Zв - заряды ионов- А и В; t: - диэлектрическая прониuае
мость( раствора) ; cr расстояние максимального сближения ионов rл +r8 , необходимое для того, чтобы произошла реакция.
С учетом формулы Стокеа - Эйнштейна
|
D = |
kT |
|
|
(2.45) |
|
в которой 11 -k |
бтr.Т]Г ' |
|
+ rв)2 |
|
||
|
2N Ak T (rл |
|
||||
|
вязкость среды, |
получим из уравнения (2.43): |
||||
|
|
|
--'-'-- |
Гд ГВ |
|
|
|
rA D |
= |
300011 |
-'--'-----' '=-- |
(2.46) |
|
|
|
|
|
|||
|
= |
|
|
|
|
|
При условии |
r8 |
имеем для нейтральных частиu |
|
|||
|
|
|||||
- SRT kD ЗООО11
или для ионов
(л/моль·с)
(2.47)
kп |
= |
SRT |
(ев |
8 |
|
|
ЗООО11 |
- 1} (л/моль·с). |
(2 .48) |
ГЛАВА 3. КИНЕТИ КА ГЕТЕРОГЕННЫХ РЕАКЦИЙ
§ 1. СКОРОСТЬ ДИФФУЗИИ
Во всякой гетерогенной реакции взаимодействие реагентов происходит на поверхности раздела фаз . Взаимодействие приво
дит к различию конuентраuий веществ в поверхностном слое и объеме и сопровождается двумя проuессами: подводом реагирую
щих веществ к зоне реакции и отводом из нее продуктов реакции.
1 90

Суммарная скорость гетерогенной реакции определястсн скоростью наиболее медленного процесса, которым, например,
при растворении солей в воде или в водных растворах кислот яв
ляется диффузия.
Большое значение в гетерогенных реакциях имеет состоя ние и величина поверхности соприкосновения фаз, на которой происходит взаимодействие.
С к о р о с т ь д и ф ф уз и и газа или растворенного вещества
измеряется обычно числом молей (или граммов) вещества, про
ходящего через площадь S в единицу времени. Согласно первому
закону Фика скорость диффузии равна:
dn -DS dc
dt = d.x ,
где D - коэффициент диффузии, измеряемый в см2/с в газах и в см2/сут в растворах; dcjdx - градиент концентрации вещества на отрезке пути dx. Знак минус указывает на то, что концентрация в направлении диффузии вещества убывает.
Если градиент концентрации на всем пути не меняется со временем, имеют дело со стационарной диффузией. В этом случае
производная (-dcjdx) может быть заменена отношением (с0 - с)/
емной фазе и у поверхности или наоборот, когда |
с |
процесс растворения твердого тела). |
|
Скорость диффузии может быть выражена соотношением: |
|
w = DS (с0 - с), |
(3.2) |
8 (с0 > с), где 8 - толщина диффузионного слоя, а с0 и -
концентрация вещества на границах этого слоя (например, в объ рассматривается
из которого видно, что она прямо пропорциональна поверхности раздел;1 фаз и разности концентраций в диффузионном слое и обратно пропорциональна толщине этого слоя.
§ 2. СКОРОСТЬ РАСТВОРЕНИЯ ТВЕ РДЫХ ТЕЛ
Скорость растворения твердых тел определяется скоростью
диффузии растворяемого вещества из поверхностного слоя в жид |
|||||||||
кую фазу. Эта w = k(c |
) |
|
|
|
|
(3.3) |
|||
|
|
|
скорость может быть представлена уравнением: |
||||||
Здесь |
|
|
нас |
|
|
|
|
|
|
|
|
- концентрация |
растворяемого вещества в слое, при |
||||||
|
|
|
твердого телu, |
приближающаяся к кон |
|||||
лег-ающем к поверхности- с |
|
. |
|||||||
центрации насыщенного раствора этого вещества; |
|
- концен |
|||||||
|
сн"с |
|
|
|
|
|
|
||
трuция |
растворенного всществu в остальном слое |
жидкости. |
|||||||
|
|
|
с |
|
|||||
1 9 1

Через k обозначают коэффициент растворения, величина которого зависит от коэффициента диффузии данного вещества в
данном растворителе, толщины и площади сечения диффузион
наго слоя, поскольку в соответствии с уравнениями (3.2) и (3.3)
W = J (С - С} |
С |
- С). |
|
|
DS |
нас |
= k( нас |
|
(3.4) |
|
|
|||
Это уравнение было впервые получено А.Н.Щукаревым
( 1 894) и может быть применено с теми или иными модификация
ми и для процессов кристаллизации солей из пересыщенных рас
творов и для процессов испарения жидкостей в воздух в замкну
том сосуде и т.д.
Пример 3.1. Определить скорость растворения куска мрамора в 1 ,0 н. растворе соляной кислоты:
если концентрация кислоты через 1 ч уменьшится в 4 раза. Решение. Если кислота поступает к твердому телу за счет
диффузии, то ее концентрация вблизи твердой поверхности из-за быстрой реакции практически падает до нуля. В этом случае ско рость растворения определяется по изменению концентрации ки слоты в объеме:
|
с |
|
с0 - сх |
w = kc, |
(3.4а) |
||
где |
= |
- |
концентрация кислоты в объеме в данный мо |
||||
|
|
||||||
мент времени. |
|
|
|||||
Уравнения (3.3) и (3.4а) показывают, что растворение твер дых веществ идет как односторонняя реакция первого порядка. В
этом случае константу скорости определим из уравнения (2.4):
|
|
|
k |
|
! ln |
|
-1- In |
1'00 |
= 2 |
' |
3 - 10-2 |
мин-t, |
|
|
а |
|
|
|
|
t |
|
|
60 |
0,25 |
|
|
|
|
|
скорость |
реакции - из уравнения (3.4): |
|
|
|||||||||||
|
|
= |
|
с |
= |
|
|
|
|
|
|
|
||
|
|
= kc = k(cо - |
х) = 2 ' 3· 10·2·0' 2 5=5' 75· |
1 0·3 гэквjмин. |
||||||||||
|
Для растворов по величинам |
D ( 1 см2/сут) и S |
можно |
|||||||||||
|
w |
|
|
|
|
с |
|
|
|
|
||||
определить толщину диффузионного слоя 8, |
которая часто ока |
|||||||||||||
зывается равной 0,02 - 0,05 мм. Перемешивание и нагрев раствора
ускоряют диффузию, поэтому опыты по измерению скоростей ге
терогенных процессов проводят обычно при постоянных темпе ратуре и скорости перемешивания.
1 92
§ 3. ДИФФУЗИОННАЯ И КИН ЕТИЧЕСКАЯ ОБЛАСТИ ГЕТЕРОГЕННОГО ПРОЦЕССА
В некоторых гетерогенных процессах могут наблюдаться соизмеримые скорости диффузии и протекания самой реакции на
поверхности раздела фаз, равной по определению
w5 = kSc. , |
(3.5) |
где n указывает на порядок реакции. |
|
Для реакции первого порядка имеем: |
|
w5 = kSc5 , |
(3.6) |
где с5 - концентрация реагента в поверхностном слое.
При протекании химического процесса происходит умень шение исходных веществ и образование продуктов реакции на поверхности раздела фаз. Пополнение первых и удаление вторых происходит за счет переноса веществ из объема газовой фазы (раствора) к (или от) поверхности раздела. Механизм этого пере носа обычно диффузионный, так как в отсутствие принудитель ных потоков он обусловлен наличием градиента концентраций
реагентов между объемом и поверхностью раздела. При устано вившейся диффузии ее скорость будет равна:
wD |
|
DS |
|
|
(3.7) |
= - (со - cs )· |
|
||||
|
|
8 |
|
|
|
В стационарном состоянии, когда w5 = w0, получим: |
|
||||
kSc5 |
DS |
(с0 - cs ) |
|
|
|
= --в |
, |
(3.8) |
|||
откуда
(3.8а)
Соответственно, скорость реакции в случае соизмеримых скоро стей w5 и w0 будет равна:
kS
Ws = со.
1 + -
D
(3.9)
Из этого уравнения вытекают два предельных случая. В пер вом случае, когда скорость диффузии меньше скорости поверхно
стной реакции, т.е. если k8jD >> 1 , то скорость всего гетероген ного процесса будет определяться скоростью переноса:
(3. 1 О)
1 93

/n k
Рис.70. З |
а |
висимость |
ln |
k от |
! / Т в |
|
|
ки нетической (ks) и диффузионной
(kп) областях
о
В друго:-.1 крайнем случж, когда скорость диффузии больше
скорости поверхностной реакции, т.е. если kO/D < < 1 , скорость всего гетерогенного процесса определится скоростью поверхно
стной реакции:
w5 = (3. 1 1)
Первую предельную область, в которой можно пренебречь скоростью поверхностной реакции, называют диффузионной (или, точнее, внешнедиффузионной), а вторую - кинетической областью.
Повышение температуры в диффузионной области слабо влияет на скорость всего гетерогенного процесса, поскольку ко эффициент диффузии слабо ( D 7112)зависит от температуры. В
кинетической области повышение температуры приводит к зна чительному увеличению скорости всего процесса в соответствии
с уравнением Аррениуса ( 1 . 1 9):
е-EA IRT .
На рис. 70 изображены схематичесю1 зависимости ln kD и ln k5
от 1 / Т в диффузионной и кинетической областях гетерогенного
процесса.
Из рисунка видно, что при повышении температуры, когда скорость поверхностной реакции становится высокой, опреде ляющими скорость всего гетерогенного процесса являются про
цессы переноса.
§ 4. РОЛЬ АДСОР БЦИИ В ПОВЕРХНОСТНОЙ Р ЕАКЦИИ
Иногда гетерогенная реакция кроме процессов персноса (диффузии и т.п.) включает в себя еще и адсорбцию в качестве одной из стадий сложного механизма гетерогенной реакции:
а..1с |
+ |
S |
--аде+ |
Амс ' |
Аrаз |
|
|
||
А |
--+ |
В |
(3 . 1 2 ) |
|
|
|
|||
1 94

В этом случае скорость реакции пропорциональна концентрации адсорбирован н о го вещества на поверхности .
Если отнести скорость поверхностной реакции к единице
поверхности, то выражение с корости такой реакции (по анало ги и со скоростью реакции в единице объема) будет иметь вид :
|
|
= |
_!_ dna |
= dc% = |
|
1cs |
|
||
|
|
|
|
|
|
|
|
||
|
Ws |
|
S dt |
dt |
k |
а ' |
(3. 13) |
||
где |
- концентрация адсорбированного вещества А н а по верх |
||||||||
ностиc-S. . |
П о с кольку эта концентрация пропорциональна доле заня |
||||||||
той п оверхности , при малой адсорбции продуктов реакции В мож но записать:
(3. 14)
где е - доля поверхности, занятой адсорбатом ; k5 - коэффици ент пропорциональности, равный скорости реакции при е = 1 .
Согласно основному постулату химической кинетики для скорости адсорбции вещества А запишем:
аде |
аде |
А |
w |
= k |
р (1 |
-
е)
'
(3 . 15)
где Рл - парциальное давление вещества А в газовой фазе; (1 - е) - доля свободной п оверхности. П р и адсорбции вещества из рас
твора вместо Рл надо взять сА (молярн ость вещества А). Для процесса десорбции имеем :
|
|
wДСС = kДСС е . |
(3. 16) |
н у 8 |
Если адсорбционные процессы происходят быстр о , величи |
||
МОЖНО ВЫЧИСЛИТЬ И З усЛОВИЯ адсорбЦИОННОГО раВНОВеСИЯ : |
|||
откуда |
kадерА( 1 - е) = kдес е ' |
|
|
е = kадсРл kде с + kадсРА
Ьл Рл 1 + Ьл Рл
(3. 1 7)
Здесь Ьл - так называемый а д с о р б ц и о н н ы й к о э ф ф и ц и е н т
в е щ е с т в а А.
И з уравнений (3. 14) и (3. 17) находим , что с корость поверхноетной реакции равна:
W |
s - |
|
П р и ЬtPА << 1
k |
Ьл Рл |
s 1 + Ьл Рл
это уравн ение приобретает вид :
(3. 1 8)
1 |
3 |
* |
1 95 |
|
|
|
|
|
|
повсрхносnюй |
реакнии (3.Рл |
|
||
|
|
|
|
12) |
|
||
|
|
|
Р и с . 7 1 . Зависи ость w5 от |
|
|
для |
|
|
|
|
H's = k)J.pA ' |
(3 . 1 8а) |
|||
т.е . является юшетичесю·!.\1 уравнением реаЮJ.ИИ первого порядка. |
|||||||
При |
Ь,..рл>> |
1 |
|
|
|
|
|
|
|
|
|
(3 . |
1 8б) |
||
т.е. является кинетическим уравнением реаЮJ.ИИ нулевого поряд ка |
|||||||
( А |
= |
1 ) . |
|
|
|
|
|
С (О) |
|
|
|
|
|
|
|
|
В области промежуточных значений давлений, когда Ь |
|
л |
||||
имеет место |
уравнение (3 . 1 8) , которое является |
кинетическимлР 1 , |
|||||
уравнением дробного порядка типа:
(3 . 1 9)
где т > 1 .
На рис. 7 1 изображена зависимость скорости поверхностной
реакции (3. 12) от давлен ия адсорбата А в объеме над поверхно стью.
§5. ПРЕДСТАВЛЕ Н И Е О КИНЕТИКЕ КР ИСТАЛЛИЗАЦИ И
Кр и с т а л л и з й ц и е й называют обычно процесс образова ния и роста криста}'JЛОВ из газовой фазы. раствора или расплава.
Она происходит благодаря пересыщению или переохлаждению
исходного газа, раствора или расплава по отношению к возни
кающим в них кристаллам .
Возникновение зародышей -- центров кристаллизации - и
рост их требуют преодолен ия о пределенного потенциального
барьера и не могут быть объяснены с по:vющью только соотноше ни й термодинамики.
Н еобходимое для этой цели рассмотрение процесса с точю1
зрения кинетики исходит из следующих предпосылок. Во-первых ,
число возникающих в единицу времени в единице объема цен
тров кристаллизации пропорц1юн 1ьно произведению вероятно
сти образования трехмерных кристаллических зародышей, равной
по Фальмеру
1 96

"(3} |
о А(З) схр[- |
Т |
( ; |
'J |
|
|
) |
|
(3 .20)
на вероятность роста на их гранях двумерных зародышей, равную
(3 .2 1 )
Здесь А(31, A<lJ' В и В' - постоянные; д Т - переохлаждение; CJ -
поверхностное натяжение на границе жидкость (или газ) - трех |
||||||||
мерный зародыш; CJ1 |
- межфазное поверхностное натяжение на |
|||||||
границе трехмерный - двумерный зародыши. |
|
|
|
|||||
Таким образом, скорость кристаллизации |
2 |
|
||||||
dn |
|
|
з |
|
|
|
|
|
|
В |
|
|
] exp[- |
-B'(---cr---')-] |
|
||
_ = w(3) w(2) = А ехр(- |
|
2 |
|
|||||
сr |
|
|
|
|
(3 .22) |
|||
dt |
|
Т(дТ) |
|
|
Тд Т |
|||
|
|
|
|
|
||||
будет тем меньше, чем больше при данном переохлаждении д Т |
||||||||
будут величины поверхностных натяжений |
|
и |
. В уравнении |
|||||
(3 .22) А = А(3Л2)" |
|
|
|
|
|
|
|
|
В связи с вышесказанным металлы, обладающие более низ |
||||||||
|
|
|
|
|
cr cr' |
|
|
|
кими значениями CJ |
и CJ' , будут кристаллизоваться при малых |
|||||||
переохлаждениях, в то' время как соли, силикаты и т.п. с высоки ми значениями CJ и CJ допускают большие переохлаждения и могут иногда не закристаллизовьшаться, образуя аморфные стеклооб разные твердые тела.
Во-вторых, линейная скорость роста различных граней кри сталлов, являющаяся также функцией переохлаждения, пропор цианальна поверхностной энергии этих граней. Исходя из этого положения медленнее всего растут грани с наименьшей величи ной cr, благодаря чему равновесная форма кристаллов содержит
преимушественно такие грани.
Большое значение в процессе кристаллизации имеют раз
ного рода дислокации (дефекты структуры), выходящие на по
верхность растушего кристалла.
§ б. КИНЕТИКА ТОПОХИ МИЧЕСКИХ РЕАКЦИ Й
Т о п о х и м и ч с к и м и р е а к ц и я и называют гетеро генные реакции, происходяшие на границе раздела твердое ис
твердый продукт реакции |
. К |
ним относятся |
|
ходное вещество - с |
1 |
|
|
реакции дегидратации (выветривания) |
типа |
|
|
! 97
реакции разложения типа СаСО3 СаО + С02 и многие другие.
Топахимическая реакция начинается обычно с образования
зародышей (ядер) кристаллизации твердого продукта на поверх
талл
ности крис исходного вещества. Центры этих ядер часто свя
заны с наличием на поверхности различного типа дефектов: дис
локаций, вакансий (дырок) или ионов в междоузлиях.
Около центров ядер начинается рост самих ядер, обычно сферического типа. По мере их роста увеличивается поверхность, т.е. поверхность раздела фаз, и реакция
Центры ядер |
ускоряется. Когда ядра сливаются и |
образуют общий реакционный фронт, |
|
лристаллизации |
|
поверхность раздела фаз и скорость становятся максимальными (рис.72).
Затем наступает замедление
вследствие перекрывания ядер. Из это го механизма топахимической реакции ясно, что скорость ее определяется как
скоростью образования ядер, так и скоростью их роста.
Поскольку реакция идет на поверхности раздела фаз, теряет смысл понятие концентрации и скорость представляют как изме нение степени превращения исходного вещества в единицу вре
мени:
W = da..
-
dt '
где сх = (g0 - g)/ g0 , а g0 и g -
вещества.
Как и скорость любого химического процесса, скорость то
похимической реакции зависит от температуры и давления и при |
|||||
постоянных |
Р |
и |
Т является искоторой функцией а..,которую и |
||
|
|
w |
необходимо определить из экс- |
||
|
|
|
|
периментальных данных. |
|
|
|
|
|
|
Опыты показывают, что |
|
|
|
|
|
кривая зависимости а..от t имеет |
|
|
|
|
|
вид сигмаобразной кривой, а |
|
|
|
|
|
скорость реакции проходит через |
|
|
|
|
|
максимум (рис. 73). Такой вид ки |
|
|
|
|
|
нетических кривых можно объяс |
|
|
|
|
|
нить следующим образом. В на |
Р ис 7 3 . О бщ и й |
|
в ил |
к и нетических |
чальный момент времени ско |
|
|
рость появления ядер и их роста |
||||
кривых топохи.\!ических рсакuи й |
|
||||
О |
|
tm |
t |
|
|
мала, затем их поверхность начинает быстро расти, так что ко времени tm скорость становится максимальной wm, а степень пре вращения (в большинстве известных реакций) достигает значе-
ния а . 0,5. После этого, из-за отсутствия свободной поверхности, новых ядер не образуется, а перекрывание ядер приводит к уменьшению по верхности раздела фаз (рис.74).
Граница раздела фаз продвигается в объем твердой фазы , и скорость реакции уменьшается.
При кинетических расчетах топахимических реакций часто
используют два подхода к скорости образования ядер. Согласно первому из них ядра образуются по экспоненциальному закону:
|
N0 и N(t) - число |
|
- |
e·kt |
|
( t = О) |
|
|
(t) |
||
|
N(t) |
= |
N0( |
1 |
|
) , |
|
|
(3.24) |
||
|
|
|
|
|
|
||||||
где |
|
|
|
ядер в начальный |
|
и данный |
|
||||
моменты времени. |
|
|
|
|
|
|
|
|
|
|
|
|
Второй подход основан на степенном законе образования |
||||||||||
ядер: |
|
|
" , |
|
|
|
|
|
|
|
|
|
N(t) = К" t |
|
|
|
|
|
(3.25) |
||||
где К" - некоторый коэффициент пропорциональности. |
а. от t , |
||||||||||
|
Первый подход приводит к сложной зависимости |
||||||||||
которая редко используется на практике. Второй подход был обос нован Х.С.Багдасарьяном (1945) с помощью модели многоста дийного образования ядер с возрастающей скоростью.
Чтобы вывести теперь зависимость а. = f(t), воспользуемся м етод о м К ол м о го р о в а - Е р о ф е е в а . Если учесть, что число ядер постоянно растет, то объем их в начальной стадии реакции и, соответственно, доля прореагировавшего вещества бу дуг равны:
(3.26)
где К - постоянная скорость роста (см/с), а К t - радиус ядра. gСкорость реакции из уравнения (3.23) будет пропорцио
нальна общей площади поверхности ядер:
|
w |
= |
---;}i |
2 = Kg [4л.N0 Kg2t 2 ). |
(3.27) |
||
|
da |
= |
4л.N0Kgt |
||||
фаз |
|
|
|
|
|
||
Однако из-за их перекрыванияз эффективная поверхность раздела |
|||||||
|
будет составлять долю ( 1 - |
а.) от общей поверхности. |
|
||||
1 99

Вследствие этого скорость реакции с учетом перекрывания ядер будет равна:
w = - = |
4тr.N0Kgt2(1 - а), |
(3.27а) |
|
da |
|||
dt |
|
|
|
откуда после интегрирования получимз |
: |
|
|
|
= l - e-kt1 |
(3 .28) |
|
Если считать скорость образования ядер постоянной, мож |
|||
но прийти к уравнению: |
|
|
|
a = 1 - e k14 . |
|
(3.29) |
|
Испо.'I ьзуя закон образования ядер с возрастающей скоро стью, полученный Х .С. Багдасарьяном, Б . В. Ерофеев получил
уравнение общего вида: |
= cr 3. |
|
|
а |
1 - e-kt" , |
(3.30) |
|
В этом уравнении |
представляет собой число элементарных ста |
||
дий превращения центра кристаллизации в растущее ядро. В более |
||||
общем случае |
n |
= cr |
n |
+ |
|
= cr + а , |
|
(3.3 1 ) |
|
где а указывает число направлений, в которых растут ядра (а = 1 ,
2 или 3). |
|
|
|
|
|
|
|
|
Константа скорости k и величина |
легко определяются гра |
|||||
фически после линеаризации уравненияn |
(3.30): |
|
|||||
|
|
1n [-1n (1 |
- а)] = |
1n k + |
n |
l n t |
(3 .32) |
|
изображения зависимости двойного логарифма от ( 1 |
а)· 1 - |
|||||
логарифма времени. |
|
|
|
|
|
||
н |
На рис. |
75 представлена такого рода зависимость для реак |
|||||
ции разложения перманганата калия: |
|
|
|
||||
ln[-ln(l-a.)) |
|
|
|
|
|
|
|
|
0 , 0 |
|
|
|
|
|
|
|
- Z,3 |
|
|
Рис.75 . |
Зависимость двойного логарифма |
||
|
|
|
|
ln[-lп( l |
- а)] от логарифма времени (ln 1) |
||
|
0 |
Ц ,О |
ln t |
для реакuи и разложения п ерм а н ганата |
|||
|
|
|
калия при 2 1 s·c |
|
|||
|
-Ц,б .__.......,'---------'---- |
|
|||||
200

2KMn04 Мп, 04 + Mn02 + 02,
изученная Б.В.Ерофеевым с сотрудниками. Как видно из рисун ка, опытные данные хорошо ложатся на прямую, однако в конце
опыта наблюдается увеличение двойного логарифма, что связано, |
||||||
по-видимому, с увеличением показателя |
n степени при |
томn, |
что |
|||
Вычисленные из графика значения I п |
k |
""' |
- 1 9,0 |
|||
говорят об образовании ядер в одну стадию |
|
= |
1 ) и о |
/. |
|
|
рост межфазовых поверхностей раздела идет(ав одном направле |
||||||
нии (а = 1 ) . |
|
|
|
|
|
|
Как показьшают опыты, величина |
растет по мере старения |
|||||
их перскристаллизацисй. |
||||||
кристалличссю1х веществ или в связи с n |
|
|
|
|
|
|
ГЛАВА 4. КИНЕТИКА РЕАКЦИЙ В ПОТОКЕ. |
|
|
||||
ПРЕДСТАВЛЕНИ Е О КАТАЛИЗЕ |
|
|
|
|||
§ l. ОБЩИЕ ПОНЯТИЯ
Большинство химических процессов в природе и технике осушествляется обычно в потоке. Реакции в потоке различаются по режимам их проведсния. Так. если в потоке отсутствует про дольное и поперечное перемешиванис, то имеет место п р ед е л ь н ы й р е ж и м и д е ал ь н о го в ы т е с н с н и я . Если же в резуль
тате персмешивания концентрации всех реагирующих веществ в любом сечении реактора равны их концентрациям на выходе, на
блюдается п р |
|
д с л ь н ы й р е ж и м и д е ал ь н о г о п е р е м е ш и - |
|
в а н и я . |
что в реальных условиях трудно осушествить любой |
||
Ясно, |
|
с |
|
предельный режим и процессы идут по каким-то смешанным ре жимам. Однако независимо от режима протекания реакции в по токе сопровождаются изменением объема реагирующих веществ. Поэтому кинетические уравнения таких рсакций1 отличаются от
уравнений кинетики реакций в замкнутых системах, рассмотрен НЬIХ выше.
Ниже будут рассмотрены в качестве примера односторон ние реакции в режиме идеального вытеснения. Это в первую оче редь обусловлено тем, что многие процессы в потоке, особенно в природных условиях, осушествляются в режимах, близких к этому. Интересуюшихся более сложными реакциями в этом режиме, а также реакциями в режиме идеа.пьного персмешивания отсылаем к рекомендуемой нами дополнительной литературе.
1 Существенный вк-1ад в раз в итие теор ии юшстики рейкций в п отоке внес
1 1 рофессор МГУ Г . М .П йнчснков .
20 1

§ 2. ОБЩИЕ УРАВНЕН ИЯ ДИНАМИ КИ И КИН ЕТИ КИ РЕАКЦИ Й В
РЕЖИМЕ ИДЕАЛЬН ОГО ВЫТЕСНЕН ИЯ
При описани и химических реакций в режиме идеального вытеснения надо учитывать наряду со скоростью самой реакции
еше и персмешение вешества вдоль реактора. В связи с этим урав
нения , опис ывающие процсссы в потоке , содержат по меньшей |
||
:v1epc, |
|
|
дв:.t пара:v1етр:1: вре:v1я и координ пу для одн омерного потока. |
||
Т:.tкис уравнен ия н азыв:.tютоi |
уравнен иями химической дин:.tми |
|
ки или ур:.tвнсниями дина шю1 хи:vшческих реакци й . |
||
Рзссмотрим поток реагирующих вешеств, проходящих через |
||
сечения /1 и 1,, н : .ходяt |
шисся на расстоянии 111 (рис .76). |
|
Рис.7Ь. I l ото=g=к |
||
---- |
- |
|
|
l1 |
..1l |
|
12 |
|
|
вещества в режиме идеального вьггеснения |
|
В потоке про исходит рсзкция типз рззложения н е которого |
||
вешества А: |
|
|
|
|
(4. 1) |
со скоростью |
|
|
w = -v1 -dnл- . |
(4.2) |
|
dt
Зададим постоян н ыми температуру рсзктор:.t и площадь его поперечного сече н и я . Для упрощения расчетов пренебрежем пе реносом всшеств зз счет диффузии .
Пусть линей н ая скорость потока в искотором сечении будет равн:.t u (см/с ) , :1 кон центрация вещества А в этом сечен и и - ел
(мольjсм3). О б ш и м у р а в н е н и е м д и н а м и к и х и м и ч е с к о й р с а к ц и и (4. 1 ) в этом случ:.tе будет уравнение материаль ного б:.t
ланса вида:
(4.3)
Левзя чзсть урзвнения обозначает количество вещества А,
проходящего через сече ния /1 и 1, за время М. Первые два слагае
\1ЫХ справа показьшают количество ве шествз А, прореагировав шего ко времени t1 и t, в объем е r/1,./, два других слагаем ых соот-
202

ветствуют количеству12• вещества А, непрореагировавшсму в объеме pbl ко времени !1 и
Разделив обе части уравнения (4. 3) на pblM, найдем:
ueл lzi - ueл lz2 |
- nл lr2 - nл lrt |
ы |
м |
v |
Переходя к пределам при 111 О и 11t
д(иел ) |
|
1 дпл |
дел |
|
|
- |
-- + - - , |
||
- --- = |
v |
|||
д! |
|
дt |
дt |
|
eл lr2 - eл lri
+ м
О, получим:
(4.4)
(4.5)
или
д |
) |
(ие |
|
л |
|
- --- |
|
д! |
|
=W +
дел - - дt
.
(4.6)
Последнее уравнение и есть уравнение динамики химической ре акции в режиме идеального вытеснения. В более общем случае нелинейной задачи получаем более общий вид уравнения:
( |
л |
|
) |
= w + |
д;;, |
- div c |
|
u |
|
|
(4.7)
которое в физике и механике называют у р а в н е н и е м |
н е п р е |
р ы в н о с т и (см. для сравнения уравнение (6.96), разд. |
I). |
Если в реактор в единицу времени подается одно и то же |
|
количество реагента А, то к моменту времени, когда этот реагент достигнет конца реактора, в системе установится стационарное состояние. В этом случае концентрация А со временем не будет изменяться, так что в любом сечении l
дел = О. дt
В связи с этим для стационарного состояния уравнение примет вид:
-д(иел ) |
|
w. |
--д' !--'- |
= |
|
-- |
|
(4.8)
(4.6)
(4.9)
Концентрация вещества и скорость потока определяются только расстоянием некоторого сечения от начала реакционной зоны:
ел = / (/ ) , и = < р /( ) . |
(4. 10) |
Представим теперь концентрацию вещества А:
(4. 1 1 )
203

аего линейную скорость:
и= vjp.
(4. 12)
В этих формулах пА - число молей вещества А, проходящего через
данное сечение |
в единицу времени; |
v - объем вещества, |
проходящий через1 |
это сечение в единицу времени. |
|
Подставив выражения (4. 1 1) и (4. 12) |
в уравнение (4.9), по |
|
лучим: |
|
|
-
-1 dnл р -- dl
= W.
(4. 13)
Если в начало реактора в единицу времени поступает n0A молей вещества А, то на расстоянии 1 от начала реактора прореа гирует доля
|
х |
= nол - nд |
, |
(4. 14) |
|||||
|
|
|
nол |
|
|
|
|
||
называемая степенью превращения вещества А. Поскольку |
|||||||||
|
nд = |
п0л |
( |
1 |
- |
х), |
(4. 15) |
||
|
|
|
|
|
|
||||
из уравнения (4. 13) |
находим: |
|
|||||||
|
|
dx |
|
|
|
|
|
|
|
|
nол - = |
|
|
|
|
(4. 16) |
|||
|
|
pdl |
|
|
|
|
|
||
Это |
|
|
|
|
|
|
к и н е т и к и |
||
уравнение |
является о б щ и м у р а в н е н и е м |
||||||||
|
|
|
|
w. |
|
|
|||
р е а к ц и и (4. 1 ) |
в р е ж и м е ид е ал ь н о го в ыте с н е н и я . |
||||||||
|
В соответствии с основным постулатом химической кинети |
||||||||
ки для односторонней реакции (4. 1) имеем: |
|
||||||||
|
floд - |
|
|
|
|
Сд . |
(4. 17) |
||
|
|
dx = k |
1 |
||||||
|
|
pdl |
|
|
|
|
|
||
Для интегрирования этого уравнения надо выразить сА = f (l ).
Задача упростится, если реагирующий газ считать идеа.Jтьным. То
гда общий объем смеси равен:
V = |
I.nR T , |
|
|
(4. 1 8) |
||
|
|
р |
|
|
|
|
а концентрация вещества А - |
|
|
||||
|
= |
п0л |
|
х р |
'- |
(4. 19) |
сА |
|
-(1'-------) |
||||
|
--2:.n-R-T - |
· |
|
|||
В этих уравнениях In |
- |
общее число молей всех реагирующих |
||||
веществ, проходящих через заданнос сечение в единицу времени.
204

При t = О концентрация продуктов реакции равна нулю и |
|
'Ln определяется соотношением: |
(4020) |
'Ln = n0л(l + х)о |
|
Здесь - изменение числа молей газообразных компонентов |
|
смеси в ходе реакции в расчете на 1 |
моль вещества А: |
fn-'
. - |
' |
- v |
|
l
+
v |
2 |
' |
|
+
0 0 0
-
1
о
(402 1 )
Давление в общем случае зависит от расстояния |
1 |
до начала реак |
ционной зоны: |
(4022) |
|
p =f(l )o |
|
Однако= часто перепад давления невелик, так что принимают р = consto
§ Зо КИН ЕТИЧЕСКОЕ УРАВНЕНИЕ РЕАКЦ И И РАЗЛОЖЕНИЯ ВЕЩЕСТВ В |
|||||||
|
РЕЖИМЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ |
|
|||||
В простейшей реакции (40 1 ) |
типа разложения веществ из |
||||||
уравнений |
(40 1 7) |
и (40 1 9) |
имеем: |
|
|
|
|
|
n |
|
dx |
1 n0л (1 - х) р |
' |
(4023) |
|
|
|
ол pdl - k |
InRT |
|
|||
или
dx |
1 |
(1 |
nол pdl = k |
|
1 |
Разделяя переменные,
-х) р
+х RT
находим
о
(4024)
1 + х |
dx |
= |
|
еР |
dl, |
|
|
|
|
|
||
(1 - х) |
|
|
|
Р |
|
|
|
|
|
|
|
|
|
|
n0лRT |
|
|
|
|
|
|
|
|||
или |
|
|
|
|
|
|
k |
1 |
p |
|
|
|
|
|
|
|
x |
|
|
|
|
||||
+ -- dx = |
|
p |
dl |
|
|
|||||||
n0л RT |
|
(4025) |
||||||||||
(1 - х) |
|
(1 - х) |
|
|
|
|||||||
Прибавляя и вычитая |
в числителе второго слагаемого в |
|||||||||||
левой части уравнения, найдем: |
|
|
|
|
|
|
|
|||||
--(1 dx |
- |
Р(- |
х |
+ 1 - |
1) |
dx - |
k |
1РР |
dl |
' |
||
|
- х) |
|
||||||||||
- х) |
|
|
(1 |
|
|
|
|
n0лRT |
|
|||
или |
|
|
|
|
|
|
|
|
|
|
|
|
205

(1 |
|
х) |
|
f3 |
x |
(1Bdx ) |
nод |
|
__!! |
|
|||||
откуда |
|
|
|
-!!!:d + |
|
= |
k |
1 |
р . |
RT |
dl, |
|
|||
- |
|
|
- |
х |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
dx |
|
|
|
|
|
р |
|
|
|
|
(1 + |
|
) |
-- - |
d |
= - - dl. |
|
(4.26) |
||||||||
|
|
|
(1 |
- |
х) |
x |
er |
· |
RT |
|
|||||
|
|
|
|
|
|
п0д |
|
|
|||||||
Проинтегрировав это выражение в |
пределах от О до /, полу |
||||||||||||||
чим уравнение: |
|
|
|
|
|
|
|
|
|
|
|
||||
-(1
+ ) ln(1 |
- х) - х = |
-klp nод
·
р - RT
1.
(4.27)
Из этого уравнения найдем аналитическое выражение для кон станты скорости реающи в потоке в режиме идеального вытесне
ния: |
|
|
е |
p V |
|
|
= nод RT [-(1 + ) ln(1 - х) - Вх], |
(4.28) |
где V = pl - объем реакционной зоны.
Для вычисления константы скорости перепишем уравнение
(4.28) в ином виде: |
|
|
|
|
|
|
|
1 |
+ в |
pv |
|
п0дх |
= -п0 |
|
|
-- |
(4.29) |
д -- 1n (l - х) - е . |
|||||
|
|
|
В |
BRT |
|
Если теперь ввести персменные
У = n0лх,
Х= - п0л ln( l-x),
то уравнению (4.29) будет соответствовать прямая линия (рис.77),
тангенс угла наклона которой равен:
1 |
+ |
|
(4.30) |
tga = -- . |
|||
|
в |
|
|
в
Рис. 7 7 . Зависимость |
от для |
одностор онних реакций |
перво го |
У Х
порядка в потоке в режиме идеальнот вьrгеснения
206

Отс юда легко определяется величина f:J . Отрезок, отсекае мый на оси ординат, равен :
|
|
|
|
|
|
|
|
|
|
(4.3 1 ) |
З н а я |
те м п ерату р у , |
давл е н и е , |
|
о бъ е м ре а кт о р а и вел ичи н у р , |
||||||
можн о в ы ч ислит ь |
из урав н е н и я (4. 3 1 ) и з н ач е н и е константы |
|||||||||
скорости реакции в режиме идеал ь н о го вытеснения . |
|
|||||||||
|
|
Если в реакции образуется л и ш ь один продукт: |
|
|||||||
|
|
|
|
А А' , |
|
|
|
(4 .32) |
||
то р = О и уравнение (4 .28) значительно упро щается до вид а : |
||||||||||
|
|
|
|
k 1 = nол p V |
n |
(l - x)), |
(4.33) |
|||
|
nол |
|
|
- |
R T [- 1 |
|
|
|||
где |
R T |
V |
объем газа , |
проходящий в единицу времени |
||||||
|
|
|
-- = |
|
|
|
|
|
|
|
|
|
|
р |
|
|
|
|
|
|
|
через сечение реактора. |
|
|
|
|
||||||
|
|
Поскольку |
|
Vjv = t, |
|
|
|
(4.34) |
||
|
|
|
|
|
|
|
|
|
||
приходим к простому виду уравнения д л я расчета константы с к о рости реакции в режиме идеального вытес н е н ия :
k 1 |
|
t In |
-1 - , |
(4. 35) |
|
1 - |
|||
совпадающему с |
уравнением односторонней реакции первого п о |
|||
= |
|
|
|
|
х
рядка в замкнутой системе (с м . уравнение т и п а 2.6). Это и понят но, поскольку реакция (4.32) в потоке происходит при сохране н и и реагирующей системой постоян ного объема.
§ 4. ПРЕдСТАВЛЕ Н ИЯ О КАТАЛИЗЕ
Катал и з о м называют явление изменения с корости реакции или возбужден и е реакции под действием веществ, которые к кон ц у реакции остаются химически неизмен н ы м и . Вещества, изме няющие с корость химических реакций (ускоряющие реакци и ) , называются катализаторами .
Примерами каталитических процессов являются: синтез ам миака на желез н ых катализаторах , контактный способ получения серной кислоты , ферментативные процессы в живых организмах и технике и мн огие другие процесс ы .
В е с каталитические процессы делятся н а гомоге н н ы е , (ка тализатор и реагенты находятся в одной фазе) и гетероге н н ые
( катализатор образует особую фазу) . Про межуточны 1 я вляется ка тализ с помошью то н коди с персных частиц кат<L'lизатора . Приме-
207
w",
|
|
Рис.78. Зависимость от времени скорости |
|
о |
автокаталитической реакции |
|
|
|
ро |
1 |
является ферментативный катализ, т.е. |
|
этого типа катализа t |
кuтализ химических и биохимических процессов под действием
ферментов (или энзимов).
Реuкции, в которых катализатором являются продукты ре акции, называются а в т о к ат ал и т и ч е с к и м и . Скорость таких реакций проходит через максимум, причем в начальный момент времени будет существовать некоторый период индукции J, тре
бующийся для накопления катализатора, когда скорость реакции
близка к нулю (рис. 78).
Эта кривая напоминает кинетическую кривую топахимиче ских реакций (рис.73), когда в начальный момент времени ско рость реакции также стремится к нулю.
К автокаталитическим реакциям относится, например, гид ролиз сложных эфиров в водных растворах, ускоряемый действи ем образующихся в процессе кислот:
RCOOR' + Нр ---RCOOH+ + R'OH .
