
Теоретический курс_ХБАС_ЛЕЧ
.pdf
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
1. образование хлорангидридов:
О-δ |
|
O |
R−С+δ |
+PCl5 → R−С |
+ POCl3 + HCl |
ОН |
|
Cl |
хлорангидрид 2. образование амидов. Поскольку аммиак не является достаточно сильным
нуклеофилом, амиды карбоновых кислот получают из их хлорангидридов, т.к. хлорболее легко уходящая группа, чем –ОН:
|
О-δ |
|
|
O |
|
R−С+δ |
+H−NH2 → R−С |
+ HCl |
|||
|
Cl |
|
|
NH2 |
|
|
|
|
|
амид |
|
|
|
|
|
||
|
|
|
|
|
|
3. реакция этерификации – это обратимый процесс образования сложных эфиров при взаимодействии карбоновых кислот со спиртами в присутствии минеральных кислот /HCl, H2SO4/:
|
О-δ |
|
|
H+ |
O |
R1−С+δ |
+H O−R2 ↔ R1−С |
+ H2O |
|||
|
ОН |
|
|
|
O−R2 |
|
|
|
|
сложный эфир |
|
|
|
|
|
||
|
|
|
|||
|
|
|
|
||
Сложные эфиры широко распространены в природе. Они придают аромат плодам, ягодам, цветам. Многие лекарственные средства содержат в своём составе сложноэфирные группировки.
4. образование ангидридов при взаимодействии двух карбоновых кислот в присутствии водоотнимающего агента /P2O5/:
R1−С+δ |
О-δ |
O |
Р2О5 |
|
|
|
|
|
|
||
+ |
|
|
C−R2 |
→ |
R1−С −O− С − R2 + H2O |
||||||
|
ОН |
H O |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
O |
|
O |
|||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
ангидрид |
|||||
При восстановлении карбоновых кислот получают альдегиды. Реакция протекает в жёстких условиях:
O |
[ H ] |
O H |
|
O |
|
R−С |
→ |
R−С |
→ R−C |
+ H2O |
|
ОН |
|
OH |
|
H |
|
|
|
H |
|
альдегид |
|
|
|
|
|
||
|
|
|
|
||
Представители монокарбоновых кислот:
насыщенные: O
H−C
OH
41

Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
-метановая /муравьиная/ кислота. Содержится в крапиве и выделениях муравьёв. При попадании на кожу вызывает ожоги.
O
H3C−C 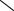
OH
-этановая /уксусная/ кислота - естественный метаболит, продукт уксуснокислого брожения сахаров. В медицине используется в виде солей.
O
H3C−CH2−CH2−C
OH
-бутановая /масляная/ кислота. Имеет неприятный запах, содержится в поте. ненасыщенные:
-простейшим представителем ненасыщенных монокарбоновых кислот является пропеновая /акриловая/ кислота. Её эфиры используются в производстве пластмасс для медицинского приборостроения.
Высшие /жирные/ карбоновые кислоты:
Насыщенные: пальмитиновая- C15H31COOH стеариновая- C17H35COOH
Ненасыщенные: олеиновая- |
C17H33COOH |
/одна= / |
линолевая- |
C17H31COOH |
/две= / |
линоленовая- |
C17H29COOH |
/три= / |
арахидоновая- |
C19H31COOH |
/четыре= / |
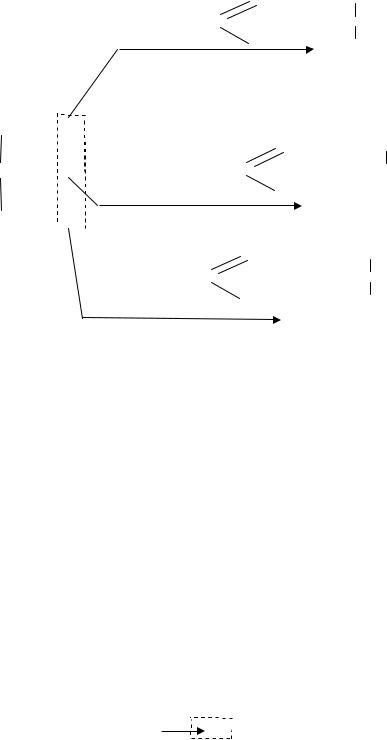
Жирные карбоновые кислоты при взаимодействии с трёхатомным спиртом глицерином образуют сложные эфиры- ацитилглицерины или глицериды. В зависимости от числа ОНгрупп глицерина, вступивших в реакцию ацилирования, различают моно-, ди- и триацилглицерины. Если ди- и триацилглицериды содержат остатки различных кислот, их называют смешанными:
42
|
Generated by Foxit PDF Creator © Foxit Software |
||||
|
http://www.foxitsoftware.com For evaluation only. |
||||
|
|
O |
|
||
O |
CH |
|
|
|
|
2−O−C−R |
|
|
|
||
1 |
|
||||
+ R−C |
CH |
OH |
+ H2O |
||
OH |
CH2OH |
|
|||
|
|
моноглицерид |
|
|||
CH2−O H |
O |
|
CH2−O−CO−R |
|
||
|
|
|
||||
CH − O H |
+2R−C |
CH−O−CO−R |
+ 2H2O |
|||
CH2− O H |
OH |
CH |
|
2OH |
|
|
|
|
|||||
|
|
|
|
диглицерид |
|
|
|
O |
CH2−O−CO−R |
|
|||
|
+3R−C |
CH−O−CO−R |
+ 3 H2O |
|||
|
OH |
CH2−O−CO−R |
|
|||
|
|
|
|
|
триглицерид |
|
Природные жиры и масла- это смесь различных смешанных триглицеридов. Дикарбоновые кислоты- это соединения с двумя карбоксильными группами .
Среди них также выделяют:
Насыщенные: НООС-СООН -этандиовая /щавелевая/ НООС-СН2-СООН -пропандиовая /малоновая/ НООС-(СН2)2-СООН -бутандиовая /янтарная/ НООС-(СН2)3-СООН - пентандиовая /глутаровая/
Ненасыщенные: НООС-СН=СН-СООН -бутендиовая и т.д.
Дикарбоновые кислоты вступают во все реакции, характерные для монокарбоновых кислот, с участием одной или обеих карбоксильных групп. Однако, для них известны также и специфические реакции:
1.декарбоксилирование- превращение дикарбоновой кислоты в монокарбоновую с выделением углекислого газа. Для организма особо важно ферментативное декарбоксилирование:
t
HOOC-CH2- COO H CO2↑ + HOOC-CH3
малоновая кислота |
уксусная кислота |
2.образование циклических ангидридов в результате внутримолекулярного отщепления воды:
43
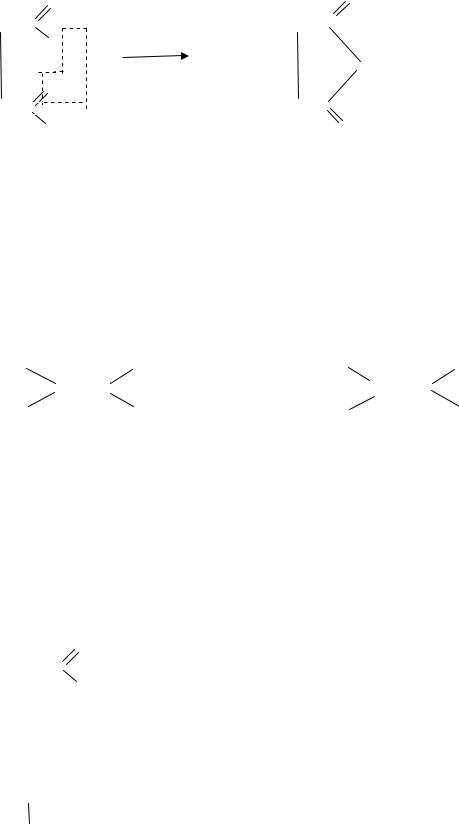
|
|
|
Generated by Foxit PDF Creator © Foxit Software |
|
|
|
http://www.foxitsoftware.com For evaluation only. |
|
|
O |
O |
H2C−C |
H2C−C |
||
|
|
O H |
t |
|
|
OH |
O + H2O |
H2C−C |
|
H2C−C |
|
|
O |
||
|
|||
|
|||
|
|
O |
|
янтарная кислота |
ангидрид янтарной кислоты |
||
Кроме этого, для ненасыщенных дикарбоновых кислот ещё характерен особый вид изомерии- геометрическая изомерия, обусловленная различным расположением в пространстве атомов относительно плоскости двойной связи. Различают цис- и транс-изомеры. В первом случае одинаковые группы атомов располагаются по одну сторону, во втором случаепо разные стороны плоскости двойной связи. Например, бутендиовая кислота существует в виде
двух изомеров: |
|
|
|
H |
H |
H |
COOH |
C = C |
|
|
C = C |
HOOC |
COOH |
HOOC |
H |
цис-изомер –малеиновая кислота |
транс-изомер- фумаровая кислота |
||
В отличие от фумаровой малеиновая кислота из-за сближенности в пространстве карбоксильных групп способна образовывать циклический ангидрид.
Фумаровая кислота широко рапространена в природе. Кроме этого, она - естественный метаболит, участник обменных процессов в организме.
Оксокислоты- это соединения, содержащие одновременно карбоксильную и карбонильную группы. Различают:
1. альдегидокислоты: O
HCOO − C |
-глиоксиловая кислота, |
||||
|
|
|
|
H |
содержится в недозрелых фруктах |
2. кетонокислоты: |
|
||||
H3C − C – COOH |
-пировиногдадная кислота |
||||
|
|
|
|
|
|
|
O |
|
|||
H3C – C – CH2 – COOH |
-ацетоуксуснаая кислота |
||||
|
|
|
|
|
|
O |
|
||||
HOOC – C− CH2 – COOH |
-щавелевоуксусная кислота |
||||
|
|
|
|
|
|
|
|
O |
|
|
|
44

Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
HOOC – C – (CH2)2 – COOH |
-α-кетоглутаровая кислота |
О
Кетонокислоты играют важную роль в биохимических процессах. Пировиноградная, щавелевоуксусная, α-кетоглутаровая кислоты участвуют в цикле трикарбоновых кислот. При их переаминировании образуются соответствующие α- аминокислоты. Пировиноградная кислота– промежуточный продукт молочнокислого и спиртового брожения углеводов. Ацетоуксусная кислота образуется в организме в процессе метаболизма высших жирных кислот и при окислении β- гидроксимасляной кислоты. Вместе с продуктами превращений она накапливается в организме у больных сахарным диабетом / ацетоновые или кетоновые тела/.
Гидрокикислоты – соединения, содержащие одновременно карбоксильную и гидроксильную группы.
O
НО-СН2-С
OH -2-гидроксиэтановая /гликолевая/ кислота.
Содержится во многих растениях, свекле, винограде.
H3C– CH – COOH
OH
-2-гидроксипропановая кислота /молочная/. Продукт молочнокислого брожения в организме. При интенсивной работе накапливается мышцах, вызывая характерную боль.
γβ α
НО-СН2-СН2-СН2-СООН -γ-гидроксимасляная кислота /ГОМК/ или 4-гидроксибутановая. Оказывает наркотическое действие. Применяется в виде натриевой соли как снотворное, а
также в качестве неингаляционного наркотического средства в анестезиологии.
βα
H3C – CH – CH2 – COOH
OH
-β-гидроксимасляная кислота или 3-гидроксибутановая. Промежуточный продукт окисления жирных кислот; предшественник ацетоуксусной кислоты. Накапливается в организме у больных сахарным диабетом.
Гидроксикислоты вступают во все типы химических реакций, характерные для кислот и спиртов, а также в специфические взаимодействия, обусловленные определённым взаимным расположением функциональных групп:
45
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
1.при нагревании от двух молекул α-гидроксикислот отщепляются две молекулы воды и образуется лактид:
|
α |
O |
|
R1 |
O |
||
R1 – CH – C |
|
|
CH – C |
||||
|
|
O H |
t |
O |
O + 2H2O |
||
O H |
O H |
|
|
C – CH |
|||
H O |
C– |
|
CH –R2 |
|
O |
R2 |
|
|
O |
|
|
|
лактид |
||
|
|
α |
|
|
|||
2.при нагревании β-гидроксикислот происходит внутримолекулярное отщепление молекулы воды. При этом образуется ненасыщенная кислота:
β |
α |
t |
||
R – CH – CH – COOH |
R – CH = CH – COOH + H2O |
|||
|
|
|
|
ненасыщенная кислота |
OH |
H |
|||
3.при нагревании γ-гидроксикислот также происходит внутримолекулярное отщепление воды, но при участии спиртовой и карбоксильной групп. При этом образуется циклическое соединение – лактон:
βα
H2C − CH2 |
|
H2C |
− CH2 |
|
|||
|
|
|
O |
t |
|
C=O |
+ H2O |
HC |
|
|
C |
|
HC − O |
|
|
|
|
|
|||||
|
|
|
OH |
|
|
|
|
R |
O H |
|
R |
|
|||
лактон Ещё одним свойством гидроксикислот является наличие у них оптических
изомеров. Это обусловлено явлением, которое называется «хиральность». Как отмечалось, sp3-гибридизованный атом углерода имеет тетраэдрическую конфигурацию. Причём, если из четырёх его заместителей хотя бы два одинаковы, то в таком тетраэдре существует плоскость симметрии, делящая молекулу на две зеркально-равные части. Если же все заместители различны - симметрия отсутствует. Хиральность - это способность молекул, не имеющих плоскости симметрии, существовать в виде пространственных изомеров. Эти изомеры являются по отношению друг к другу предметом и несовместимым с ним его зеркальным отображением.
Для возникновения в молекуле хиральности необходимо:
1.наличие центра хиральности, т.е. асимметрического атома углерода с четырьмя различными заместителями /С*/;
2.отсутствие плоскости и центра симметрии.
Выделяют два типа изомеров. Энантиомеры- это стереоизомеры, молекулы которых относятся между собой как предмет и несовместимое с ним его зеркальное отображение. Их обозначают как L и Д-изомеры. Они имеют
46
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
одинаковые химические и физические свойства, поэтому могут быть отделены друг от друга. Энантиомеры оптически активны, т.к. способны отклонять плоскость поляризованного света / на одинаковый угол, но в противоположные направления/.
Смесь равных количеств энантиомеров- рецемат оптической активностью не обладает.
Диастереомеры- стереоизомеры, молукулы которых не являются зеркальным отображением друг друга. Они имеют различные химические и физические свойства и могут быть отделены друг от друга. Диастереомеры содержат более одного центра хиральности и различаются между собой конфигурацией хотя бы одного из центров.
Для изображения энантио- и диастереомеров на плоскости используют проекционные формулы Фишера: в точке пересечения линий находится асимметрический атом углерода; вверху – старшая характеристическая группа /с минимальным номером/. По горизонтали обычно располагают неуглеродные заместители – H, NH2,OH. Например, молекулу молочной кислоты можно представить в виде двух энантиомеров:
H3C– C*H – COOH |
1 |
2 |
||||||
|
|
COOH |
COOH |
|||||
|
||||||||
|
|
|
|
|
|
|
|
|
|
OH |
H– C* –OH |
HO– |
|
C* –H |
|||
|
|
|||||||
|
|
|
|
CH3 |
|
|
||
|
|
|
|
CH3 |
||||
|
|
|
|
Д-ряд |
L-ряд |
|||
Абсолютная конфигурация, т.е. истинное расположение в пространстве заместителей у хирального центра определяется физико-химическими методами. Она была установлена для глицеринового альдегида, который
используется как |
стандарт для определения |
относительной конфигурации |
|||||||
/принадлежность к L или Д-ряду/ других молекул: |
|||||||||
глицериновый альдегид |
|
|
|
||||||
|
|
|
O |
|
|
|
|
|
|
C |
|
|
COH |
COH |
|||||
|
|||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
C*H OH |
H– C*–OH |
HO– |
|
||||
|
|
C*–H |
|||||||
|
|
CH2OH |
|
|
CH2OH |
|
|
||
|
|
CH2 OH |
|||||||
|
|
|
|||||||
|
|
|
|
Д-ряд, т.к. ОН-группа |
L-ряд, т.к. ОН-группа у |
||||
|
|
|
|
у хирального центра |
хирального центра –слева |
||||
|
|
|
|
справа. |
|
|
|
||
|
|
|
|
|
|
|
47 |
||
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
Исходя из этого, первый энантиометр молочной килоты относится к Д-ряду, второй к L-ряду.
Наличие стереоизомеров характерно и для других соединенийаминокислот, углеводов; причём, стереохимическое строение тесно связано с проявлением биологической активности.
48
Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
Тема 6 Углеводы
Ключевые слова и понятия: моносахориды, эпимеры, пиранозный цикл, фуранозный цикл
Углеводы широко распространены в природе. Наряду с липидами, белками, нуклеиновыми кислотами они являются важнейшими химическими соединениями растительного и животного мира. Углеводы составляют 2% от сухой массы животных организмов и 80% от сухой массы растений. Они присутствуют во всех частях человеческого организма (кровь, клеточная ткань, мозг, печень и т.д.). Например, гликоген – животный крахмал может составлять до 20% от общего веса печени. В одной бактериальной клетке присутствуют примерно 4 млн. молекул глюкозы и фруктозы, 2 млн. молекул рибозы и 4 млн. молекул дезоксирибозы.
Наиболее распространенный представитель углеводов – глюкоза содержится в растительных соках, плодах, фруктах. Это вещество – обязательный компонент крови и тканей живых организмов. Содержание глюкозы в крови поддерживается на постоянном уровне (гомеостаз). Резкие его колебания приводят к различным патологиям. Повышение уровня глюкозы в крови – гипергликемия наблюдается при сахарном диабете, остром панкреатите, эпилепсии, сотрясении головного мозга и др. Снижение уровня глюкозы – гипогликемия бывает при передозировке инсулина, онкологических заболеваниях, некоторых инфекционных и токсических поражениях печени и т.д. Пополнение глюкозы в организме происходит или с пищей, или за счет гликогена.
Углеводы выполняют многообразные функции:
Энергетическую. Энергия, выделяющаяся при метаболизме углеводов, запасается в виде АТФ и затем расходуется в процессе жизнедеятельности.
Структурную. Участвуют в построении клеточных стенок растений, бактерий, грибов.
Служат составными элементами важнейших веществ организма: нуклеиновых кислот, витаминов, ферментов, кофакторов.
Выступают в роли субстратов и регуляторов биохимических процессов.
Входят в состав многих лекарственных препаратов.
Являются главным компонентом пищи млекопитающих.
Участвуют в формировании иммунитета и осуществлении рецепторных функций.
Синтезируются углеводы растениями в процессе фотосинтеза из СО2 и Н2О. Они служат "мостом" между неорганическими и органическими веществами. Животные организмы не способны синтезировать углеводы и получают их с пищей растительного происхождения.
49

Generated by Foxit PDF Creator © Foxit Software
http://www.foxitsoftware.com For evaluation only.
Углеводы подразделяют на три класса:
1.Моносахариды или простые сахара – простейшие углеводы, не гидролизующиеся с образованием более простых углеводов.
2.Олигосахариды –углеводы, при гидролизе которых образуются от 2 до 10 моносахаридов.
3.Полисахариды – высокомолекулярные углеводы, при гидролизе которых образуются сотни и тысячи молекул моносахаридов.
Моносахариды
Моносахариды или монозы имеют общую формулу Сm(H2О)n , которая объясняет происхождение термина "углеводы".
Моносахариды – это полигетерофункциональные соединения. В их молекулах одновременно содержатся одна оксо-группа (альдегидная или кетонная) и несколько гидроксильных групп. То есть это полигидроксиальдегиды или полигидроксикетоны. Для них характерны неразветвленные углеродные цепи. В природе также встречаются производные моносахаридов, в молекулах которых вместо одной или нескольких ОН–групп содержатся другие заместители: –Н; –NH2 – SH (аминосахара, дезоксисахара).
Моносахариды классифицируют:
I. По характеру карбонильной группы:
с группой |
|
|
|
O |
с группой |
|
|
|
|
|
|
|
– кетозы |
|
|
C |
– альдозы |
C |
|
|
|
|
O |
||||
|
|
|
H |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
O |
|
CH 2OH |
|
||||||||
|
H |
|
C |
|
|
|
O |
|
|||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||
(CHOH)n
(CHOH)n
CH2OH
II. По числу атомов углерода в цепи:
CH 2OH
1. Триозы: |
альдотриозы |
кетотриозы |
|||||||
|
|
|
|
O |
|
|
|
|
|
|
|
C |
|
CH2OH |
|||||
|
|
|
|
H |
|
||||
|
|
|
|
||||||
|
H |
|
|
OH |
C |
|
|
O |
|
|
|
|
|
|
|||||
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
CH2OH |
||||||
|
глицериновый альдегид |
дигидроксиацетон – |
|||||||
простейшие представители моносахаридов.
2. Тетрозы: альдотетрозы и кетотетрозы – в природе встречаются редко.
50
