
- •Продуценты в биотехнологии Бактерии
- •Дрожжи (внетаксономическая группа грибов, утративших мицелиальное строение)
- •3.1. Смешанные культуры микроорганизмов. Использование. Типы взаимодействия между микроорганизмами в смешанной культуре.
- •3.2. Отличия биотехнологических процессов от химических. Обобщенные схемы основных производств микробиологического синтеза.
- •3.3. Биотехнология получения витаминов на примере витамина b12.
- •3.4. Общие показатели загрязненности сточных вод. Классификация методов очистки сточных вод.
- •4. Бактериальные и биологические загрязнения сточных вод
- •3.5. Среднее время пребывания потока в аппарате, как одна из основных характеристик кривых распределения. С- и f- кривые. Моменты с-кривой и их сущность.
- •4.1. Конкурентное ингибирование в периодической и хемостатной культуре.
- •4.2. Сорбционные методы выделения продуктов биосинтеза.
- •4.3. Уксусная кислота. Методы получения. Технология уксуснокислого брожения.
- •4.4. Ксенобиотики как загрязняющие факторы окружающей среды
- •1. Ксенобиотический профиль биогеоценоза
- •2. Пути переноса и трансформации ксенобиотиков
- •4. Ксенибиотики (кб) как зазрязняющие факторы ос. Основные источники поступления. Пути миграции и превращения.
- •5.1.Пищевая конкуренция в смешанных культурах. Влияние условий культивирования на состав популяций. Аутостабилизация фактора, ограничивающего развитие популяции.
- •5.2. Конструкции барботажных и барботажно-эрлифтных ферментеров.
- •5.2. Ферментеры газлифтные колонные и тарельчатые. Достоинства и недостатки.
- •5.3. Аминокислоты. Биосинтез, производство и характеристика лизина.
- •5.4 Аэробная очистка сточных вод. Последовательные стадии очистки.
- •5.6. Решение:
- •6.2. Сублимационная сушка.
- •6.3. Направленный синтез аминокислот и его регуляция. Ферментативная конверсия субстратов в аминокислоты.
- •6.4. Особенности микробиологической трансформации отдельных классов органических ксенобиотиков (пестициды, пав, органические галогенированные соединения).
- •7.1. Основные фазы роста и развития микробной культуры при периодическом культивировании.
- •7.3. Пищевая биотехнология. Производство молочных продуктов.
- •7.4. Микробиологические превращения металлов. Биосорбция металлов из растворов.
- •7.5. Аппаратурное оформление и основные принципы процесса ректификации.
- •8.1. Параметры роста культур микроорганизмов: скорость роста, время генерации, скорость деления, время удвоения. Эффективность биосинтеза.
- •8.2. Методы очистки и стерилизации воздуха. Аппаратурное оформление операций.
- •8.3.Продуценты белка
- •8.4. Характеристика анаэробных реакторов. Методика расчета менатенка. Области применения анаэробной очистки сточных вод. Сравнительный анализ эффективности работы аэробных и анаэробных реакторов.
- •8.5. Этапы процесса проектирования. Этапы создания детализированной технологической схемы, предварительной компоновки оборудования и корректировки начальной технологической схемы.
- •9.1. Особенности, условия и приемы культивирования изолированных тканей.
- •9.2. Экстракция. Применение в биотехнологии. Способы экстрагирования.
- •9.3. Спиртовое брожение. Производство этилового спирта. Области применения. Сырье, технологическая схема.
- •10.1. Одноступенчатое гомогенное культивирование микроорганизмов с рециркуляцией. Преимущества и недостатки.
- •10.2. Охрана труда, техника безопасности и санитарный контроль микробиологических производств.
- •10.3. Глутаминовая кислота: способы получения, биосинтез и схема получения.
- •10.4.Химия и использование бактериального окисления сульфидных минералов. Выщелачивание куч и отвалов, подземное выщелачивание
- •Механизм бактериального выщелачивания
- •Организация выщелачивания
- •10.5. Конструкции теплообменных аппаратов.
- •11.1 Влияние условий культивирования на скорость роста микроорганизмов.
- •11.2. Способы выделения биолологически активных веществ из биомассы микроорганизмов.
- •11.3. Лимонная кислота. Биосинтез. Технологическая схема производства.
- •11.4. Бактериальное выщелачивание.
- •11.5. Выпаривание. Температура кипения растворов (ткр). Температурная депрессия (тд). Технические методы выпаривания (тмв).
10.1. Одноступенчатое гомогенное культивирование микроорганизмов с рециркуляцией. Преимущества и недостатки.
Одним из недостатков хемостата является его склонность к вымыванию культуры. Действительно, для получения высокой производительности необходимо работать при оптимальной скорости разбавления Doпm, близкой к критической Dкр. В таких условиях при случайном уменьшении концентрации субстрата на входе или неточном задании протока D может начаться необратимое вымывание культуры из аппарата.
Для борьбы с этим явлением предложено использовать комплекс «ферментер—сепаратор» (рис. 9.14). В этом комплексе выходящая из ферментера жидкость сгущается на сепараторе, и часть сгущенного потока непрерывно возвращается в ферментер, остальная часть идет как товарный продукт. Осветленная жидкость сбрасывается в стоки.
Свежая среда поступает с расходом F0 и концентрацией субстрата S0 в ферментер с объемом рабочей жидкости V, где концентрации биомассы Хисубстрата Sиудельная скорость роста mu одинаковы в каждой его точке. Из-за рециркуляции жидкости из сепаратора (которую рассмотрим позже) поток из ферментера больше, чем входной; он равен F с концентрацией биомассы X.
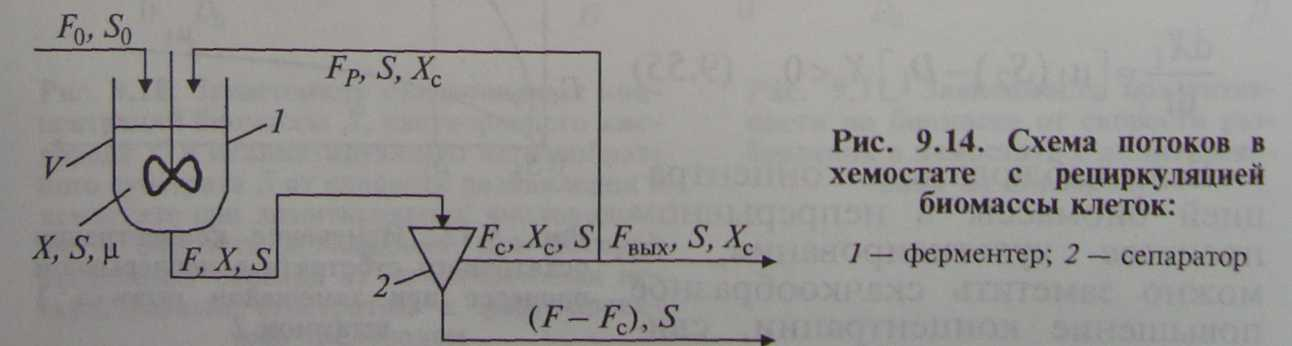
На сепараторе биомасса сгущается в b раз, т. е. ее концентрацияХс в выходном потоке равна bХ. Концентрация же субстрата при этом не меняется и составляет S. Из сепаратора выходят два потока: один — сгущенная биомасса с расходом Fc, второй — осветленная или отработанная жидкость с практически нулевой концентрацией биомассы. При этом расход отработанной жидкости составит (F- Fc) с концентрацией субстрата S.
Материальный баланс биомассы в сепараторе позволяет найти связь между Fcи F.
![]()
FP = aF0,
а — коэффициент рециркуляции, причем 0 <=а <=1.
Выходящий поток из системы Fвых равен:
Fвых=Fc-FP
С учетом (9.56) и (9.57) получаем:
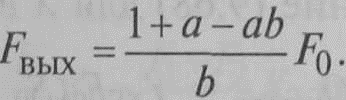
Поскольку по определению
XC = bX,
производительность комплекса «ферментер—сепаратор» равна:
Qкомпл = XC Fвых= (1 +a - ab)F0X.
Составляем материальный баланс по субстрату:
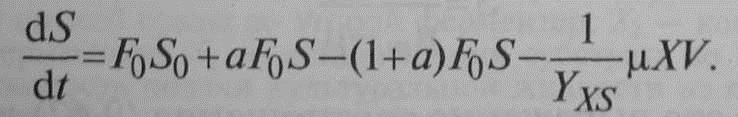
Принимая для стационарного состояния dS/dt= 0, получаем:
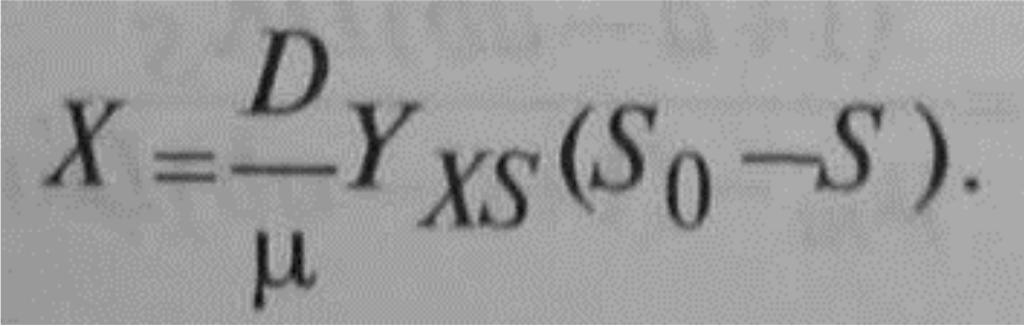
Материальный баланс биомассы в ферментере в стационарном состоянии:
![]()
Поскольку
F=F0 + FP
и скорость разбавления D равна
D= F0/V
D= F0из уравнений (9.64), (9.57), (9.60), (9.65) и (9.66) можно найти выражение для удельной скорости роста в ферментере:
mu = (1 + а - ab)D.
Поскольку b > 1 по определению, в данной системе удельная скорость роста микроорганизмов меньше скорости разбавления D (в одиночном хемостате эти величины равны).
Совместное решение уравнений (9.63) и (9.67) дает выражение для концентрации биомассы:
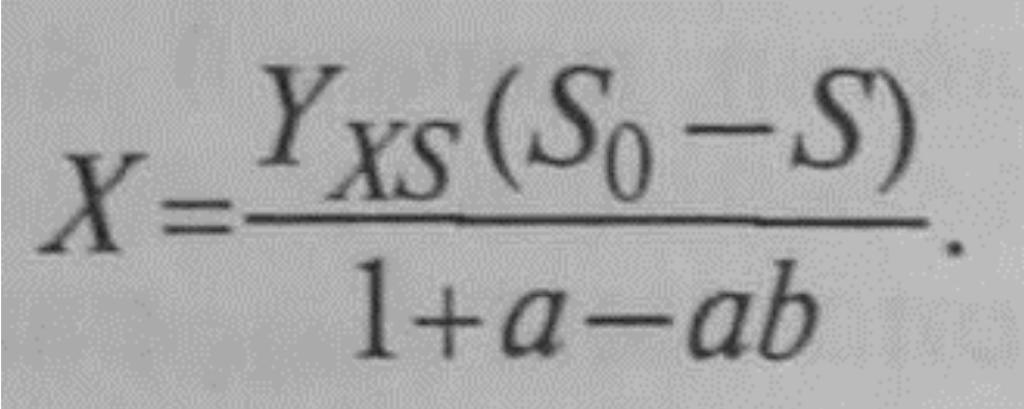
Поскольку b >1, концентрация биомассы при рециркуляции в ферментер выше, чем в обычном хемостате (при а = 0) и той же концентрации субстрата в исходной среде.
Подставляя выражение (9.68) для Хвуравнение (9.61), получаем:
Qкомпл = YXS F0 (S0 - S).
Связь концентрации субстрата в ферментере со скоростью разбавления можно определить исходя из уравнения Моно:
откуда

Подставляя в это выражение соотношение (9.67) для mu, получаем:

Из (9.72) следует, что при работе комплекса «ферментер—сепаратор» концентрация субстрата на выходе из ферментера S уменьшается по сравнению с обычным хемостатом (при а = 0), а производительность системы по биомассе Qкомпл при этом увеличивается.
Отсюда вытекают основные направления использования рассматриваемого комплекса:
повышение производительности системы непрерывного культивирования, если этого невозможно достичь просто за счет повышения исходной концентрации субстрата S0, например при очистке сточных вод или утилизации малоконцентрированных растворов субстрата;
более полное потребление из среды субстрата.
