
- •Продуценты в биотехнологии Бактерии
- •Дрожжи (внетаксономическая группа грибов, утративших мицелиальное строение)
- •3.1. Смешанные культуры микроорганизмов. Использование. Типы взаимодействия между микроорганизмами в смешанной культуре.
- •3.2. Отличия биотехнологических процессов от химических. Обобщенные схемы основных производств микробиологического синтеза.
- •3.3. Биотехнология получения витаминов на примере витамина b12.
- •3.4. Общие показатели загрязненности сточных вод. Классификация методов очистки сточных вод.
- •4. Бактериальные и биологические загрязнения сточных вод
- •3.5. Среднее время пребывания потока в аппарате, как одна из основных характеристик кривых распределения. С- и f- кривые. Моменты с-кривой и их сущность.
- •4.1. Конкурентное ингибирование в периодической и хемостатной культуре.
- •4.2. Сорбционные методы выделения продуктов биосинтеза.
- •4.3. Уксусная кислота. Методы получения. Технология уксуснокислого брожения.
- •4.4. Ксенобиотики как загрязняющие факторы окружающей среды
- •1. Ксенобиотический профиль биогеоценоза
- •2. Пути переноса и трансформации ксенобиотиков
- •4. Ксенибиотики (кб) как зазрязняющие факторы ос. Основные источники поступления. Пути миграции и превращения.
- •5.1.Пищевая конкуренция в смешанных культурах. Влияние условий культивирования на состав популяций. Аутостабилизация фактора, ограничивающего развитие популяции.
- •5.2. Конструкции барботажных и барботажно-эрлифтных ферментеров.
- •5.2. Ферментеры газлифтные колонные и тарельчатые. Достоинства и недостатки.
- •5.3. Аминокислоты. Биосинтез, производство и характеристика лизина.
- •5.4 Аэробная очистка сточных вод. Последовательные стадии очистки.
- •5.6. Решение:
- •6.2. Сублимационная сушка.
- •6.3. Направленный синтез аминокислот и его регуляция. Ферментативная конверсия субстратов в аминокислоты.
- •6.4. Особенности микробиологической трансформации отдельных классов органических ксенобиотиков (пестициды, пав, органические галогенированные соединения).
- •7.1. Основные фазы роста и развития микробной культуры при периодическом культивировании.
- •7.3. Пищевая биотехнология. Производство молочных продуктов.
- •7.4. Микробиологические превращения металлов. Биосорбция металлов из растворов.
- •7.5. Аппаратурное оформление и основные принципы процесса ректификации.
- •8.1. Параметры роста культур микроорганизмов: скорость роста, время генерации, скорость деления, время удвоения. Эффективность биосинтеза.
- •8.2. Методы очистки и стерилизации воздуха. Аппаратурное оформление операций.
- •8.3.Продуценты белка
- •8.4. Характеристика анаэробных реакторов. Методика расчета менатенка. Области применения анаэробной очистки сточных вод. Сравнительный анализ эффективности работы аэробных и анаэробных реакторов.
- •8.5. Этапы процесса проектирования. Этапы создания детализированной технологической схемы, предварительной компоновки оборудования и корректировки начальной технологической схемы.
- •9.1. Особенности, условия и приемы культивирования изолированных тканей.
- •9.2. Экстракция. Применение в биотехнологии. Способы экстрагирования.
- •9.3. Спиртовое брожение. Производство этилового спирта. Области применения. Сырье, технологическая схема.
- •10.1. Одноступенчатое гомогенное культивирование микроорганизмов с рециркуляцией. Преимущества и недостатки.
- •10.2. Охрана труда, техника безопасности и санитарный контроль микробиологических производств.
- •10.3. Глутаминовая кислота: способы получения, биосинтез и схема получения.
- •10.4.Химия и использование бактериального окисления сульфидных минералов. Выщелачивание куч и отвалов, подземное выщелачивание
- •Механизм бактериального выщелачивания
- •Организация выщелачивания
- •10.5. Конструкции теплообменных аппаратов.
- •11.1 Влияние условий культивирования на скорость роста микроорганизмов.
- •11.2. Способы выделения биолологически активных веществ из биомассы микроорганизмов.
- •11.3. Лимонная кислота. Биосинтез. Технологическая схема производства.
- •11.4. Бактериальное выщелачивание.
- •11.5. Выпаривание. Температура кипения растворов (ткр). Температурная депрессия (тд). Технические методы выпаривания (тмв).
4.1. Конкурентное ингибирование в периодической и хемостатной культуре.
Скорость протекания биохимических реакций, катализируемых ферментами, часто зависит не только от природы и концентрации фермента и субстрата, но и от присутствия некоторых веществ — ингибиторов или активаторов. В живой природе ингибирование и активация ферментов и ферментных систем являются важнейшими способами регулирования метаболизма и приспособления к условиям окружающей среды.
Значительный теоретический и практический интерес представляют два варианта ингибирования, получивших название конкурентного и неконкурентного. Перт предложил исследовать действие ингибитора через потребление субстрата все вещества м/б разделены на две группы:
Конкурентный ингибитор к применению роста МО не снижает скорость роста, но снижает сродство к субстрату, т.е. увеличивает KS.
Неконкурентный ингибитор не влияет на KS, но снижает скорость роста.
В этих случаях константу равновесия KR .принято обозначить KI - константа ингибирования. Как и KS Ki численно равна концентрации ингибитора, замедляющего рост МО вдвое.

Полное конкурентное ингибирование имеет место в тех случаях, когда ингибитор препятствует образованию фермент-субстратного комплекса в результате «конкуренции» за активный центр фермента. С точки зрения общей схемы (1) это означает, что комплекс RES не может существовать, т. е. α , а значение β не определено, т. к. этот путь образования продуктов исключен (рис. 2):
Кинетическое описание полного конкурентного ингибирования при переходе к пределу при α :

[1]

Зависимость (1) имеет форму уравнения Михаэлиса — Ментен, причем характерно, что измененной оказывается лишь константа KM, тогда как rMAX остается без изменений. Это указывает на то, что при любой концентрации ингибитора экспериментальные данные по зависимости r0 от S0 должны образовывать в координатах Лайнуивера — Берка прямую, пересекающую ось ординат в точке l/rMAX. В серии экспериментов при изменяющихся концентрациях ингибитора будет получаться пучок прямых (рис. 3), пересекающихся в одной точке на оси ординат, отсекая отрезок 1/rMAX. Поскольку каждая из прямых будет отсекать на оси абсцисс отрезок, равный – 1/КМ, то из найденных этим способом значений КМ легко найти Ks и Ki, строя линейную зависимость в координатах КМ_ЭКСП = f (I):
![]()
[2]

Если значения rМАХ и Ks для фермента известны и требуется найти лишь константу ингибирования Ki, удобно использовать координаты Диксона, связывающие 1/г0 с [I].
![]()
[3]
т. е. в координатах l/r0 = f(I) можно получить пучок прямых, угол наклона которых будет определяться начальной концентрацией субстрата (рис. 3.1). Нетрудно увидеть, что при I = — KI все прямые, описываемые выражением (3), проходят через точку с абсциссой — KI и ординатой l/rMAX. Это свидетельствует о том, что при полном конкурентном ингибировании серия экспериментов по зависимости начальной скорости реакции от концентрации ингибитора при различных начальных концентрациях субстрата и постоянном значении Е0 дает в координатах Диксона пучок прямых, пересекающихся в одной точке. Ее абсцисса позволяет найти константу нестойкости комплекса фермент — ингибитор KI.
Из культивирования:
Для конкурентного ингибитора:
μ = μmaxS/(αKS + S), где α= 1 + I/Ki
при I – концентрация ингибитора.
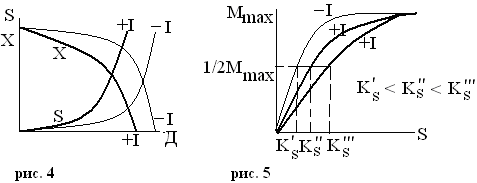
В периодической культуре ингибитор расширяет фазу затухания роста:

