
- •Дніпродзержинський державний технічний університет
- •Конспект лекцій
- •«Аналітична хімія та інструментальні методи аналізу»
- •«Кількісний аналіз. Хімічні методи кількісного аналізу»
- •6.051401 „Біотехнологія»,
- •6.051301 “Хімічна технологія»
- •2.1 Кількісний аналіз. Метрологічні характеристики методів аналізу
- •2.2 Гравіметрія(ваговий аналіз)
- •2.3 Титриметрія(об’ємний аналіз)
- •2.4 Кислотно-основне титрування
- •2.5С принципи розрахунку кривих титрування
- •2.6 Окисно-відновне титрування
- •2.7С методи редоксиметрії
- •2.8С методи осадження в титриметрії
- •2.9 Комплексонометрія
- •Література
- •51918 М. Дніпрдзержинськ,
2.8С методи осадження в титриметрії
Сутність методів. Аргентометрія. Роданометрія. Меркурометрія. Меркуриметрія. Сульфатометрія. Визначаємі речовини. Стандартні розчини. Індикатори методів осадження.
Методи
осадження
при титруванні засновані на використанні
реакцій, які супроводжуються утворенням
малорозчинних сполук. Кількісне утворення
осаду залежить від його розчинності,
яка визначається добутком розчинності
(ДР). Якщо виходити з необхідності
досягнення практично повного осадження,
то для цього методу можна використовувати
реакції, які дають осад з добутком
розчинності менш ніж 110-8
(для найпростішого випадку при однаковій
зарядності іонів, наприклад
![]() ).
Крім того, реакції утворення осаду
повинні перебігати швидко, процеси
соосадження повинні бути відсутні, а
точка еквівалентності повинна фіксуватися
чітко. Найбільш поширені такі методи
осадження:
).
Крім того, реакції утворення осаду
повинні перебігати швидко, процеси
соосадження повинні бути відсутні, а
точка еквівалентності повинна фіксуватися
чітко. Найбільш поширені такі методи
осадження:
Аргентометрія.
Використовується для аналізу хлоридів,
бромідів, йодідів лужних і лужноземельних
металів, а також солей аргентуму.
При цьому утворюються малорозчинні
осади AgCl(ДР=1,8*10-10);
AgBr(ДР=4,9*10-13);
AgI(ДР=1*10-16).
Також цей метод може бути використаний
для аналізу ціанідів з утворенням
![]() і роданідів з утворенням
і роданідів з утворенням
![]() .
Стандартним розчином у аргентометрії
є розчин
.
Стандартним розчином у аргентометрії
є розчин
![]() з концентрацією 0,1н, 0,05н, 0,02н чи 0,01н.
Іноді для визначення
з концентрацією 0,1н, 0,05н, 0,02н чи 0,01н.
Іноді для визначення
![]() використовують
титрантом 0,1н розчин
використовують
титрантом 0,1н розчин
![]() чи
чи
![]() Титр розчину
встановлюють по
чи
,
які перекристалізують та висушують до
сталої маси.
Титр розчину
встановлюють по
чи
,
які перекристалізують та висушують до
сталої маси.
Роданометрія (Метод Фольгарда). Використовується для визначення солі аргентуму. Метод заснований на реакції:
![]() .
.
Титрантом
використовуються 0,1н розчин
![]() .
Крім того, методом зворотного титрування
можна визначати галогеніди і роданіди.
Індикатор у роданометрії – солі
.
Крім того, методом зворотного титрування
можна визначати галогеніди і роданіди.
Індикатор у роданометрії – солі
![]() ,
які підкислені
,
які підкислені
![]() .
Біля точки еквівалентності аналізуємий
розчин при надлишку
забарвлюється у червоний колір внаслідок
утворення комплексного іону
.
Біля точки еквівалентності аналізуємий
розчин при надлишку
забарвлюється у червоний колір внаслідок
утворення комплексного іону
![]() :
:
![]() .
.
Меркурометрія заснована на титруванні розчинів хлоридів і йодідів титрантом – розчином Hg2(NO3)2:
![]() .
.
Добуток
розчинності
![]() .
Цей метод економніше і більш чутливий
ніж аргентометрія, але при його
використанні слід бути вельми обережним,
тому що солі гідраргіруму отруйні.
Індикатором використовують роданід
феруму, який здобувають у титруємому
розчині додаючи 1 мл 0,05н
і 2 мл концентрованого розчину
.
Цей метод економніше і більш чутливий
ніж аргентометрія, але при його
використанні слід бути вельми обережним,
тому що солі гідраргіруму отруйні.
Індикатором використовують роданід
феруму, який здобувають у титруємому
розчині додаючи 1 мл 0,05н
і 2 мл концентрованого розчину
![]() .
.
З’являється
червоне забарвлення внаслідок утворення
.
Коли усі галогени будуть пов’язані
розчин знебарвлюється внаслідок
осадження іонів
![]() у
вигляді важкорозчинної сполуки
у
вигляді важкорозчинної сполуки
![]()
![]()
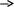
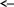
![]() .
.
При титруванні роблять контрольний дослід і віднімають від результату титрування об’єм титранту, який пішов на взаємодію з індикатором.
Меркуриметрія
заснована на використанні титранту
![]() .
Цим методом визначаються хлориди,
броміди, ціаніди, роданіди, які з іонами
.
Цим методом визначаються хлориди,
броміди, ціаніди, роданіди, які з іонами
![]() утворюють слабо дисоційовану сполуку:
утворюють слабо дисоційовану сполуку:
![]()
![]() .
.
Індикаторами використовують нітропрудис натрію (титрують до появи муті, яка не зникає з часом) чи дифенілкарбазон (титрування закінчують при появі інтенсивно синього кольору).
Цей метод також потребує уважності і використання спеціальних засобів безпеки внаслідок отруйності солей .
Сульфатометрія
використовується
для аналізу солей барію, титруванням
їх
![]() .
При цьому утворюється осад
.
При цьому утворюється осад
![]() .
Також ним можна визначати сульфати
титруванням
.
Також ним можна визначати сульфати
титруванням
![]() чи
чи
![]() .
Індикаторами використовують метало
хромні індикатори нитрохромазо та
ортаніловий А. Вони у вільному стані
мають рожевий колір і з іонами
.
Індикаторами використовують метало
хромні індикатори нитрохромазо та
ортаніловий А. Вони у вільному стані
мають рожевий колір і з іонами
![]() утворюють
комплексну сполуку фіолетового кольору.
Титрування виконують у кислому середовищі
при
утворюють
комплексну сполуку фіолетового кольору.
Титрування виконують у кислому середовищі
при
![]() .
При титруванні солі барію
колір розчину у точці еквівалентності
змінюється з фіолетового у рожевий.
Якщо титрують сульфати то навпаки – у
точці еквівалентності колір змінюється
з рожевого у фіолетовий.
.
При титруванні солі барію
колір розчину у точці еквівалентності
змінюється з фіолетового у рожевий.
Якщо титрують сульфати то навпаки – у
точці еквівалентності колір змінюється
з рожевого у фіолетовий.
Сульфатометрія дозволяє визначати сульфати просто і швидко і замінює поступово незручний гравіметричний метод.
Самостійно опрацювати тему більш детальніше за літературою:
[2] – стор. 78-90; [4] – стор. 96-101; [8] – стор. 224-252.
Контрольні питання до теми 2.8С
8.1.На чому засновано метод осадження в титриметрії?
8.2.Які вимоги до реакції що застосовують в методі осадження?
8.3.Аргентометрія. Визначаємі речовини. Стандартні розчини. Індикатори.
8.4.Роданометрія. Визначаємі речовини. Стандартні розчини. Індикатори.
8.5.Меркурометрія. Визначаємі речовини. Стандартні розчини. Індикатори.
8.6.Меркуриметрія. Визначаємі речовини. Стандартні розчини. Індикатори.
8.7.Сульфатометрія. Визначаємі речовини. Стандартні розчини. Індикатори.
