- •Физические свойства
- •Химические свойства
- •I тип реакций. Реакции, характерные для органических кислот.
- •II тип реакции. Восстановление сульфогруппы
- •III тип реакций. Реакции нуклеофильного замещения сульфогруппы
- •IV тип реакций. Реакции электрофильного замещения в ядре идут в соответствии с правилами замещения
- •4.6.1.Нитросоединения ароматического ряда
- •1.Нитросоединения с нитрогруппой в ядре
- •Физические свойства
- •Химические свойства
- •II. Реакции в ядре
- •II. Нитросоединения с группой no2 в боковой цепи
- •Способы получения
- •Химические свойства ароматических нитросоединений с группой no2 в боковой цепи
- •4.6.1.Ароматические амины Классификация
- •I. По положению аминогруппы относительно ароматического ядра.
- •II. По количеству радикалов, связанных с азотом
- •III. По количеству аминогрупп
- •Получение
II. Реакции в ядре
1) Реакции электрофильного замещения в ароматическом ядре.
Происходят в м-положении к нитрогруппе (т.к. это заместитель II рода) и протекает значительно труднее, чем у углеводородов.
а) галоидирование
|
(Fe) + Br2 HBr + t0 |
|
|
|
м-бромнитробензол
|
б) нитрование – требует более высокой температуры.
в) сульфирование – только олеумом или хлорсульфоновой кислотой (т.е. хлорангидрид серной кислоты).
2) Реакции нуклеофильного замещения в ароматическом ядре.
Являясь сильным электроноакцептором, нитрогруппа понижает электронную плотность кольца и особенно сильно в о- и п-положении, поэтому в этих положениях могут довольно легко идти реакции нуклеофильного замещения, которые почти не имеют места у ароматических углеводородов.
а) нуклеофильное замещение водорода в о- или п-положении к нитрогруппе.
Взаимодействие со щелочами
|
t0 + KOH H2 + (тв.) |
|
|
|
О-нитрофенолят калия |
Нуклеофильное замещение идет легче, если в молекуле имеются две нитрогруппы в м-положении.
|
+ KOH H2 + (раствор) |
|
м-динитробензол |
|
2,6-динитрофенолят калия ярко-фиолетовое окрашивание |
б) нуклеофильное замещение других атомов или групп, находящихся в о- или п-положениях к нитрогруппе (особенно легко замещаются галогены в о- или п-положении к нитрогруппе).
|
+ KOH KCl + (водный) |
|
о-хлорнитробензол |
|
о-нитрофенол |
Реакция с замещением галоида в этом случае идет легко.
II. Нитросоединения с группой no2 в боковой цепи
Например, фенилнитрометан C6H5-CH2-NO2
или метилфенилнитрометан (1-фенил-1-нитроэтан)

Способы получения
1. Нитрование гомологов бензола в условиях реакции Коновалова (действие разбавленной азотной кислоты при нагревании).
2. Замещение галогена в боковой цепи на NO2.
C6H5-CH2Cl + NaNO2 C6H5-CH2NO2 + NaCl
хлористый бензил нитрит натрия фенилнитрометан
Химические свойства ароматических нитросоединений с группой no2 в боковой цепи
По свойствам сходны с нитросоединениями
жирного ряда, но обладают большей
склонностью к изомеризации в аци-форму,
т.к. обладают исключительной подвижностью
водорода в
![]() -положении
к группе NO2.
-положении
к группе NO2.
|
|
|
+NaOH H2O +
|
|
нейтральная форма (фенилнитрометан) |
|
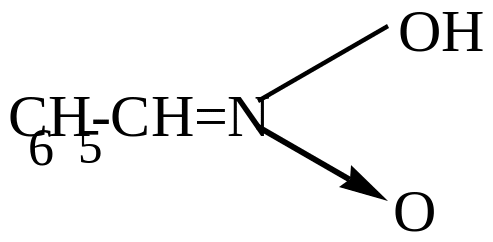
аци-форма |
|
натриевая соль аци-формы |
таутомеры |
|
|
||
При подкислении соли аци-формы ее можно выделить в свободном состоянии.
|
+ HCl NaCl + |
|
Способность аци-формы существовать в
свободном состоянии обуславливается
сопряжением двойной связи с
![]() -электронами
ароматического ядра и неподеленной
парой р-электронов кислорода гидроксильной
группы.
-электронами
ароматического ядра и неподеленной
парой р-электронов кислорода гидроксильной
группы.