
- •1)Биогенные элементы.Классификация, участие в химических процессах в организме.
- •2) Человек и биосфера. Понятие об эндемических заболеваниях, микроэлементозах.
- •3) Характеристика кислотно-основных, о-в, комплексообразовательных свойств соединений s, p, d-элементов.
- •2.3.1. Окислительно-восстановительные свойства
- •2. 3. 2. Кислотно-основные свойства (свойства оксидов и гидроксидов, образуемых d–элементами)
- •2.3.3. Реакции комплексообразования
- •4) Химические св-ва одно-, двух- и трёхатомных спиртов, кислотно-основные, электрофильные-с-алкилирование, с-ацетилирование, окисления. Написать уравнения реакций.
- •Свойства спиртов
- •Реакции с разрывом связи о—н:
- •Реакции, сопровождающиеся разрывом связи с—о:
- •5) Химические свойства одно-, двух- и трёхатомных фенолов, кислотно-основные, электрофильные: с-алкилирование, с-ацетилирование, окисление, восстановление. Напишите уравнения реакций.
- •9. Химические свойства фенола (карболовой кислоты)
- •I. Свойства гидроксильной группы
- •II. Свойства бензольного кольца
- •2). Гидрирование фенола
- •III. Качественная реакция - обнаружение фенола
- •6) Химические свойства кетонов, альдегидов: реакции нуклеофильного присоединения, восстановления, окисления. Уравнения реакций.
- •10) Олигосахариды.Дисахариды мальтоза, целлобиоза, лактоза, сахароза.Строение, номенклатура, цикло-оксо-таутомерия. Восстанавливающие свойства. Гидролиз кислотный и ферментативный.
- •2. Дисахариды
- •2.1. Строение
- •2.2. Химические свойства
- •13) Строение, номенклатура, стереоизомерия аминокислот.Классификация аминокислот: химические (по природе радикала и содержащихся в нём заместителей, по полярности радикалов) и биолгическая.
- •3.3. Кислотно-основные свойства.
- •15) Строение, номенклатура, образование аминокислот из кетокислот (восстановительное амминирование и трансамминирование)
- •3.4. Реакции аминокислот in vivo
- •17) Понятие о белках.Классификация белков(химическая и биологическая) Биологическая роль белков. Строение и свойства пептидной связи.
- •18) Уровни структурной организации белков. Уровни организации
17) Понятие о белках.Классификация белков(химическая и биологическая) Биологическая роль белков. Строение и свойства пептидной связи.
Аминокислоты соединяются друг с другом ковалентной пептидной связью. Образование ее происходит за счет a-аминогруппы (–NH2) одной аминокислоты и a-карбоксильной (–СООН) группы другой с выделением молекулы воды.
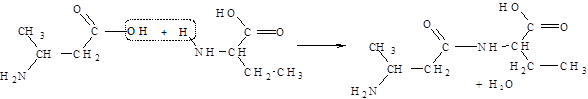
В результате реакции поликонденсации можно получить соединения, составленные из многих аминокислотных остатков – полипептиды.
Каждый пептид содержит только одну свободную a-амино- и a-карбоксильную группу, которые находятся на концевых остатках аминокислот. Эти группы и R-группы некоторых аминокислот могут быть ионизированы, поэтому пептиды могут нести заряды, и могут быть электронейтральными (т.е. иметь изоэлектрическую точку (ИЭТ).
По форме частиц белки делят на фибриллярные (волокнистые) и глобулярные (корпускулярные).
Белки в зависимости от сложности химического строения делят на простые и сложные. Простые белки при гидролизе распадаются только на аминокислоты. При гидролизе сложных белков наряду с аминокислотами образуется вещество небелковой природы – простетическая группа.
Классификация простых белков основана на их растворимости.
Альбумины – водорастворимые белки с высокой гидрофильностью, выпадают в осадок при 100%-ом насыщении сульфатом аммония. К этим белкам относятся белок куриного яйца, белки зародыша семян злаковых и бобовых культур.
Глобулины – растворяются в солевых растворах. Они осаждаются 50%-ным раствором сульфата аммония.
Проламины- эти белки растворяются в 60-80%-ом растворе этилового спирта.
Глютелины растворяются они в щелочах (чаще 0,2%-ым NaOH). Наиболее исследованы глютелин пшеницы.
Протеиды – сложные белки, в которых белок связан с веществом небелковой природы – простетической группой. В зависимости от химической природы простетической группы их делят на липопротеины, гликопротеины, хромопротеины, нуклеопротеины, фосфопротеины, металлопротеины.
В липопротеинах простетическая группа представлена каким-либо липидом.
Гликопротеины – в качестве простетической группы содержат углеводный компонент. Это могут быть глюкоза, манноза.
Хромомпротеины – состоят из простого белка и связанного с ним окрашеного небелкового компонента.
Нуклеопротеины – одна из самых важных групп белков, состоящая из простых белков связанных с нуклеиновыми кислотами. Эти белки играют первостепенную роль в хранении и передаче генетической информации и биосинтезе белка и содержаться в основном в ядрах клеток.
Фосфопротеины – эти белки содержат органически связанный, лабильный фосфат, абсолютно необходимый для выполнения клеткой ряда биологических функций.
Металлопротеины наряду с белком содержат ионы какого-либо металла или нескольких металлов.
Классификация белков в соответствии с выполняемыми функциями: каталитически активные белки, белки-гормоны, белки-регуляторы активности генома, защитные белки, токсичные белки, транспортные белки, мембранные белки, рецепторные белки, белки-ингибиторы ферментов, белки вирусных оболочек.
Биологическую роль, я думаю, все напишут!
