
- •1)Биогенные элементы.Классификация, участие в химических процессах в организме.
- •2) Человек и биосфера. Понятие об эндемических заболеваниях, микроэлементозах.
- •3) Характеристика кислотно-основных, о-в, комплексообразовательных свойств соединений s, p, d-элементов.
- •2.3.1. Окислительно-восстановительные свойства
- •2. 3. 2. Кислотно-основные свойства (свойства оксидов и гидроксидов, образуемых d–элементами)
- •2.3.3. Реакции комплексообразования
- •4) Химические св-ва одно-, двух- и трёхатомных спиртов, кислотно-основные, электрофильные-с-алкилирование, с-ацетилирование, окисления. Написать уравнения реакций.
- •Свойства спиртов
- •Реакции с разрывом связи о—н:
- •Реакции, сопровождающиеся разрывом связи с—о:
- •5) Химические свойства одно-, двух- и трёхатомных фенолов, кислотно-основные, электрофильные: с-алкилирование, с-ацетилирование, окисление, восстановление. Напишите уравнения реакций.
- •9. Химические свойства фенола (карболовой кислоты)
- •I. Свойства гидроксильной группы
- •II. Свойства бензольного кольца
- •2). Гидрирование фенола
- •III. Качественная реакция - обнаружение фенола
- •6) Химические свойства кетонов, альдегидов: реакции нуклеофильного присоединения, восстановления, окисления. Уравнения реакций.
- •10) Олигосахариды.Дисахариды мальтоза, целлобиоза, лактоза, сахароза.Строение, номенклатура, цикло-оксо-таутомерия. Восстанавливающие свойства. Гидролиз кислотный и ферментативный.
- •2. Дисахариды
- •2.1. Строение
- •2.2. Химические свойства
- •13) Строение, номенклатура, стереоизомерия аминокислот.Классификация аминокислот: химические (по природе радикала и содержащихся в нём заместителей, по полярности радикалов) и биолгическая.
- •3.3. Кислотно-основные свойства.
- •15) Строение, номенклатура, образование аминокислот из кетокислот (восстановительное амминирование и трансамминирование)
- •3.4. Реакции аминокислот in vivo
- •17) Понятие о белках.Классификация белков(химическая и биологическая) Биологическая роль белков. Строение и свойства пептидной связи.
- •18) Уровни структурной организации белков. Уровни организации
18) Уровни структурной организации белков. Уровни организации
![]()
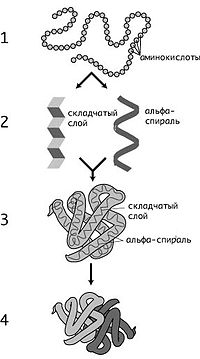
Уровни структуры белков: 1 — первичная, 2 — вторичная, 3 — третичная, 4 — четвертичная
Кроме последовательности аминокислот полипептида (первичной структуры), крайне важна третичная структура белка, которая формируется в процессе фолдинга (от англ. folding, «сворачивание»). Третичная структура формируется в результате взаимодействия структур более низких уровней. Выделяют четыре уровня структуры белка[14]:
Первичная структура — последовательность аминокислот в полипептидной цепи. Важными особенностями первичной структуры являются консервативные мотивы — сочетания аминокислот, играющих ключевую роль в функциях белка. Консервативные мотивы сохраняются в процессе эволюции видов, по ним часто удаётся предсказать функцию неизвестного белка.
Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями. Ниже приведены самые распространённые типы вторичной структуры белков:
α-спирали — плотные витки вокруг длинной оси молекулы, один виток составляют 3,6 аминокислотных остатка, и шаг спирали составляет 0,54 нм[15] (так что на один аминокислотный остаток приходится 0,15 нм), спираль стабилизирована водородными связями между H и O пептидных групп, отстоящих друг от друга на 4 звена. Спираль построена исключительно из одного типа стереоизомеров аминокислот (L). Хотя она может быть как левозакрученной, так и правозакрученной, в белках преобладает правозакрученная. Спираль нарушают электростатические взаимодействия глутаминовой кислоты, лизина, аргинина. Расположенные близко друг к другу остатки аспарагина, серина, треонина и лейцина могут стерически мешать образованию спирали, остатки пролина вызывают изгиб цепи и тоже нарушают α-спирали.
β-листы (складчатые слои) — несколько зигзагообразных полипептидных цепей, в которых водородные связи образуются между относительно удалёнными друг от друга (0,347 нм на аминокислотный остаток[15]) в первичной структуре аминокислотами или разными цепями белка, а не близко расположенными, как имеет место в α-спирали. Эти цепи обычно направлены N-концами в противоположные стороны (антипараллельная ориентация). Для образования β-листов важны небольшие размеры боковых групп аминокислот, преобладают обычно глицин и аланин.
π-спирали;
310-спирали;
неупорядоченные фрагменты.
Третичная структура — пространственное строение полипептидной цепи (набор пространственных координат составляющих белок атомов). Структурно состоит из элементов вторичной структуры, стабилизированных различными типами взаимодействий, в которых гидрофобные взаимодействия играют важнейшую роль. В стабилизации третичной структуры принимают участие:
ковалентные связи (между двумя остатками цистеина — дисульфидные мостики);
ионные связи между противоположно заряженными боковыми группами аминокислотных остатков;
водородные связи;
гидрофильно-гидрофобные взаимодействия. При взаимодействии с окружающими молекулами воды белковая молекула «стремится» свернуться так, чтобы неполярные боковые группы аминокислот оказались изолированы от водного раствора; на поверхности молекулы оказываются полярные гидрофильные боковые группы.
Четвертичная структура (или субъединичная, доменная) — взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру. В состав белка с четвертичной структурой могут входить как идентичные, так и различающиеся полипептидные цепочки. В стабилизации четвертичной структуры принимают участие те же типы взаимодействий, что и в стабилизации третичной. Надмолекулярные белковые комплексы могут состоять из десятков молекул.
